SỬ DỤNG THUỐC KHÁNG GIÁP TỔNG HỢP
TRONG THỜI KỲ CHO CON BÚ
BS Nguyễn Thị Giang, BSCK2 Nguyễn Thị Hồ Lan, BS Nguyễn Mạnh Hà
Khoa Nội Chung – Bệnh viện Nội tiết Trung ương
SUMMARY
Use of Antithyroid Drugs in
Breastfeeding period
Antithyroid drugs (ATD) are widely used for the treatment of Graves’ disease (GD) in the general population. Over the past decade there has been an increasing awareness that several disturbances of thyroid function may occur in mothers after delivery which may be more prevalent than previously appreciated. Exacerbation of immune reactions occurs 3–12 month following delivery. Management of hyperthyroidism during lactation requires special considerations and should be implemented to prevent any adverse outcomes in mother and neonate. Continuation of breastfeeding is safe and should be encouraged in hyperthyroid mothers taking ATDs, whether these are ATDs being continued after gestation or indeed ATD treatment initiated in the postpartum period. Given PTU hepatotoxicity concerns, experts currently recommend using low-to-moderate MMI doses as a first-line therapy in lactating mothers. PTU should be reserved only as a second-line agent for cases of severe hyperthyroidism (thyroid storm) and allergic reactions to previous MMI treatment. ATD should be administered in divided doses immediately following each feeding. Evaluation of thyroid function tests is advisable at least 3–4 weeks after initiation of breastfeeding.
TÓM TẮT
Thuốc kháng giáp trạng được sử dụng rộng rãi để điều trị bệnh basedow trong dân số nói chung. Trong hơn một thập kỷ qua, người ta thấy rối loạn chức năng tuyến giáp rất hay gặp ở bà mẹ sau khi sinh so với đánh giá trước đây. Các phản ứng miễn dịch trong cơ thể diễn ra mạnh mẽ sau sinh 3 – 12 tháng. Quản lý cường giáp trong thời kỳ cho con bú cần được đánh giá và cân nhắc một cách cẩn thận và nên được thực hiện để ngăn ngừa tác dụng bất lợi cho mẹ và trẻ sơ sinh. Tiếp tục cho con bú là an toàn và nên được khuyến khích ở bà mẹ cường giáp đang sử dụng thuốc kháng giáp trạng, cho dù là những thuốc kháng giáp trạng đang được sử dụng trước đó trong khi mang thai hay bắt đầu điều trị kháng giáp trạng tổng hợp trong giai đoạn sau sinh. Do tác dụng gây viêm gan nhiễm độc của PTU. Các chuyên gia khuyên nên sử dụng liều MMI từ thấp đến trung bình ở các bà mẹ đang cho con bú. PTU chỉ được lựa chọn trong các trường hợp cường giáp nghiêm trọng (cơn bão giáp) hoặc bệnh nhân dị ứng với MMI trước đó. Thuốc kháng giáp trạng nên được chia liều sử dụng ngay sau mỗi bữa ăn. Xét nghiệm chức năng tuyến giáp được thực hiện ít nhất 3 – 4 tuần sau khi bắt đầu cho con bú.
Từ khoá: cho con bú; cường giáp; thuốc kháng giáp trạng tổng hợp
Chịu trách nhiệm chính: Nguyễn Thi Giang
Ngày nhận bài: 01/7/2019
Ngày phản biện khoa học: 21/7/2019
Ngày duyệt bài: 1/8/2019
1. CHO CON BÚ VÀ CHỨC NĂNG TUYẾN GIÁP
Cho con bú là con đường tự nhiên cung cấp các chất dinh dưỡng cần thiết cho trẻ sơ sinh, cần cho sự phát triển và trưởng thành. Những trẻ sơ sinh được bú mẹ hoàn toàn trong ít nhất 6 tháng thì ít mắc bệnh đường tiêu hóa hơn trẻ sơ sinh bú sữa mẹ không hoàn toàn trong 3 hoặc 4 tháng [1]. Do có những lợi ích cho trẻ sơ sinh, bao gồm dinh dưỡng, bảo vệ chống lại bệnh truyền nhiễm và miễn dịch, thúc đẩy sự phát triển và tâm lý gắn bó mẹ con. Việc tiếp xúc với thuốc kháng giáp qua sữa mẹ có khả năng gây ra các tác dụng phụ hoặc có những ảnh hưởng bất lợi đến trẻ sơ sinh. Mặc dù vậy, thuốc kháng giáp trạng vẫn được coi là một liệu pháp cốt lõi trong việc điều trị cường giáp ở bà mẹ cho con bú (Figure 1).
2. QUẢN LÝ TÌNH TRẠNG CƯỜNG GIÁP TRONG THỜI KÌ CHO CON BÚ
Thuốc kháng giáp trạng, thionamides gồm propylthiouracil (PTU) và methimazole (MMI). MMI được sử dụng phổ biến ở Châu Âu, Châu Á và Hoa Kỳ. Một số nơi, carbimazole (CBZ), một loại tương tự methimazole thì được sử dụng ở Vương quốc Anh và thuộc địa trước đây của Anh [2]. Tác động chính của chúng là ức chế tổng hợp hormone tuyến giáp thông qua việc gắn vào men peroxydase: ức chế cạnh tranh gắn iode vào peroxydase) [2].
Trước đây, thuốc kháng giáp trạng không được sử dụng trong thời kì cho con bú do những lo ngại về nồng độ thuốc trong sữa mẹ có thể gây ra tác dụng bất lợi cho tuyến giáp của trẻ [3,4]. Tác động của các thuốc kháng giáp trạng thế hệ mới đã được nghiên cứu từ những năm 1980. MMI và PTU, được hấp thu nhanh từ đường tiêu hóa. Tác dụng kháng giáp trạng có hiệu lực kéo dài 12 – 24h đối với PTU và dài hơn đối với MMI. Vì vậy MMI chỉ cần uống 1 lần 1 ngày và PTU chia liều từ 2 – 3 lần/ngày. MMI chủ yếu là ở dạng tự do trong huyết thanh, trong khi 80% đến 90% PTU gắn với albumin [2]. Khi sử dụng thuốc kháng giáp trạng tổng hợp như là một lựa chọn đầu tay cần cân nhắc lợi ích và nguy cơ của liệu pháp điều trị triệt để khác như liệu pháp iod phóng xạ hay phẫu thuật. Những bà mẹ vẫn muốn tiếp tục cho con bú thì sử dụng thuốc kháng giáp trạng vẫn là ưu tiên hàng đầu trong điều trị (Figure1).
PTU vào sữa mẹ với lượng rất nhỏ (0,025%), (tỷ lệ sữa – huyết tương: 0.1) [5]. Lượng MMI bài tiết vào sữa bằng với nồng độ MMI huyết tương, (tỷ lệ sữa – huyết tương: 1.0) với sự bài tiết trung bình vào sữa mẹ trong khoảng thời gian 8 giờ tương đương với 0,1- 0,17% liều dùng đường uống [6]. Nồng độ MMI huyết thanh ở trẻ sơ sinh < 0,03 mg/mL 2 giờ sau khi uống MMI của người mẹ, thấp hơn nhiều so với liều điều trị [7].
Do nồng độ trong sữa thấp hơn, trong nhiều thập kỷ, PTU là thuốc được lựa chọn điều trị cường giáp cho người mẹ trong thời gian cho con bú [8]. Cả hai loại thuốc đều xuất hiện trong sữa mẹ (MMI nhiều hơn PTU) nhưng ở nồng độ thấp. Các nghiên cứu lâm sàng ở trẻ bú mẹ đã cho thấy chức năng tuyến giáp bình thường và sự phát triển trí tuệ bình thường khi người mẹ sử dụng thuốc kháng giáp trong thời gian cho con bú [9,10]. Nghiên cứu cũng cho thấy rằng khi sử dụng MMI (liều tối đa 20 mg/ngày) hoặc PTU (tối đa 600 – 750 mg/ngày) trong thời kỳ cho con bú không ảnh hưởng đáng kể đến nồng độ hormone tuyến giáp của trẻ sơ sinh [11].
Bên cạnh thuốc từ huyết tương mẹ qua sữa, một số yếu tố khác đóng vai trò then chốt làm gia tăng nguy cơ ngộ độc thuốc ở trẻ sơ sinh với thuốc kháng giáp có trong sữa mẹ [8].
- Tần số và số lượng bữa ăn của trẻ sơ sinh
- Mối liên quan của thức ăn với sự hấp thu thuốc vào huyết tương
- Nồng độ đỉnh của thuốc trong sữa mẹ
- Chức năng gan và thận của trẻ sơ sinh
Liều thionamides điều trị nên được chia ra trong ngày, uống ngay sau khi cho con bú và lý tưởng nhất là uống 3 đến 4 giờ trước khi cho con bú lần tiếp theo [13-15]. Mặc dù các chuyên gia nhi khoa hiện đang khuyến khích cho con bú theo nhu cầu, các chuyên gia nội tiết học khuyến cáo rằng các thuốc KGTTH nên được uống sau bữa ăn và chia liều [13]. Do đó, có vẻ hợp lý khi xem xét chuyển đổi mô hình cho con bú theo nhu cầu sang cho con bú theo lịch trình để tạo điều kiện cho điều chỉnh liều và làm giảm sự tiếp xúc của trẻ với thuốc KGTTH.
Trong trường hợp CBZ dùng 1lần/ngày, có thể chia liều thuốc 2-3 lần/ngày hoặc chuyển nó sang MMI[16].
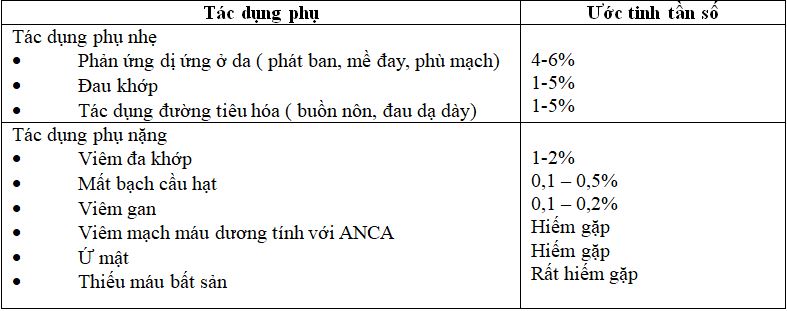
Trong dân số nói chung, thuốc KGTTH gây ra tác dụng phụ nhẹ ở 10 – 15% người bệnh. Tác dụng phụ nặng ít gặp hơn. Tác dụng phụ liên quan đến MMI phụ thuộc vào liều, trong khi PTU ít liên quan đến liều lượng. Tác dụng phụ của thuốc KGTTH được liệt kê trong Bảng 1.
Tuy nhiên, với tỷ lệ sử dụng thuốc KGTTH thấp ở các bà mẹ cho con bú và hầu hết các tác dụng phụ là không phổ biến, rất khó để xác định liệu tỷ lệ tác dụng phụ trong bà mẹ cho con bú và trẻ sơ sinh có tương tự như trong dân số nói chung hay không.
Thuốc KGTTH, đặc biệt là PTU, có liên quan đến rối loạn chức năng gan cả ở trẻ em và người lớn. Biểu hiện lâm sàng rất khác nhau từ tổn thương gan nhẹ, hồi phục đến suy gan cấp, ghép gan, hoặc thậm chí tử vong [8]. Hầu hết các trường hợp sử dụng PTU thường nặng hơn, do đặc tính riêng và không phụ thuộc vào liều.
Không có dấu ấn sinh học nào có thể dự đoán tổn thương gan. Do đó, PTU thường là lựa chọn thứ hai. Hầu hết các tổn thương gan phát triển trong thời gian vài tháng đầu (trung bình 120 ngày) điều trị và hầu hết đều có diễn biến lành tính, nhưng rất khó dự đoán [8,18]. Hiệp hội Tuyến giáp Hoa Kỳ cùng với FDA đã đánh giá lại viêm gan nhiễm độc có liên quan đến PTU và ước tính rằng 3- 4 người lớn hoặc trẻ em mỗi năm sẽ bị suy gan nặng cần phải điều trị cấy ghép ngay lập tức [8,19]. Do đó, ngay cả một lượng nhỏ thuốc cũng có khả năng gây hại cho trẻ sơ sinh và nhiễm độc gan có thể xuất hiện sau một thời gian tiềm ẩn từ vài tháng đến vài năm[8].
Vì vậy, MMI với liều tối đa 20-30mg/ngày là an toàn cho bà mẹ cho con bú và trẻ. Thuốc MMI hiện nay được khuyến cáo điều trị cường giáp cho những bà mẹ đang cho con bú cần sử dụng thuốc KGTTH. Do độc tính trên gan, PTU (tốt nhất là dưới 300mg/ngày) chỉ nên là lựa chọn thứ hai cho các trường hợp như cường giáp nặng (cơn bão giáp) hoặc có dị ứng với MMI[13].
3. TÁC DỤNG CỦA THUỐC KHÁNG GIÁP ĐỐI VỚI TRẺ SƠ SINH
Một số nghiên cứu đã được công bố, trong đó bao gồm gần 200 trẻ cho có mẹ bị nhiễm độc giáp dùng PTU, MMI hoặc carbimazole[3]. Tóm tắt của các nghiên cứu này cho thấy rằng sử dụng MMI của mẹ (liều tối đa 20 mg/ngày) hoặc PTU (tối đa 600 đến 750 mg/ngày) trong thời gian cho con bú không ảnh hưởng đáng kể đến nồng độ hormone tuyến giáp của trẻ sơ sinh.
Azizi và cộng sự chứng minh rằng ngay cả khi người mẹ bị suy giáp do điều trị thuốc KGTTH chức năng tuyến giáp của trẻ bú mẹ vẫn bình thường [7,20].
Khi đánh giá tác động của KGTTH đến chức năng tuyến giáp của trẻ sơ sinh cũng như di chứng lâu dài ở trẻ, các nghiên cứu đã không tìm thấy trường hợp nào[21]. Tác dụng phụ liên quan đến thuốc KGTTH, như phát ban, mất bạch cầu hạt, rối loạn chức năng gan và di chứng tự miễn, chưa được mô tả ở trẻ bú mẹ của các bà mẹ điều trị bằng thuốc KGTTH.
Một số nghiên cứu cho thấy sự phát triển về thể chất và trí tuệ và tình trạng tuyến giáp của trẻ sơ sinh của các bà mẹ được điều trị thuốc KGTTH sau khi sinh trong khi cho con bú không thay đổi so với nhóm chứng[8,13]. Chiều cao, cân nặng, FT4, FT3, TSH và kháng thể kháng tuyến giáp ở trẻ bú mẹ của các bà mẹ bị cường giáp cho con bú sử dụng MMI (20-30 mg/ngày) không khác biệt so với nhóm chứng, cũng không có sự khác biệt về chỉ số IQ [7]. PTU với liều hàng ngày lên tới 750mg cũng không ảnh hưởng đến chức năng tuyến giáp của trẻ sơ sinh.
Tuy nhiên với tác dụng không mong muốn của PTU, liều PTU nền < 450 mg/ngày[3]. Các chuyên gia hiện khuyến cáo rằng trẻ bú sữa mẹ ở người mẹ có dùng thuốc KGTTH nên xét nghiệm đánh giá chức năng tuyến giáp. Nồng độ TSH, FT4 nên được đánh giá mỗi 3-4 tuần sau khi bắt đầu cho trẻ bú [22], nhưng không cần phải kiểm tra thường xuyên, trừ khi nhận thấy có vấn đề với sự phát triển thể chất hay tinh thần ở trẻ sơ sinh.
4. KẾT LUẬN
Tóm lại, việc tiếp tục cho con bú là an toàn và nên được khuyến khích ở các bà mẹ cường giáp có sử dụng thuốc KGTTH. Do độc tính trên gan của thuốc PTU, liều MMI từ thấp đến trung bình được khuyến cáo như một liệu pháp điều trị đầu tiên ở các bà mẹ cho con bú.
PTU chỉ nên được lựa chọn như thuốc thứ hai cho các trường hợp cường giáp nặng (cơn bão giáp) hoặc dị ứng với MMI. Liều dùng thionamides nên được chia nhiều lần trong ngày, uống ngay sau khi cho con bú và lý tưởng nhất là uống 3-4 giờ trước khi cho con bú lần tiếp theo. Có ý kiến cho rằng trẻ sơ sinh bú sữa mẹ có sử dụng thuốc KGTTH nên được sàng lọc đánh giá chức năng tuyến giáp.
Tuy nhiên người ta thấy rằng sự phát triển về thể chất và trí tuệ và chức năng tuyến giáp của trẻ sơ sinh của người mẹ nhận thuốc KGTTH trong khi vẫn cho con bú không thay đổi.
Bảng 1. Tác dụng phụ của thuốc KGTTH
Hình 1. Quy trình để quản lý các bà mẹ cho con bú bị cường giáp.
Đường đứt nét đại diện cho lựa chọn phương pháp điều trị thay thế.
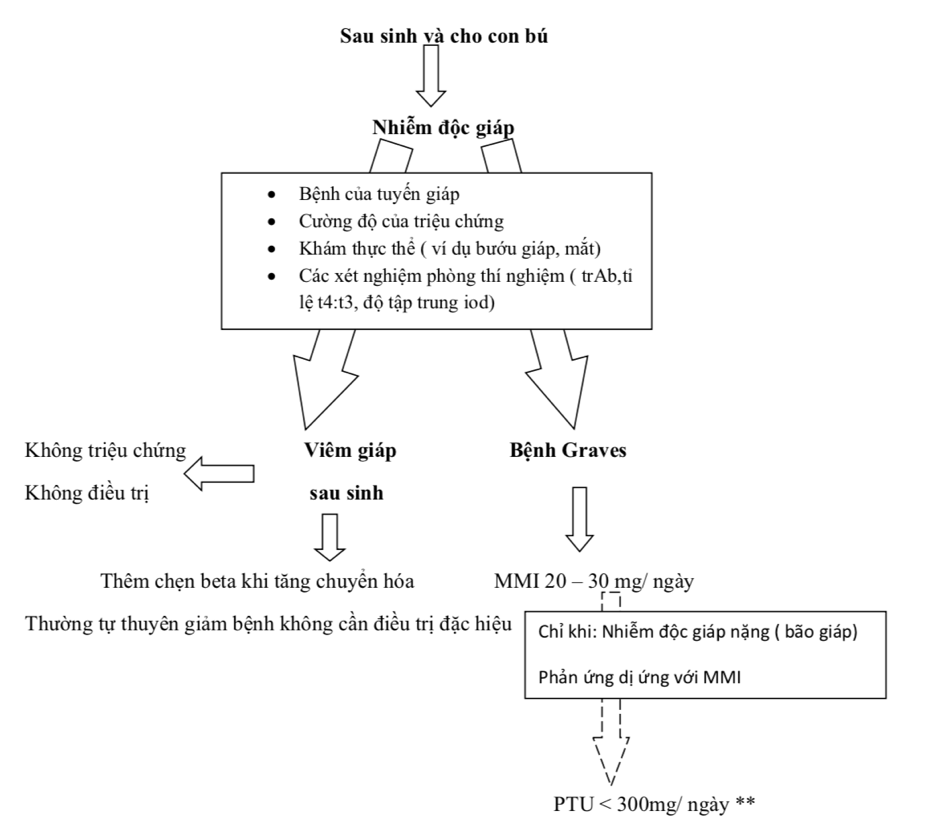
* Thực hiện chia liều ngay sau mỗi bữa: cần theo dõi chức năng gan.
** Liệu pháp điều trị thay thế: thực hiện chia liều ngay sau mỗi bữa: đòi hỏi theo dõi chức năng gan.
TÀI LIỆU THAM KHẢO
- Kramer, M.S. & Kakuma, R. (2012) Optimal duration of exclusive breastfeeding. Cochrane Database Syst Rev 8, CD003517.
- Cooper, D.S. (2005) Antithyroid drugs. N Engl J Med 352, 905-917.
- Mandel, S.J. & Cooper, D.S. (2001) The use of antithyroid drugs in pregnancy andlactation. JClin Endocrinol Metab 86, 2354-2359.
- Williams, R.H., Kay, G.A. & Jandorf, B.J. (1944) Thiouracil. Its Absorption,Distribution, and Excretion. J Clin Invest 23, 613-627.
- Kampmann, J.P., Johansen, K., Hansen, J.M. & Helweg, J. (1980) Propylthiouracil inhuman milk. Revision of a dogma. Lancet 1, 736-737.
- Johansen, K., Andersen, A.N., Kampmann, J.P., Molholm Hansen, J.M. & Mortensen,B. (1982) Excretion of methimazole in human milk. Eur J Clin Pharmacol 23, 339-341.
- Azizi, F., Khoshniat, M., Bahrainian, M. & Hedayati, M. (2000) Thyroid function andintellectual development of infants nursed by mothers taking methimazole. J Clin EndocrinolMetab 85, 3233-3238.
- Karras, S. & Krassas, G.E. (2012) Breastfeeding and antithyroid drugs: a view fromEur Thyroid J 1, 30-33.
- Momotani, N., Yamashita, R., Makino, F., Noh, J.Y., Ishikawa, N. & Ito, K. (2000)Thyroid function in wholly breast-feeding infants whose mothers take high doses ofClin Endocrinol (Oxf) 53, 177-181.
- Azizi, F. & Hedayati, M. (2002) Thyroid function in breast-fed infants whose motherstake high doses of methimazole. J Endocrinol Invest 25, 493-496.
- Lao, T. (2005) Management of hyperthyroidism and goitre in pregnancy, andpostpartum thyroiditis. J Paediatr Obstet Gynaecol 31, 155-164.
- Ito, S. (2000) Drug therapy for breast-feeding women. N Engl J Med 343, 118-126.This article is protected by copyright. All rights reserved.
- Stagnaro-Green, A., Abalovich, M., Alexander, et al (2011) Guidelines of theAmerican Thyroid Association for the diagnosis and management of thyroid disease duringpregnancy and postpartum. Thyroid 21, 1081-1125.
- Abalovich, M., Amino, N., Barbour, L.A., Cobin, R.H., De Groot, L.J., Glinoer, D.,Mandel, S.J. & Stagnaro-Green, A. (2007) Management of thyroid dysfunction duringpregnancy and postpartum: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 92, S1-47.
- Prunty, J.J., Heise, C.D. & Chaffin, D.G. (2016) Graves’ Disease Pharmacotherapy inWomen of Reproductive Age. Pharmacotherapy 36, 64-83.
- Krishna, U.R., Tank, D.K. & Daftary, S. Pregnancy at risk : current concepts. New Delhi : Jaypee, 2001, (2004 [printing]).
- Rivkees, S.A. & Mattison, D.R. (2009) Ending propylthiouracil-induced liver failurein children. N Engl J Med 360, 1574-1575.
- Kim, H.J., Kim, B.H., Han, Y.S., Yang, I., Kim, K.J., Dong, S.H., Chang, Y.W., Lee,I. & Chang, R. (2001) The incidence and clinical characteristics of symptomatic propylthiouracil-induced hepatic injury in patients with hyperthyroidism: a single-center
retrospective study. Am J Gastroenterol 96, 165-169. - S. Food and Drug Administration (2009 Propylthiouracyl (PTU)-related livertoxicity. April 18 2009 workshop.).
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam