BỆNH CƠ TIM NHIỄM ĐỘC GIÁP
GS.TS. Nguyễn Hải Thủy
Trường Đại học Y Dược Huế
SUMMARY
Thyrotoxic cardiomyopathy
Thyrotoxic cardiomyopathy (TCMP) defines a myocardial damage caused by the toxic effects of abundant thyroid hormones (TH) that result in altered energy production by myocytes (oxidative phosphorylation, glycolysis), intracellularmetabolism (protein synthesis) and myofibril contractile function . The main manifestations of TCP are left ventricularhypertrophy (LVH) , heart rhythm disturbances (usually, atrial fibrillation) , dilation of the heartchambers and heart failure , pulmonary hypertension and diastolic dysfunction. LVH used to be considered reversible in TCMP patients and LVH was found to be completely reversible when euthyroidism was achieved. However, it was not proven in more prolonged studies when thyroid function was normalized by thymasol therapy , Cardiac function and output, as well as systolic blood pressure were altered even after euthyroid state was restored. It could result from TH-induced expression of the genes of contractile proteins and β-adrenoreceptors. Reversiblechanges might not be complete and would take longer time.Some authors confirmed betablocker benefits for LVH prevention. The impact of rennin-angiotensin system onLVH development and potential role of angiotensin converting enzyme inhibitors (ACEi) inLVH prevention and treatment in thyrotoxicosis. Therefore, recent studies demonstrated high risk of irreversible LVH and left atrial dilationin AF in prolonged thyrotoxicosis and/or in elderly patients. The risk is high even aftereuthyroidism restoration by antithyroid medication. Beta-blockers and ACEi contribute to a
better reversibility of the alterations, but complete recovery is not observed. Therefore, nonreversible (non-medication) treatment seems to be beneficial in a high-risk patients (males,women over the age of 44 years, systolic hypertension) regarding TCMP prevention.Delayed diagnosis of thyrotoxicosis is of great medical importance as TCMP maymanifestat first examination. These patients should be considered for non-medication treatmentimmediately after euthyroidism is restored.
Chịu trách nhiệm chính: Nguyễn Hải Thủy
Ngày nhận bài: 01/7/2019
Ngày phản biện khoa học: 21/7/2019
Ngày duyệt bài: 1/8/2019
1. ĐẶT VẤN ĐỀ.
Nhiểm độc giáp (thyrotoxicosis) là một hội chứng thường gặp trên lâm sàng, theo điều tra của Wickham tỷ lệ này là 2% ở phụ nữ và 0,2% ở nam giới ở những vùng có lượng iode sử dụng bình thường. Trong vòng 20 năm qua, tỷ lệ nhiểm độc giáp (NĐG) là 0,8/1000 ở phụ nữ và 0,6/1000 ở nam giới.
Nhiểm độc giáp dưới lâm sàng (NĐGDLS) được xác định khi nồng độ TSH thấp hơn bình thường nhưng nồng độ FT4 và FT3 còn trong giới hạn bình thường. Tuy nhiên thực tế nồng độ hormon giáp thường nằm ở giới hạn trên của bảng tham chiếu do đó nồng độ hormon giáp tăng lên vừa đủ để làm giảm TSH và với nồng độ hormon giáp này cũng có khả năng gây ra các hậu quả không bình thường trên tổ chức đích về lâu dài.Tỷ lệ NĐGDLS dao động từ 0,6 đến 16% tùy thuộc vào các yếu tố nguy cơ như tuổi (tăng gấp đôi ở người cao tuổi), thiếu hụt iode (tăng gấp 5 lần ở những vùng thiếu iode) và giảm TSH. Tình trạng NĐGDLS phổ biến hơn so với nhiểm độc giáp lâm sàng
Có 2 loại NĐGDLS bao gồm nhiểm độc giáp ngoại sinh (iatrogenic) và nội sinh. Nhiểm độc giáp ngoại sinh chủ yếu là do liệu pháp sử dụng L. thyroxin nhằm giảm nồng độ TSH dưới mức bình thường được chỉ định ở những bệnh nhân sau phẫu thuật K giáp và được xem như là phương tiện dự phòng tái phát ung thư. Nhóm bệnh nhân này được điều trị L-Thyroxin kéo dài (2 năm và lâu hơn), và được xem xét trong các nghiên cứu về các phản ứng phụ của liệu pháp điều trị ức chế. Ngoài ra các bệnh nhân có bướu giáp nhân lành tính có liệu pháp L Thyroxin với thời gian ngắn (6-12 tháng) nhằm làm giảm nhẹ TSH (TSH trên 0,1U/l). Theo phần lớn dữ liệu 1/2-2/3 trường hợp NĐGDLS ngoại sinh .
Nhiểm độc giáp nội sinh cũng được chia thành 2 nhóm liên quan miễn dịch (Basedow) và không do miễn dịch (u tuyến độc, tiền độc tính (pretoxic)và bướu giáp độc đa nhân) trong đó bệnh Basedow là nguyên nhân phổ biến nhất gây ra nhiểm độc giáp nội sinh.
Bệnh cơ tim nhiểm độc giáp (BCTNĐG) là một biến chứng nguy hiểm của nhiểm độc giáp làm gia tăng nguy cơ tàn phế và tử vong liên quan tim mạch. Sự thay đổi cấu trúc cơ tim trong nhiểm độc giáp được xem như tiên lượng vì có khả năng hồi phục cao nếu tuyến giáp đạt bình giáp được nhanh chóng.Tuy nhiên, các nghiên cứu dài hạn cũng đã ghi nhận sự kết hợp của những thay đổi này không phải lúc nào cũng hoàn toàn. Một số thay đổi mô học không thể đảo ngược của cơ tim được ghi nhận ở những bệnh nhân đã bị nhiểm độc giáp trước đó như hoại tử tế bào cơ tim phì đại và phát triển xơ hóa cơ tim.
Xơ hóa cơ tim cũng đã được phát hiện bằng phương pháp phóng xạ miễn dịch với các kháng thể antimyosin ở những bệnh nhân BCTNĐG có biến chứng do suy tim (Martí et al., 1997). Có một bằng chứng hiện nay cho thấy dù thành công điều trị nhiểm độc giáp có liên quan đến tiên lượng xấu. Do đó, tử vong trên bệnh nhân có bệnh tim mạch (tăng huyết áp, bệnh van tim, suy tim, và bệnh động mạch vành) là 1,2 ở những bệnh nhân này và tỷ lệ tử vong mạch máu não cao hơn 1,4 lần so với dân số nói chung . Sự tổn thương cơ tim kéo dài được xem là một nguyên nhân làm tăng tỷ lệ tử vong của nhiểm độc giáp.
NĐGDLS ảnh hưởng đến sức khỏe chưa được xác nhận một cách đầy đủ và một số vấn đề chưa được giải quyết. Tuy nhiên, một số lượng khá lớn các thông tin của hai thập kỷ qua đã xác nhận các tác dụng có hại của hormon giáp và nhất là trên hệ thống tim mạch. Hơn nữa, còn có bằng chứng về sự gia tăng tử vong ở bệnh nhân có NĐGDLS. Trong nghiên cứu tại Anh Quốc ở những bệnh nhân tử vong trên 60 tuổi (theo dõi 5 năm) có nồng độ TSH dưới mức bình thường là cao gấp đôi so với những người cùng độ tuổi bình giáp. Bệnh tim mạch là nguyên nhân phổ biến nhất gây ra những biến cố nguy hiểm. Do đó, các biến chứng về tim mạch về lâu lài của nhiểm độc giáp là rất quan trọng.
2. ĐỊNH NGHĨA – DỊCH TỄ HỌC VÀ ĐẶC ĐIỂM LÂM SÀNG VỀ BỆNH CƠ TIM NHIỄM ĐỘC GIÁP
Bệnh lý cơ tim nhiểm độc giáp (BCTNĐG) được xác định bởi tổn thương cơ tim do các tác dụng độc hại của lượng lớn hormon giáp gây ra tình trạng rối loạn tạo năng lượng các tế bào cơ tim (phosphoryl hóa oxy hóa, glycolysis), rối loạn chuyển hóa nội bào (tổng hợp protein) và rối loạn chức năng co bóp của cơ tim.
Các biểu hiện chính của BCTNĐG là phì đại thất trái, rối loạn nhịp tim (thường là rung nhĩ), tăng áp phổi , dãn các buồng tim,rối loạn chức năng tâm trương, tâm thu và suy tim
Hiện chưa có dữ liệu về dịch tễ học về BCTNĐG. Điều này là do thiếu các tiêu chuẩn chẩn đoán và việc đưa ra thuật ngữ “bệnh cơ tim nhiểm độc giáp” trong thực hành lâm sàng và nghiên cứu chỉ xuất hiện sau khi có sự phân loại bệnh cơ tim của WHO/ISFC (1995).
MeanWhile et al. (1959) phát hiện 4/9 cuộc khám nghiệm không phát hiện nguyên nhân nào khác gây suy tim nặng ngoại trừ nhiểm độc giáp và 64/150 bệnh nhân (43%) có nhiểm độc giáp có các biến chứng về tim mạch do không có bất kỳ bệnh tim nào từ trước.Các bằng chứng sẵn có chỉ cung cấp số liệu về tần suất các biểu hiện BCTNĐG bao gồm những biến chứng bệnh nặng nhất –rung nhĩ và Suy tim.
Rối loạn nhịp tim trong nhiễm độc giáp
Nhịp nhanh xoang là phổ biến nhất xảy ra 42% -73% Nhịp tim nhanh khi nghỉ ngơi và trong khi ngủ là triệu chứng điển hình về nhiểm độc giáp.Tỉ lệ tăng nhịp tim lúc nghỉ ngơi là một trong những thông số dự báo quan trọng nhất và tiên đoán về các biến chứng tim mạch nghiêm trọng. Tỉ lệ nhịp tim tăng lên có liên quan đến tỷ lệ tử vong cao hơn. Nguy cơ tử vong từ tất cả các nguyên nhân là cao gấp 3 lần ở những bệnh nhân có nhịp tim nghỉ ngơi 90-99 so với 60 nhịp mỗi phút. Giá trị tiên đoán của tần số timnhanh thường gặp hơn ở người bị tăng huyết áp và những người có bệnh động mạch vành. Nhịp tim nhanh có thể làm tăng huyết áp, tăng nguy cơ biến cố tim mạch, bệnh mạch vành, rối loạn nhịp thất là nguyên nhân gây đột tử, gây tăng huyết áp và suy tim.
Nhịp chậm xoang thường hiếm gặp ở bệnh nhân nhiểm độc giáp.
Rung nhĩ (RN) xảy ra ở 9% -23% bệnh nhân bị nhiểm độc giáp so với 0.4% -0.0% trong dân số nói chung. Đây là biến chứng tim mạch phổ biến nhất về nhiểm độc giáp và có tỷ lệ bệnh tật và tử vong cao liên quan đến huyết khối gây thuyên tắc. Tỷ lệ biến chứng rất khác nhau. Sandler và Wilson (1959) và Petersen và Hansen (1988) ghi nhận 14% và 14,9% sự xuất hiện của rung nhĩ, trong dân số của những người không có bệnh tim đồng thời. Trong một nghiên cứu về phụ nữ bị rung nhĩ có bệnh tim khác nhau đã phát hiện 67% bệnh nhân bị nhiểm độc giáp.
Nhiểm độc giáp dưới lâm sàng (NĐGDLS) cũng có liên quan đến gia tăng nguy cơ RN . Trong nghiên cứu Framingham ở thời điểm 20 năm theo dõi, tỷ lệ mắc RN là 25% ở những bệnh nhân có nồng độ TSH thấp, cao gấp 3 lần so với ở nhóm bình giáp (7%) (Sawin và cộng sự, 1994). Tần suất xuất hiện của RN có thể so sánh được với chứng nhiểm độc giáp lâm sàng và cận lâm sàng. Theo Auer J. et al. (2001), RN chiếm 13,8% ở những bệnh nhân nhiểm độc giáp lâm sàng, 12,7% trong NĐGDLS, và 2,3% ở bệnh nhân bình giáp (Auer et al., 2001). Ngoại tâm thu (5% -7%), nhịp nhanh kịch phát (0.2% -3.3%) và cuồng động nhĩ (khoảng 1.4%) xảy ra trong nhiễm độc giáp.
Khảo sát Holter điện tâm đồ cho thấy rốiloạn nhịp nhĩ là điển hình đối với nhiểm độc giáp trong khi các rối loạn nhịp thất thường chỉ xảy ra ở những trường hợp nặng và ở những bệnh nhân mắc bệnh tim mạch đồng thời
Các rối loạn nhịp tim thường gặp trong nhiểm độc giáp bao gồm:Nhịp nhanh xoang : 42-73%, Rung nhĩ : 9-23%, Ngoại tâm thu : 5-7%, Rung nhĩ : 1,2-2,3%, Nhịp nhanh kịch phát : 0,2-3,3%, Bloc nhĩ thất: 2,7-5% và Hội chứng nút xoang bệnh lý có thể gặp ở người cao tuổi
Phì đại thất trái (PĐTT)
Một số nghiên cứu ghi nhận có sự gia tăng khối lượng thất tráiở cả hai trường hợp nhiểm độc giáp lâm sàng và dưới lâm sàng . Hiện không đủ nghiên cứu để xem sự xuất hiện của PĐTT trong nhiễm độc giáp và các yếu tố góp phần vào sự phát triển của nó, hình thái học tim (lệch tâm hoặc đồng tâm) và sự hồi phục của cơ tim.
Theo nghiên cứu dịch tễ học (1510 bệnh nhân trên 45 tuổi) do M. Dörr et al. (2005) PĐTT được chẩn đoán ở 57,1% bệnh nhân bị nhiểm độc giáp, so với 10,5% ở các cá nhân bình giáp. Do đó, nhiểm độc giáp được xem là một yếu tố dự báo độc lập về PĐTT . Tuy nhiên khi phân tích sự xuất hiện PĐTT và các yếu tố góp phần phát triển và khả năng đảo ngược giữa các bệnh nhân nhiểm độc giáp. Sự xuất hiện PĐTT là 22,7%, thấp hơn so vớidữ liệu trên. Những bệnh nhân dưới 55 tuổi mà không có bệnh lý tim mạch và đây có thể là lý do có thể cho tỷ lệ thấp hơn .
Sự gia tăng chỉ số khối cơ thất trái (CSKCTT) đã được chứng minh trong tất cả các nghiên cứu liên quan đến NĐGDLS (Ching et al., 1996, Auer, 2001), tuy nhiên, các giá trị này không đáp ứng các tiêu chuẩn chẩn đoán cho phì đại thất trái..
Chỉ có phụ nữ bị nhiểm độc giáp lâm sàng, so với NĐGDLS có giá trị CSKCTT cao (đáp ứng các tiêu chuẩn PĐTT) liên quan đến sự giảm thể tích thất trái cuối tâm trương và sự phát triển của PĐTTđồng tâm báo cáo của Donatelli M và cộng sự. (2003), mặt khác đa số các nghiên cứu chứng minh có sự gia tăng của cả CSKCTT và thể tích thất trái cuối tâm trương và sự phát triển PĐTT lệchtâm. Ngoài ra một số nghiên cứu ghi nhận sự tái cấu trúc thất trái đồng tâm thường xảy ra NĐGDLS trong khi tái cấu trúc lệch tâm lại phổ biến hơn trong nhiểm độc giáp lâm sàng
Suy tim: Các nghiên cứu ghi nhận tỷ lệ suy tim khác nhautrên các bệnh nhân nhiểm độc giáp từ 12% lên 68% có khiđến 90% bệnh nhân và suy tim phát triển rung nhĩ .
BCTNĐG vớithể giãn các buồng tim được xem như là một biến chứng đe doạ độc tính của nhiểm độc giáp cần được quan tâm báo cáo có 1% sự xuất hiện của bệnh cơ tim nhiểm đôc giáp thể dãn ở bệnh nhân bị nhiểm độc giáp và một phần ba trường hợp không thể phục hồi.
Nhiễm độc giáp chiếm 1% sốbệnh nhân có BCTNĐG thể giãn .
Tăng áp phổi (TAP): có sự liên quan giữa tình trạng nhiểm độc giáp và tăng áp phổi (TAP)đã được mô tả sớm nhất vào đầu những năm 1980 và các cơ chế liên quan cho đến nay vẫn chưa thống nhất trong số đó Basedow chiếm hầu hết các trường hợp TAP trong đó 47-65% bệnh nhân cường giáp có bướu giáp lan tỏa kèmTAP.Tỷ lệ cao như vậy có thể được giải thích bằng cả dạng nhiểm độc giáp và tác dụng liên quan tự miễn dịch. Sự xuất hiện của TAP trong NĐGDLS không rõ Theo số liệu nghiên cứu ghi nhận tỷ lệ TAP hiện mắc là 29% ở NĐGDLS và 39,6% ở nhiểm độc giáp lâm sàng.
Sa van hai lá: Tỷ lệ sa van hai lá là 18-41% bệnh nhân nhiểm độc giáp so với 6-20% dân số nói chung (Brauman và cộng sự, 1985, Evangelopoulou và cộng sự, 1999).
- SINH BỆNH HỌC VÀ BIỂU HIỆN CỦA BỆNH CƠ TIM NHIỄM ĐỘC GIÁP
3.1. Tác dụng hormon giáp lên tim mạch
Hormon giáp tác động trên hệ thống tim mạch thông qua ba tiến trình nội bào trong tế bào cơ timbao gồm (1) sản xuất năng lượng (phosphoryl oxy hoá, glycolysis), (2)tổng hợp protein và (3) co bóp cơ tim (Dillmann, 1990; Klein et al., 2000, 2001).
Rối loạn tạo năng lượng. Tiêu thụ oxy cơ tim gia tăngtrong nhiểm độc giáp. Số lượng và hoạt tính chức năng của ty thể cũng tăng lên dẫn đến việc tăng sản xuất adenosine triphosphate (ATP).
Tuy nhiên, trong tình trạng nhiểm độc giáp nặng, mặc dù mức tiêu thụ oxy tăng lên, nhưng hiệu quả sử dụng lại giảm đáng kể. Điều này theo sau sựrối loạn phosphoryl oxy hóa xảy ra do hoạt động bất thường của enzyme oxy hóa (giảm nồng độ ATP cơ tim và nồng độ creatine phosphate sẽ dẫn đến kích hoạt thoái biến glucose (glycolysis). Ngoài ra tác động trực tiếp và gián tiếp lên tim với lượng lớn hormon giáp dẫn đến rối loạn co bóp tim.
Tác động trực tiếp hormon giáp lên cơ tim liên quan đến phiên mã của một số gen điều hòa chức năng của tế bào tim, các tế bào cơ trơn mạch máu và các đơn vị cấu trúc khác. Triiodothyronine (T3) là một horrmon chính của tuyến giáp có hoạt tính sinh học xâm nhập vào tế bào tim thông qua các vận chuyển đặc hiệu nằm trên màng tế bào và gắn kết với thụ thể hormon tuyến giáp (THR) trong nhân tế bào.
Ngày nay, có hai loại thụ thể hormon giáp được biết: (1) thụ thể homodimer (THR / THR) và (2) thụ thể heterodimer- axit retinoic 9-cis (THR / RXR). Hình thức hoạt động của các thụ thể này ảnh hưởng đến biểu hiện gen thông qua liên kết các yếu tố đáp ứng DNA đặc hiệu, được gọi là các yếu tố nhạy hormon giáp (TRE), nằm trong khu vực promoter của các gen nhạy cảm với T3. Sự phiên mã gen được gia tăng trong các vùng mã hóa chuỗi nặng của alpha-myosine (MNC-а), enzyme Cа2+ -ATPase của hệ vỏng trạng bào tương (sarcoplasmatic reticulum) của các tế bào cơ tim, các thụ thể Cа2+ K-ATPase, Ca2+ uretic, thụ thể beta1-adrenergic, troponine I và Cа + Uretic peptide.
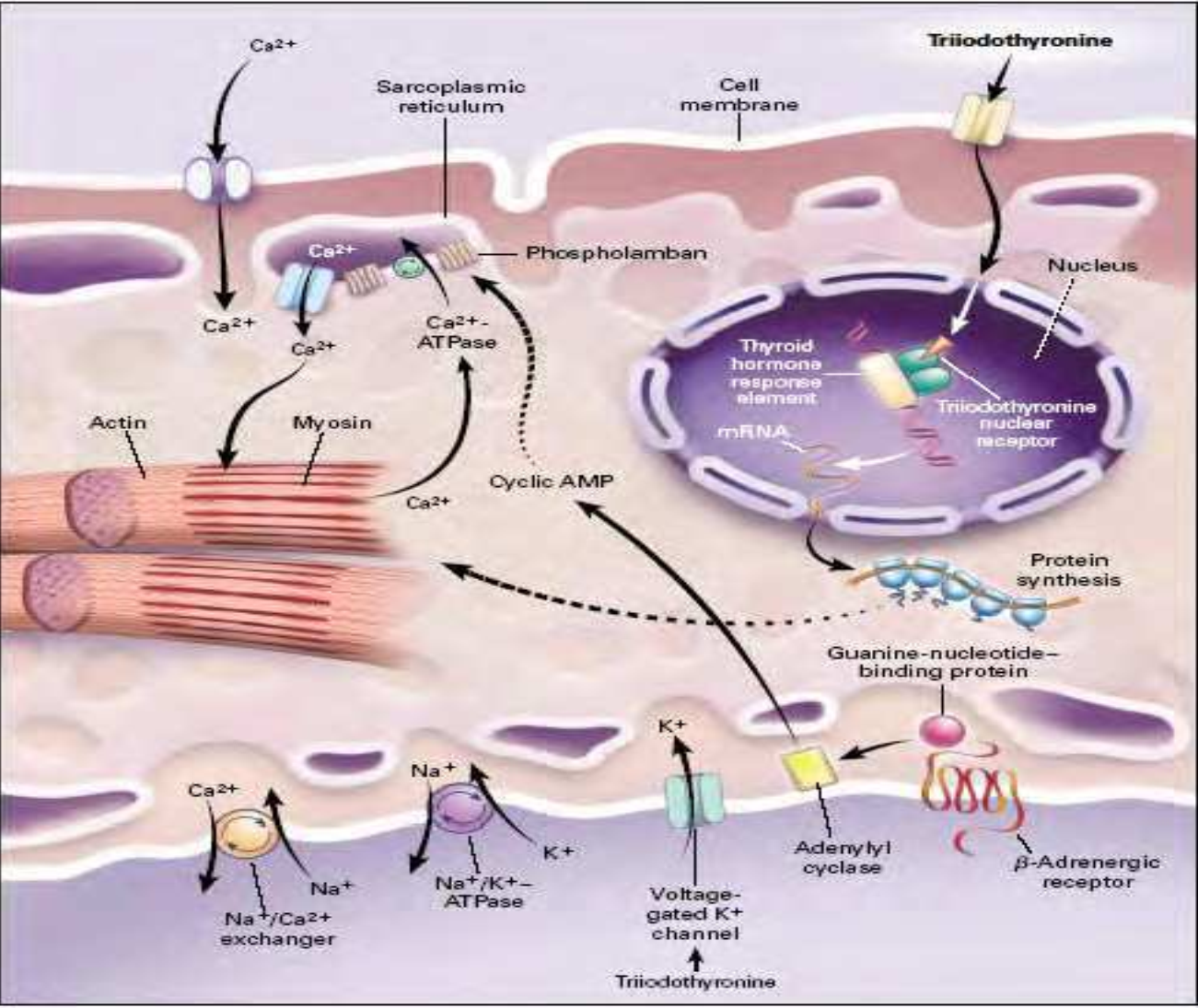
Hình 1. Ảnh hưởng lên gen và không gen của triiodthyronine trong tế bào tim
(trích dẫn từ Klein & Ojamaa, 2000)
Có ba loại đồng dạng myosine được phân biệt:
V1 bao gồm chuỗi MNC-alpha / alpha,
V2 – bao gồm các chuỗi MNC-alpha / beta, và V3 – bao gồm chuỗi MNC-beta / beta.
Nồng độ cao hormon giáp ảnh hưởng đến sự trình diện đồng dang myosine và dẫn đến sự tăng tổng hợp của đồng dạng V1 và sự giảm chất đồng dạng V3. Enzyme ATPase hoạt động mạnh hơn trong các chuỗi myosine MNC-alpha / alpha so với chuỗi MNC-beta/beta, vận tốc của các cơn co cơ tim tăng lên (Hình.1)
Tác động gián tiếp hormon giáp trên cơ tim của sự gia tăng hormon tuyến giáp bao gồm (1) phóng thích Ca2+ từ các kho nội bào và (2) tái thu nhận sau đó bằng hệ vỏng trạng bào tương (sarcoplasmic reticulum). Kết quả (2) này là do tăng cường trình diện Ca2 + ATPase (SERCA) và sự ức chế phospholamban liên quan đến việc điều chỉnh nồng độ canxi nội bào cơ tim trong qúa trình chu kỳ tim (tâm thu và tâm trương). Điều này dẫn đến sự gia tăng đỉnh điểm sự căng của sợi cơ tim và rút ngắn kỳ thu tâm thất.
Sự gia tăng hormon tuyến giáp đã được chứng minh là gây ra sự biểu hiện của các thụ thể ryanodine tạo điều kiện cho sự phóng thích canxi (Ca2 +) từ lưới võng trạngbào tương, do đó khuếch đại sự co và sự phì đại cơ tim. Ngoài ra, nồng độ cao của hormon giáp gây ra sự huy động canxi nội bào ảnh hưởng trực tiếp đến các kênh Ca2 + dạng L . (Hình 1).
Vì vậy, khi nồng độ hormon giáp cao sẽ góp phần làm tăng sự co bóp cơ tim bằng việc tăng cường phiên mã của các gen chuỗi nặng củađồng dạng beta cơ timvà ATPase phụ thuộc vào canxi, làm tăng tổng hợp protein và làm tăng lượng tiêu thụ canxi và glucose trong cơ tim.
Ngoài ra, hormon giáp còn làm giảm 50-70%sức cản hệ thống của thành mạch thông qua trực tiếp và gián tiếp (làm gia tăng sự tạonhiệt và tăng sản lactate tại mô) lên các tế bào cơ trơn thành mạch dẫn đến hạ huyết áp tâm trương và gia tăng thể tích thất trái cuối tâm trương. Đặc biệt, hormon giáp được biết là gây ra sản xuất oxit nitric gây giãn mạch bằng các tác động trực tiếp trên các tế bào cơ trơn thành mạch.
Khi nông độ hormon giápcao dẫn đến sự gia tăng lưu lượng máu lưu thông và máu tĩnh mạch trở về thông qua các cơ chế bao gồm sau đây : kích hoạt hệ thống aldosterone-renin, tăng cường tổng hợp erythropoietin và tái hấp thu muối ở ốngthận. Phức hợp bộ máy cầu thận được kích hoạt khi giảm HA tâm trương. Thêm vào đó T3 trực tiếp kích thích tổng hợp chất renin và aldosteone tại gan làm gia tăng thể tích máu và thể tích cuối tâm trương và hậu quả sau cùng là quá tải cho tim (hình 2).
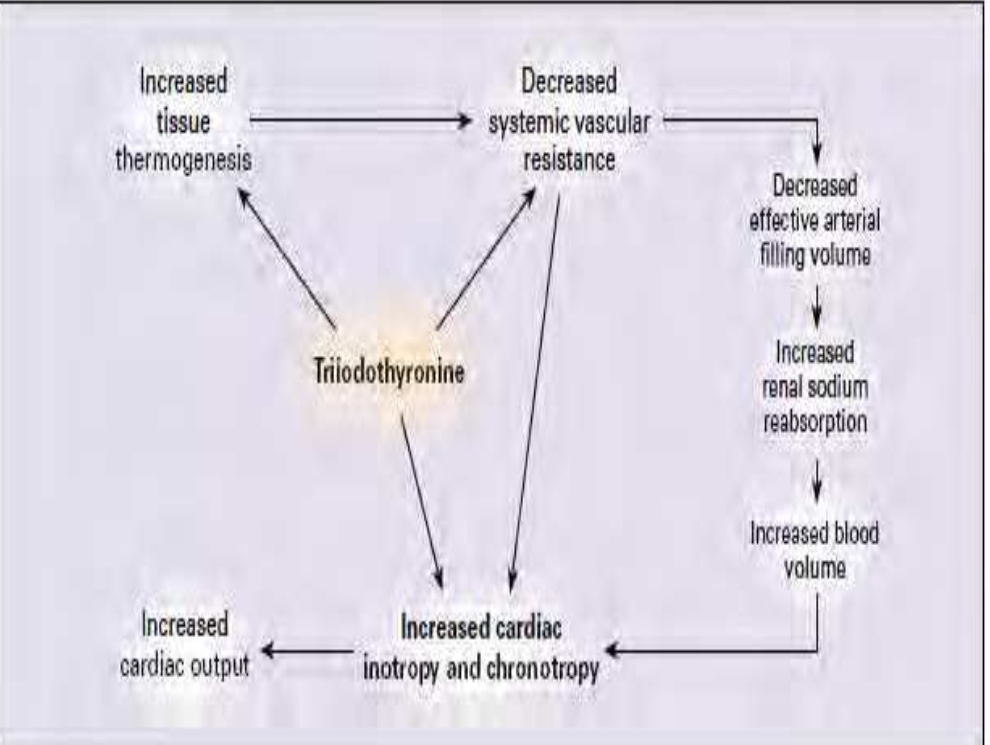
Hình 2. Tác động hormon giáp lên hệ thống huyết động tim mạch
Nhịp tim nhanh là một đặc điểm điển hình về nhiểm độc giáp. Đây là hiện tượng do sự khử cực tâm trương nhanh hơn phối hợp với sự rút ngắn của tác động tiềm năng của nút xoang nhi. Nhìn chung các tác động của hormon giáplên hệ thống điều hòa nhịp tim và hệ thống dẫn truyền điện học cơ tim bao gồm gia tăng sự khử cực tâm thu và tâm trương và rút ngắn thời gian hoạt động tiềm tàng, cũng như thời gian phản ứng của các tế bào cơ nhĩ và nhĩ thất. Tác dụng sau có thể dẫn đến sự gia tăng sự xuất hiện RN trong nhiễm độc giáp. Các cơ chế khác bao gồm gia tăng áp lực ở tâm nhĩ trái, thiếu máu và ngoại tâm thu nhĩ trái.
Bên cạnh đó hormone tuyến giáp còn điều chỉnh một số gen cơ tim mã hóa tổng hợp các kênh ion (K+/Na+-ATPase, chất trao đổi Ca+/Na+ và các kênh kali phụ thuộc tiềm năng) trong màng tế bào. Những tác dụng ngoài nhân tế bào này liên quan đến việc vận chuyển amino axit, glucose và canxi qua màng tế bào. Do đó, T3 có thể làm thay đổi hoạt động của các kênh ion khác nhau (bao gồm các kênh natri, kali và canxi) nằm trên màng tế bào.
Đặc biệt, phospholipid và proteinkinase phụ thuộc Ca, proteinkinase phụ thuộc vào cAMP và phức hợp Ca2 + -calmodulin như là các thành phần của hệ thống dẫn truyền tín hiệu liên quan đến tác dụng lên tế bào không liên quan gen của T3.Do đó, tác động hormon giáp không theo gen bao gồm việc điều chỉnh nồng độ ion nội bào và sự phân bố ion nội bào. Tác dụng hormon giáp trao đổi đổi vận chuyển ion qua màng ảnh hưởng đến tính năng điện sinh lý của các tế bào cơ tim .
Sự biểu hiện của các kênh canxi týp L do T3 dẫn đến những hiện tượng sau đây: ít ion canxi vào các tế bào cơ tim qua các kênh kiểu L và khả năng hoạt động sẽ ngắn hơn.
Sự xuất hiện các rối loạn nhịp ở tâm nhĩ (rung nhĩ, ngoại tâm thunhĩ sớm) với tần suất cao hơn trongnhiểm độc giáp, trong khi tỷ lệ rối loạn nhịp ở tâm thất thì tương đương với tần suất của quần thể chung . Sự nhạy cảm cơ tim ở tâm nhĩ và tâm thất đối với hormon giáp khác nhau có thể gây ra sự khác biệt về tần số rối loạn nhịp nhĩ và thất. Sự nhạy cảm cơ tâm nhĩ cao đối với các tác dụng gây loạn nhịp do hormon giáp gây ra là do gia tăng mật độ thụ thể β-adrenoreceptor ở bề mặt của các tế bào cơ tâm nhĩ và sự khác biệt về khởi phát tính tự động giữa nhĩ và thất . Golf et al. nhận thấy mật độ thụ thể β-adrenoreceptor ở tâm nhĩ phải của tim người cao gấp hai lần so với tâm thất trái. Mật độ thụ thể β cao hơn trong nhiễm độc tuyến giáp có liên quan đến độ nhạy catecholaminecủa cơ tim nhiều hơn.
Ngoài ra hormon Androgen kích thích sự biểu hiện của gen thụ thể β-adrenoreceptor dẫn đến mật độ tăng lên. Điều này có thể giải thích sự nhạy cảm cao hơn với rối loạn nhịp tim ở nam giới nhiều so với phụ nữ.
Biểu hiện của các kênh K + phụ thuộc vào điện thế ở tâm nhĩ là 30% bằng ở tâm thất (Ojamaa và cộng sự, 1999). Sự biểu hiện của các gen mã hoá cả thụ thể β-adrenoreceptor và các kênh K + liên quan vào điện thế phụ thuộc hormon giáp gây ra rối loạn nhịp tim. Các nghiên cứu trên chuột thí nghiệm cho thấy thời gian điện thế tác động tâm nhĩ ngắn hơn, và luồng kali máu xoay chiều trì hoãn ở nhĩ (cực nhanh – Ikur và chậm – Iss) gây tái khử cực cao hơn trong nhiểm độc giáp. Nồng độ RNA đưa tin và biểu hiện gen của kênh K + (Kv1.5 иKv2.1) được hiển thịcao hơn ở cả hai tâm nhĩ cũng dẫn đến mật độ lớn hơn của các kênh kali chỉnh trì hoãn (Ikur иIss) trong cường giáp. Tác dụng hormon giáp đối với điện thế hoạt độngvà dòng kali chỉnh lưu trì hoãn được thể hiện nhiều hơn ở tâm nhĩ phải so với trái dẫn đến sự khác biệt về khoảng cách giữa thời gian điện thế tác động (Bielecka-Dabrowa và cộng sự, 2009)., làm rút ngắn khả năng hoạt động tâm nhĩ ở nhiểm độc giáp được kết hợp với thời gian ngắn hơn của thời gian trơ có hiệu quả tạo điều kiện cho sự tái phát triển ổ vào lại. Mặt khác, sự khác biệt giữa 2 tâm nhĩ về tiềm năng tác động giữa các tế bào bình thường là rất quan trọng đối với sự co thắt tâm nhĩ đồng bộ (về vị trí bên phải của nút xoang).
Hoạt động lạc chổ tự phát, đặc biệt ở tâm nhĩ trái, có thể tăng dẫn đến rối loạn nhịp tim tâm nhĩ (rung nhĩ) khi sự khác biệt tiềm năng tương tácliên nhĩ bị giảm (Bielecka-Dabrowa, 2009).. Các tĩnh mạch phổi được cho là nguyên nhân gây ra chứng rung nhĩ kịch phát có thể là do hoạt động tự phát tăng lên của vùng đó. Tiềm năng hoạt động ngắn hơn của các tế bào cơ tim nằm trong tĩnh mạch phổi liên quan đến việc rút ngắn thời gian trơ và tạo điều kiện khởi phátquá trình vào lại được trình bày trong các mô hình nhiểm độc giáp thực nghiệm (Chen, 2002).
Sự tiềm ẫn của hormon giáp gia tăng hoạt tính tự phát trong các tế bào cơ tim trong tĩnh mạch phổi tương tự như tác động của nó đối với các tế bào nút xoang nhĩ. Hoạt động khởi phát được cho là cơ sở hoạt động tự phát của tĩnh mạch phổi (Bielecka Dabrowa et al 2009)..
3.2. Cơ chế bệnh sinh các biểu hiện lâm sàng của bệnh cơ tim nhiểm độc giáp.
Nhịp tim nhanh trong nhiễm độc giáp phát triển do sự khử cực tâm trương nhanh hơn do rút ngắn tiềm năng hoạt động của các tế bào nút xoang nhĩ [Osman F et al. 2002]. Chứng nhịp tim chậm xoang có thể phát triển trong trường hợp rối loạn bẩm sinh hoặc hội chứng nút xoang bệnh lý. Loại thứ hai này cũng như nhịp tim bất thường có thể là kết quả của giảm dự trữ của chất trung gian acetylcholine .Sinh bệnh học của rối loạn nhịp tim không rõ ràng, và các yếu tố gây bệnh sau đây đang được thảo luận: tác động độc hại của hormon giáp, tăng hoạt tính giao cảm, giảm nồng độ kali nội bào (Bảng 1).
Tăng chức năng tim và tăng kích thích adrenergic góp phần làm mất đi các ion kali nội bào dẫn đến rối loạn nhịp tim. Sự loạn dưỡng nhĩ (atrial dystrophic alteration) kết hợp kết hợp với sự không đồng nhất của mô cơ tim là một yếu tố phối hợp gây rung nhĩ. Tiếp xúc với bất kỳ yếu tố bổ sung nào làm tăng sự không đồng nhất của mô cơ tim nền tảng dẫn đến sự rối loạn nhịp tim .
Sự dãn tâm nhĩ, sự gia tăng sự kích thích của tâm nhĩ có liên quan đến sự không đồng nhất của cơ tim qua trung gian rối loạn chức năng dẫn truyền, cơ sở cho rối loạn nhịp vào lại. Sự vào lại liên quan đến tần suất hoạt động khu trú được cho là cơ chế chính của rung nhĩ và cuồng động nhĩ của nhiểm độc giáp.
Tăng cung lượng tim và giảm sức cản hệ thống thành mạch máu (SVR) trong nhiễm độc giáp thường dẫn đến sự khuếch đại biên độ xung. Huyết động rối loạn trong nhiểm độc giáp. Những thay đổi bao gồm tăng nhịp tim, đột qụyvà thể tích phút (minute volume), gia tăng lưu lượng máu, giảm sức cản thành mạch và kết quả thay đổi huyết áp giảm – huyết áp tâm thu tăng lên một cách vừa phải, trong khi huyết áp tâm trương trong mức bình thường hoặc giảm.
Bảng 1. Cơ chế bệnh sinh rối loạn nhịp tim trong nhiểm độc giáp

Do đó áp suất xung tăng lên. Các nghiên cứu gần đây đã chứng minh tăng sự cứng động mạch và giảm sức cản thành mạch (SVR) trong nhiễm độc giáp (Palmieri và cộng sự, 2004). Do đó, gia tăng hormon tuyến giáp gây ra tăng huyết áp tâm thu dẫn đến tăng huyết áp tâm thu đơn độc ở bệnh nhân cao tuổi có độ co dãn động mạch giảm do tổn thương mạch máu xơ vữa động mạch. Tần suất tăng huyết áp tâm thu đơn độc cao hơn đáng kể ở những bệnh nhân bị nhiểm độc giáp hơn so với những người bình giáp .
NĐGDLSg cũng có thể dẫn đến tăng huyết áp tâm thu và tăng huyết áp trung bình vào ban đêm (Botella-Carretero và cộng sự, 2004). Đây là một trong những yếu tố làm phát triển phì đại thất trái trong nhiễm độc giáp.
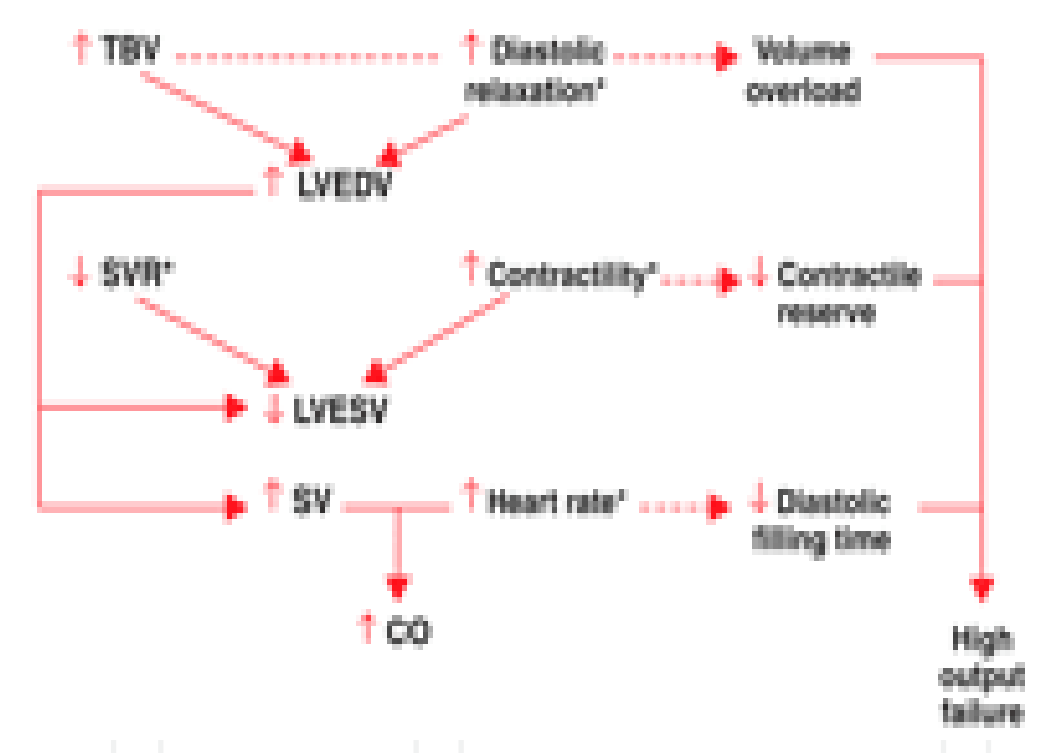
Hình 3. Tác động cường giáp trên hệ thống tim mạch và tiên lượng
Phì đại thất trái lệch tâm là do giảm sức cản thành mạch và quá tải thể tích trong tim là biểu hiện điễn hình nhiểm độc giáp. Tuy nhiên có nhiều dữ liệu cho rằng cấu trúc thất trái bình thường, type lệch tâm, cũng như týp đồng tâm có thể xãy ra trên bệnh nhân nhiểm độc giáp. Nó tùy thuộc vào mức độ tổn thương tim mach do ảnh hưởng bởi các yếu tố khác nhau.
TBV (total blood volume): Thể tích máu toàn, LVEDV (left ventricular end diastolic volume): Thể tích thất trái cuối tâm trương, LVESV (left ventricular end systolic volume): Thể tích thát trái cuối tâm thu,SV (stroke volume): thể tích tâm thu; SVR (systemic vascular resistance) Sức cản hệ thống thành mạch,CO (cardiac output): cung lượng tim (nguồn A Toft, N Boon 2000).
Giảm chức năng tim dự trữ (functional cardiac reserve)và giảm khả năng chịu đựng hoạt động cũng rất phổ biến ở nhiểm độc giáp bởi vì nhịp tim nhanh khi nghĩ ngơi nhằm dự phòng sự gia tăng nhịp tim và phân suất tống máu và giảm sức cản hệ thống thành mạch khi hoạt động thể lực.
Tăng áp phổi (TAP)
Áp lực động mạch phổi trung bình khoảng 25 mmHg khi nghĩ và tăng trên 30 mmHg khi hoạt động) .TAP thường được báo cáo ở nhiểm độc giáp. Tăng áp phổi thường liên quan đến hỡ van (van ba lá và van hai lá) do rối loạn chức năng các cơ nhú (Whitner và cộng sự, 2005, Mercé et al, 2005). Bệnh nhân bị bệnh Graves có nhiều khả năng bị thoái hoá mucoid (myxomatous degenerelation) và sa van hai lá do hậu quả củatổn thương nội tâm mạc so với những người bị bướu gíap độc đa nhân (Kahaly, 1987).Có hai cơ chế liên quan đến tổn thương van có liên quan đến bệnh Graves. Cơ chế đầu tiên bao gồm việc tạo ra sự tổng hợp glycosaminoglycan trong nội tâm mạc (tương tự như tổn thương sau hốc mắt trong bệnh mắt nội tiết) dẫn tới sự dày lên của đỉnh van (Kahaly, 1987).
Loại thứ hai liên quan giảm trương lực các cơ nhú và kết quả là quá căng của cơ dẫn đến sụpđỉnh van hai lá ở tâm nhĩ trái trong thì tâm thu tâm thất (Brauman et al., 1985).
Tăng áp phổi phát triển do phản xạ Kitaev – co thắt động mạch phổi dẫn tới sự gia tăng trở kháng mạch máu phổi (Okura & Takatsu, 1994).
Nhiều nghiên cứu ghi nhận hormon giáp tác động đến các mạch máu phổi theo một cách khá khác so với các mạch máu khác vì chúng làm giảm trở kháng hệ thống SVR và tăng lượng máu lưu hành. Huyết áp giảm trong các mạch điện trở do hiệu ứng giãn mạch của hormon giáp và tăng các mạch máu phổi.Điều này có thể là do qua trung gian của rối loạn chức năng nội mạc (Okura & Takatsu, 1994)và do sự chuyển hóa nhanh các chất giãn mạch phổi, chẳng hạn như acetylcholine, được quan sát ở những bệnh nhân bị nhiểm độc giáp nặng (Okura & Takatsu, 1994; Nakchbandi và cộng sự, 1999). Ngoài ra, sự mất cân bằng về tự động, đặc biệt, sự tăng hoạt giao cảm và giảm trương lực phế vị (Burggraaf et al., 2001), gây ra bởi cường giáp tạo điều kiện cho sự co thắt mạch phổi và phát triển tăng áp phổi.Ngoài ra cơ chế tự miễn dịch có thể là một yếu tố bổ sung cho sự phát triển tăng áp phổi
Chẩn đoán suy tim ở những bệnh nhân bị nhiểm độc giáp phức tạp vì các triệu chứng suy tim kinh điển bao gồm nhịp tim nhanh và khó thở xuất hiện ngay khi bắt đầu chứng tăng hoạt giáp do cả tác dụng độc hại của hormon tuyến giáp lên nút xoang nhĩ và trung tâm hô hấp và suy yếu cơ liên sườn.
Suy tim (HF) phát triển trong nhiểm độc giáp do co thắt cơ tim đẳng hình (quá tải khối lượng) của tâm thất trái và tình trạng quá tải hỗn hợp (quá tải cả thể tích và sức cản) của tâm thất phải, do đó suy tim thất phải thường gặp hơn ở trạng thái cường giáp. Suy và hỡ van ba lá đồng thời và sự hồi phục có thể làm trầm trọng thêm tình trạng này.
Suy tim (HF) trong nhiểm độc giáp phổ biến hơn ở người cao tuổi hơn là bệnh nhân trẻ với các cơ chế được nghiên cứu tốt hơn ở các nhóm tuổi. Đối tượng người cao tuổi thường có các bệnh tim mạch cùng đi kèm (bệnh động mạch vành, tim van bệnh, tăng huyết áp động mạch) dẫn đến thay đổi chức năng và cấu trúc cơ tim, do đó, khả năng co bóp cơ tim dễ bị suy giảm trong trường hợp quá tải cơ tim gây ra bởi cường giáp. Bệnh nhân cao tuổi bị rối loạn nhịp tim, chẳng hạn như rung nhĩ (AF), có nguy cơ phát triển suy tim cao nhất, vì rung nhĩ thường liên quan với nhịp tim tăng lên sau đó là suy giảm chức năng của tế bào cơ tim.
Trong khi đó những bệnh nhân trẻ tuổi không mắc bệnh lý tim mạch thường phát triển dạng suy tim tăng cung lượng Loại suy tim này được đặc trưng bởi cơ tim tăng tính co thắt. Ngoài ra suy tim với cung lượng thấp và giãn các buồng tim (bệnh cơ tim nhiểm độc giáp thể dãn ) cũng có thể phát triển ở những bệnh nhân trẻ tuổi trong trường hợp nhiễm độc giáp nặng và kéo dài. Tuy nhiên, thời gian cường giáp không phải lúc nào cũng rõ ràng, vì vậy các cơ chế vẫn chưa đầy đủ
Các cơ chế tự miễn dịch được coi là có khả năng (Kahaly, 1987; Koshiyama et al., 1996),nhưng giả thuyết này đã bị từ chối sau đó (Fatourechi & Edwards, 2000). Hai giả thuyếtđược thảo luận ngày nay. Theo một trong hai bệnh đầu tiên được cho là cùng tồn tại trên một cá nhân – Bệnh Graves, và bệnh cơ tim giãn vô căn (IDC). Nó được hỗ trợ bởi cơ chế bệnh sinh phổ biến của chúng – khuynh hướng di truyền được xác định bởi HLA haplotypes (Limas & Limas, 1989; Olson et al., 1992) và phối hợp chung của bệnh cơ tim dãn vô căn và bệnh tuyến giáp tự miễn (Markoviuel et al., 2005).
Theo giả thuyết thứ haiphì đại cơ tim kéo dài có thể chuyển thành cơ tim giãn và các buồng timgiãn có thể phát triển trong quá trình kéo dài không được điều trị và thậm chí ngay cả NĐGDLSDo đó, có hai cơ chế chính của sự phát triển suy tim trong nhiểm độc giáp
1) Suy timdo nhịp tim nhanh có rối loạn chức năng tâm thất trái (suy tim trái) phổ biến nhất ở bệnh nhân bị RN;
2) Suy tim phải là kết quả của sự quá tải khối lượng tâm thất phải do lượng máu tuần hoàn tăng và máu tĩnh mạch trở về được đặc trưng bởi sự giãn tâm thất phải, mở rộng vòng van ba lá và hở van ba lá và thường liên quan đến tăng áp phổi.
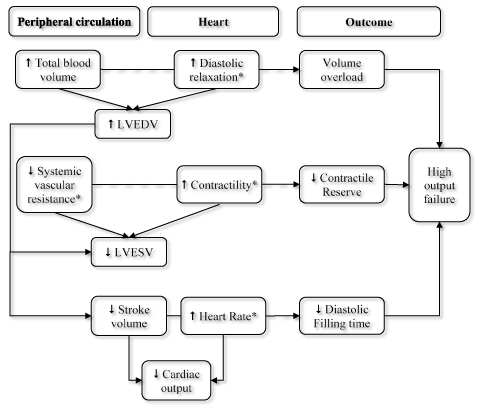
Hình 4. Tác dụng T3 trên chức năng tim gây suy tim giảm cung lượng
Tri-iodothyronine (T3) gây suy tim nhiểm độc giáp thông qua tác dụng của hormon lên tuần hoàn ngoại bên và tim làm gia tăng cung lượng tim, quá tải thể tích,rối loạn co bóp cơ tim và giảm làm đây tâm trương ( nguồn Toft & Boon, 2000)
TBV ( total blood volume):Thể tích máu toàn ,LVEDV ( left ventricular end diastolic volume): Thể tích thất trái cuối tâm trương,LVESV ( left ventricular end systolic volume): Thể tích thát trái cuối tâm thu,SV( stroke volume): thể tích tâm thu;SVR (systemic vascular resistance) Sức cản hệ thống thành mạch, CO (cardiac output): cung lượng tim
Ba giai đoạn của BCTNĐG được xác định: (1) tăng động hyperkinetic (có chức năng tâm thất trái bảo tồn, nhưng ở trạng thái hoạt động phân suất tống máu thất trái sẽ không tăng), (2) hoạt động bình thường (normokinetic) (một giai đoạn bù trừ với phì đại cơ tim hồi phục nhanh và cung lượng tim bảo tồn), và (3) giai đoạn giảm động (giai đoạn mất bù với cung lượng tim thấp và thể tích tim bóp, phì đại và dãn các buồng tim có thể hồi phục hoặc không hồi phục).
Huyết khối : Sự gia tăng xuất hiện các hiện tượng huyết khối động mạch (cao hơn so với dân số nói chung) là điển hình đối với nhiểm độc giáp và thậm chí cả khi không có rung nhĩ Sự rối loạn chức năng nội mạc là một lời giải thích cho tỷ lệ huyết khối cao,rối loạn đáp ứng giãn mạch khi tiếp xúc acetylcholine (Faber và cộng sự, 2001, Napoli và cộng sự., 2001) cũng như các tăng yếu tố dịch thể như yếu tố Von Willebrand (ǿucuianu et al. , 1989), chất kích hoạt plasminogen, endothelin (Baumgartner-Parzer và cộng sự, 1997) xác nhận sự kích hoạt huyết khốitrong nhiểm độc giáp (Homoncik và cộng sự, 2007).
Nhiểm độc giáp dưới lâm sàng gần đây đã cho thấy tác dụng tiền sinh huyết khối (Horne et al., 2004, Erem, 2006). Tăng hoạt tính của yếu tố Von Willebrand (Coban và cộng sự, 2006) và tăng nồng độ fibrinogen (Dörr và cộng sự, 2001) đã được chứng minh ở NĐGDLS.
4. LÂM SÀNG VÀ THĂM DÒ VỀ CHẨN ĐOÁN BỆNH CƠ TIM NHIỄM ĐỘC GIÁP
Các triệu chứng thường gặp nhất của BCTNĐG bao gồm hồi hộp, đau thắt ngực, khó thở, nhịp tim không đều. Nhịp tim nhanh và rối loạn nhịp tim, huyết áp tâm thu, hạ huyết áp tư thế đứng, tim lớn, thổi tâm thu tối đa van hai lá và ran ẩm trong trường hợp suy tim là những triệu chứng thường gặp nhất
Nhịp tim nhanh khi nghĩ và trong khi ngủ và gia tăng đáng kể nhịp tim khi gắng sức là điển hình cho nhiểm độc giáp. Nhịp tim nhanh có vị trí độc lập và có khả năng kháng trị với glycosides trợ tim.
Thông thường có mối liên quan trực tiếp giữa tần số tim và độ bướu giáp
Nhịp tim tăng lên 120-140 nhịp mỗi phút, và lên đến 160 nhịp mỗi phút và nhiều hơn khi đi lại , hoạt độngthể lực và cảm xúc.
Bệnh nhân than phiền về nhịp mạch đậpở cổ, đầu và bụng.
Rung nhĩ có thể có trong nhiểm độc giáp lâm sàng lẫn dưới lâm sàng và dạng tiềm ẩn. Do đó, như là một nguyên nhân tiềm ẩn nhiểm độc giáp nên được loại trừ ở tất cả các bệnh nhân có rung nhĩ dai dẵng kháng thuốc chống loạn nhịp. Rối loạn chức năng tuyến giáp là nguyên nhân gây ra 46% các rối loạn nhịp tim loại này.
Rung nhĩ kịch phát ngay giai đoạn khởi phát chứng nhiểm độc giáp thường chuyển thành dạng vĩnh viễn song song với sự tiến triển của bệnh.
Có một dạng đặc biệt của nhiểm độc giáp được đặc trưng bởi rung nhĩ kịch phát với nhịp xoang bình thường hoặc nhịp tim chậm mà không có bất kỳ triệu chứng nào khác về nhiểm độc giáp.Nồng độhormon giáp là rất quan trọng để chẩn đoán trong những trường hợp như vậy.
Khám lâm sàng cho thấy nhịp tim nhanh và mỏm tim đập mạnh. Bờ tim lan rộng sang trái, tiếng tim có cường độ mạnh, tiếng tim lớn và có thể nghe thấy tiếng thổi tâmthu . Huyết áp tâm thu tăng lên, trong khi huyết áp tâm trương nằm trong các giá trị bình thường hoặc giảm (dẫn đến áp lực xung cao, hoặc biên độ xung).
Phù do ứdịch thường gặp và có thể được tìm thấy ngay cả ở bệnh nhân có phân suất tống máu bảo tồn. Nếu các triệu chứng này liên tục xảy ra sau khi điều trị thành công nhiểm độc giáp thì phải loại trừ nguyên nhân khác.Mặt khác những người khoẻ mạnh, đánh trống ngực có liên quan đến giới tính nữ và tuổi trên 50, khó thở có liên quan đến giới tính nữ và nồng độ T4> 30 pmol/l. Sau khi bình giáp triệu chứng khó thở có thể tồn tại ở những người hút thuốc lá (Osman et al., 2007).
Suy tim liên quan đến tràn dịch màng phổi, và suy tim phải là phổ biến hơn ở bướu giáp lớn (Levina, 1989). Bệnh nhân bị bệnh cơ tim nhiểm độc giáp thể giãn có tim lớn và xung huyết phổi (Soh & Croxson, 2008) kèm các tiệu chứng lâm sàng về suy tim.
Chẩn đoán.
Thay đổi ECG bao gồm các sóng P và T cao, nhọn, rung nhĩ vàNgoại tâm thu, đoạn ST dẹt và sự đảo ngược sóng T có thể có mà không có triệu chứng đau thắt ngực và do những thay đổi về chuyển hóa. Thay đổi ECG có thể hồi phục nếu hormon tuyến giáp trở về bình thường.
Sự giãn của cả hai tâm thất và sự nới rộng của quai động mạch phổi (conus pulmonalis) là những dấu hiệu điển hình xquang về nhiểm độc giáp nặng. Mở rộng động mạch phổi và tâm thất phải lớn hình thành dạng hẹp van hai lá giả.
Tuy nhiên, không thấy có sự nỡ rộng tâm nhĩ trái ở phim nghiêng không giống như sự thay đổi hẹp van hai lá.Phù phổi là một dấu hiệu khác của x quang về bệnh cơ tim nhiểm độc giáp.
Siêu âm tim thấy phì đại thất trái bao gồm dày thành sau và dày vách liên thất, tăng thể tích cuối tâm trương và tăng khối cơ thất trái.
Bảng 2. Thông số siêu âm tim chẩn đoán suy tim nhiểm độc giáp ( Thyrotoxic heart failure)
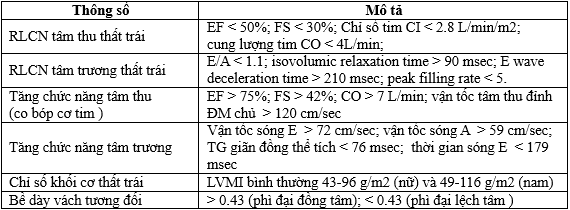
Chứng sa van hai lá cũng là một phát hiện thường gặp về nhiểm độc giáp. Sự giãn nở của tất cả các buồng tim và giảm chức năng tâm thu thất trái có thể được tìm thấy trong bệnh cơ tim NĐG thể dãn .
Khảo sát xạ hình tim bằng thallium chloride 201 thể hiện sự giảm hoạt động về trao đổi chất của tế bào cơ tim cí tính chất lan tỏa và khu trú.
Phương pháp chẩn đoán này cho phép đánh giá các tế bào tim còn nguyên vẹn và rất có ích để loại trừ tổn thương cơ tim ở những giai đoạn sớm của bệnh. Siêu âm tim gắng sức rất hữu ích cho việc đánh giá chức năng cơ tim dự trử (functional myocardial reserve) .
Tăng nồng độ hormon giáp và giảm TSH là những thông số quan trọng để xác nhận nguyên nhân (nhiểm độc giáp) trên lâm sàng.
5. ẢNH HƯỞNG CỦA CÁC YẾU TỐ TRONG BIỂU HIỆN LÂM SÀNG BỆNH CƠ TIM NHIỄM ĐỘC GIÁP
5.1. Giãn nhĩ trái và rung nhĩ
Phì đại nhĩ phải liên quan đến giãn và kiểm tra bằng điện tim được tìm thấy ở 30,5% bệnh nhân bị nhiểm độc giáp, phì đại thất trái – 13,7%, và phì đại 2 nhĩ ở 11,8% bệnh nhân.
Sự xuất hiện rung nhĩ ở nhiểm độc giáp rất khác nhau tùy thuộc vào dân số nghiên cứu. Tuổi, giới tính, mức độ nghiêm trọng và cường độ của chứng tăng hoạt giáp và các bệnh tim mạch đồng thời ảnh hưởng đến tần suất của rung nhĩ.
Tuổi : Sự liên quan về tuổi đãđược biết về nguy cơ phát triển rung nhĩ tăng lên khi bệnh nhân già đi.Do đó, theo dõi 10 năm, tỷ lệ mắc chứng rung nhĩ là 25% ở bệnh nhân trên 65 tuổi bị nhiểm độc giáp, thậm chí ở dạng cận lâm sàng, và đây là nguy cơ gấp 3 lần so với TSH bình thường (7%). Tỷ lệ hiện mắc của RN là 21% trong tổng số bệnh nhân có tình trạng nhiểm độc giáp lâm sàng và 31% ở bệnh nhân trên 40 tuổi, trong khi ở những người dưới 40 tuổi ghi nhận không có trường hợp nào. Trong một nghiên cứu khác ghi nhân đối tượng nhiểm độc giáp trên 60 tuổi có RN là 25% so với 5% ở nhóm trẻ (Agner et al., 1984).
Phân tích hồi quy được thực hiện bởi Nakazawa H. (2000) đã chứng minh sự phụ thuộc tuổi tác vào tỷ lệ RN tăng dần theo từng giai đoạn cho đến những giá trị tối đa ở bệnh nhân trên 70 tuổi.
Giới tinh : Nam giới là một yếu tố nguy cơ khác của N (Staffurt et al., 1977). Toft A. & Boon N (2000) báo cáo tỷ lệ hiện nhiễm trên 50% ở nam giới ở độ tuổi 60 bị cường giáp.
Thời gian nhiểm độc giáp ít khảo sát .RN khá hiếm gặp (ít hơn 2%) ngay khi khởi phát chứng nhiểm độc giáp (Nakazawa và cộng sự, 2000) và ở bệnh nhân dưới 40 tuổi mà không có các bệnh tim mạch đi kèm (Toft A. & Boon N (2000).
Một số các yếu tố sau đây được coi là quan trọng nhất cho sự phát triển RN ở những bệnh nhân trẻ tuổi mà không có bệnh lý tim mạch: thời gian nhiểm độc giáp (p = 0,0005, OR = 72 (6,6-794)), giới tính nam (OR = 10,4 (3 , 0-36,0), p = 0,0003) và nhịp tim (OR = 1,07 (1,03-1,11) Ȟ = 0,0001) (Babenko và cộng sự, 2011). Những yếu tố này cũng rất quan trọng trong trường hợp bệnh nhân có bệnh tim mạch đi kèm.
Sau khi khảo sát 40 628 bệnh nhân nhiểm độc giáp Frost (2004)ghi nhận nguy cơ cao nhất của RN liên quan đến nam giới, bệnh động mạch vành và suy tim sung huyết. J. Mercé et al. (2005) phát hiện thấy sự xuất hiện của RN ở bệnh nhân nhiểm độc giáp với triệu chứng hỡ van hai lá hoặc 3 lá (40% so với 14%, P = 0,02 ở hỡ 2 lá và 86% so với 3%, P = 0,01 ở hỡ van 3 lá).
Mức độ nhiểm độc giáp : Dữ liệu về ảnh hưởng của cường độ nhiểm độc giáp (lâm sàng hoặc cận lâm sàng) đang còn tranh luận i. Auer và cộng sự (2001) báo cáo nguy cơ tương đối tương tự của RN trong cả NDGDLS và nhiểm dộc giáp lâm sàng (lần lượt là 12,7% và 13,8%). Theo các dữ liệu khác, sự xuất hiện của RN ở NĐGDLSlà 7% so với 16% trong nhiễm độc giáp lâm sàng (Babenko và cộng sự, 2011).
Loại hormon giáp ưu thế : Có sự liên quan giữa xuất hiện rung nhĩ và loại hormon giáp tăng ưu thế (T3 hoặc T4). Do đó, rung nhĩ xảy ra ở 36% bệnh nhân nếu T3 tăng cao, trong 13% nếu T4 tăng và 21% nếu mức độ của cả hai hormone tuyến giáp cao.
Do đó, sự xuất hiện tần suất cao nhất của rung nhĩ đã được quan sát thấy trong nhiểm độc giáp do T3 đơn độc. Tuy nhiên, sự khác biệt có thể được giải thích bởi thời gian khác nhau của bệnh: nhiểm độc giáp T3 đơn độc phát triển trong nhân giáp tự độngđặc trưng bởi giai đoạn không triệu chứng kéo dài và tăng chậm mức hormon tuyến giáp ở lần đầu tiên dẫn đến chứng NDGDLS và sau đó nhiểm độc giáp do T3 . Sự chuyển đổi RN sang nhịp xoang chỉ được báo cáo ở 19% bệnh nhân bị chứng rung nhĩ và chứng NĐGDLS.
Các yếu tố nguy cơ cho rung nhĩ bao gồm : Tuổi, nam giới,thời gian bị cường giáp, tần số tim và bệnh tim mạch đi kèm
Tiêu chuẩn ECG có thể được sử dụng để xác định các bệnh nhân có nguy cơ cao ở bệnh nhân NĐGDLS có khoảng PR ngắn trong nhóm người có xu hướng nhịp nhanh xoang nhĩ thất vào lại (Biondi B và cộng sự, 1998) và những người có thời gian sóng P cao và hai đỉnh (p wave diperson) có khuynh hướng RN (Aras D và cộng sự, 2005).
Ở những bệnh nhân có xu hướng (những người có hai mô hình biểu hiện khác nhau về chức năng dẫn truyền nhĩ thất), liệu pháp l-thyroxine (l-T4) có thể làm tăng sự xuất hiện của nhịp nhanh xoang nhĩ thất vào lại do kích thích nhĩ làm tăng số lượng ngoại tâm thu nhĩ và rút ngắn thời kỳ trơ củadẫn truyền trong cơ tim (Biondi B et al, 1998). Hơn nữa, bằng cách đo các giá trị P tối đa và P hai pha, một trong những phương pháp lý thuyết có thể xác định được bệnh nhân có NĐGDLS cónguy cơ cao về RN .
Holter ECG có thể được thực hiện trước khi bắt đầu điều trị bằng l-T4 trong liều ức chế TSH để phát hiện những bệnh nhân không dung nạp với điều trị bằng l-T4
5.2. Phì đại thất trái (PĐTT)
Chỉ số khối cơ thất trái (LVMMI)trên bệnh nhân nhiểm độc giáp còn bị tác động bởi nồng độ T3, huyết áp tâm thu và chỉ số khối cơ thể (Marcisz và cộng sự, 2006). Tái cấu trúc thất trái lệch tâm là chủ yếu và điều trị phục hồi bình giáp không liên quan đến bình thường hóa LVMI (theo dõi 9 tháng).
Giới tính cũng ảnh hưởng đến sự xuất hiện của PĐTT ở bệnh nhân bị nhiểm độc giáp : tỷ lệ PĐTT ở nam cao hơn nữ (21,3% so với 30,6%, OR = 3,6; CI (1 , 8, 7,4), p = 0,05). PĐTTdạng lệch tâm xuất hiện ở 18,2%, và đồng tâm 4,3%, việc tái tạo đồng tâm xảy ra ở 7,4% bệnh nhân (Babenko và cộng sự, 2011).Tỷ lệ PĐTT gia tăng ở người cao tuổi, tuy nhiên, phụ thuộc vào tuổi tác là khác nhau ở nam và nữ giới. Sự tương quan giữa LVMI và tuổi tác là quan trọng trong tổng số dân số (r = 0,22, p = 0,0007) và ở nữ (r = 0,27, p = 0,0002), so với sự liên quan không đáng kể ở nam giới (r = 0,10, p = 0,58). Phân tích chính xác hơn rằng các thông số này liên quan không tuyến tính, và sự biến đổi của LVMI tăng ở những người lớn tuổi. Phân tích hồi quy tuyến tính xác định ngưỡng tuổi 44 tuổi: LVMI không thay đổi đến giới hạn này và tăng nhanh ở những người lớn tuổi hơn 10 g / m2.
Điều này cũng rõ hơn ở phụ nữ: LVMI trung bình là 90 ± 20 g / m2 ở phụ nữ trẻ hơn 44 tuổi và 105 ± 25 g / m2 ở phụ nữ người cao tuổi. Tỷ lệ phì đạithất trái tăng đáng kể từ 11 đến 36% (OR = 4 T,4, CI (2,1, 9,1), p = 0,0002). Mức tăng LVMI tương tự được ghi nhận ở nam giới – từ 117 ± 27 đến 124 ± 36 g / m2, nhưng sự thay đổi các giá trị LVMI và tỉ lệ LVH không đáng kể do biến đổi LVMI cao (và nhóm nhỏ hơn) (p = 0,63) (Babenko Et al., 2011).
Rung nhĩ là một yếu tố khác liên quan đến cả sự có mặt và mức độ nặng nhẹcủa LVM( giá trị LVMI (Babenko và cộng sự, 2011).
Các yếu tố ảnh hưởng đến PĐTT trong chứng NĐGDLS chưa được khảo sát hoàn toàn. Shapiro L.C. et al. (1997) không thấy sự phát triển của PĐTT trong NĐGDLS kéo dài (9,2 ± 5,4 năm) và TSH rất thấp TS -0,001 mIU / l ở những người có NNĐGDLSnội sinh (trung bình 45 ± 10 năm (27-63)). Biondi B. еt al. (2000) báo cáo có sự gia tăng đáng kể LVMI (162 ± 24 g / m2) ở nhóm tuổi phù hợp (43±9 năm (27-69)) với NĐGDLS nội sinh nhưng với các giá trị TSH cao hơn (0,15 mIU / l) và thời gian ngắn hơn của chứng NĐGDLS (6 tháng), tuy nhiên, cần lưu ý 80% trong nhóm nghiên cứu là phụ nữ.
Các tác giả cũng cho thấy tương quan dương giữa LVMI và thời gian và liều L-thyroxin ở bệnh nhân có NĐGDLS nội sinh. Có bằng chứng về các cơ chế cơ bản khác nhau của sự phát triển của PĐTT đối với chứng nhiểm độc giáp lâm sàng và dưới lâm sàng (Donatelli và cộng sự, 2003), mặc dù mức PĐTT là tương đương. PĐTT đã phát triển thậm chí ở NĐGDLS với nhịp tim , huyết áp và chức năng thất trái tâm thu bình thường điều này cho thấy tác dụng trực tiếp của hormon giáp.
LVMI cao hơn ở những bệnh nhân NĐGDLSvới nguyên nhân khác nhau ( do thuốc, cường giáp tự miễn Graves giai đoạn dưới lâm sàng và do u tuyến giáp độc) so với nhóm đối chứng theo tuổi và giới tính (p<0,005). Tỷ lệ hiện mắc LVH là 39% (43 bệnh nhân, 45,5% ở nam và 38,4% ở nữ) ở NĐGDLS.
Không có sự khác biệt về nguyên nhân và thời gian NĐGDLS. Nam giới là một yếu tố nguy cơ cho LVH ở NĐGDLS cũng như trong cường giáp lâm sàng (Babenko và cộng sự, 2011).
Tuổi và huyết áp tâm thu là hai yếu tố nguy cơ khác đối với PĐTT (Babenko và cộng sự, 2007). Vì vậy, các yếu tố nguy cơ cho sự PĐTT và rung nhĩ là khác nhau . Tóm lại các yếu tố nguy cơ đối với chứng phì đại thất trái bao gồm Tuổi tác, Nam giới, Thời gian nhiểm độc giáp, tăng huyết áp và bệnh tim mạch đồng thời
5.3. Tăng áp phổi
J. Mercé et al. (2005) đã phân tích dữ liệu về tăng áp phổi và các yếu tố nguy cơ.
Tăng áp phổi (TAP) xảy ra ở 41% bệnh nhân bị nhiểm độc giáp. Các bệnh nhân nhiểm độc giáp và hở van 2 lá và 3 lá có áp lực ĐM phổi cao hơn: 53,8 so với 34,9 mmHg, P = 0,0001 trong hở 2 lá , 43,9 so với 35,12 mmHg, P = 0,07 ở hở van tricuspid
Không có mối liên hệ giữa TAP và các yếu tố sau: tuổi tác, giới tính, nguyên nhân của tăng năng tuyến giáp, các triệu chứng tim mạch hoặc các triệu chứng khác, nhịp tim và loại rối loạn nhịp tim, nồng độ các kháng thể thyroperoxidase, TSH, và hormon giáp. Tăng áp phổi tồn tại 16% đối tượng sau khi tuyến giáp phục hồi .
Một số nghiên cứu phát hiện 39% TAPcủa nhiểm độc giáp và áp lực ĐM phổi giảm xuống đến các giá trị bình thường ở 61,5% bệnh nhân sau khi đạt bình giáp. Sự gia tăng áp lực phổi liên quan đến nồng độ FT4 trước điều trị (r = 0,5, p = 0,0001), tuổi (r = 0,25, p = 0,002) và chức năng giãn mạch nội mạc , r = -0,37, p = 0,002).
Đường kính tâm thất phải tương quan với áp suất ĐM phổi (r = 0,36, p = 0,0001), và được coi là dự báo của TAP vì tăng áp lực ĐM phổi lên 100% ở những bệnh nhân có giãn tâm thất phải và áp suất ĐM phổi bình thường ban đầu.
Theo dữ liệu TAP xảy ra ở 29,6% bệnh nhân bị NĐGDLS.Sự xuất hiện này cao nhất (37,5%) ở những bệnh nhân có NĐGDLSnội sinh không do tự miễn (nhân giáp tự trị). T3 tự do và mức độ ức chế TSH có tác động lớn nhất. Như vậy có tương quan giữa áp suất phổi và nồng độ FT3 (r = 0,56, p <0,001) và TSH (r = -0,34, p <0,005). nồng độ cao hơn FT3 dường như là nguyên nhân của sự gia tăng áp lực phổi ở NĐGNS nội sinh không do tự miễn (Babenko và cộng sự, 2008).
5.4. Suy tim
Các yếu tố nguy cơ gây suy tim hình thành trong nhiễm độc giáp chưa rõ. Theo báo cáo của Siu C-W et al. (2007), 5,8% bệnh nhân nhiểm độc giáp bị suy tim, và RN là một dự báo độc lập về suy tim (OR 37,4 (CI 9,72- 144,0, p <0,001)). 47% có rối loạn chức năng tâm thất (EF <50%), nghiêm trọng hơn ở bệnh nhân có nồng độ TSH huyết thanh thấp nhất. Nam giới liên quan đến sự phát triển của suy tim (OR 26,6 (CI 2,6-272,5), p = 0,006). Rối loạn chức năng thất trái và sự giãn buồng tim ở 1/3 bệnh nhân có chức năng tuyến giáp đã hồi phục. Các bệnh nhân có cung lượng tim đảm bảo (phân suất tống máu 55% so với 30%, p <0,001) và mức độ suy tim thấp hơn (NYHA) cho thấy kết quả tốt hơn (thay đổi ngược) (1,2 (0,1) so với 2,5 (0,2), p <0,001 ).
Các yếu tố dự báo chính sau đây về sự phát triển suy tim trong nhiễm độc tuyến giáp (Babenko và cộng sự, 2011) được xác định bằng phân tích đa yếu tố: huyết áp tâm thu và nồng độ FT3 trước khi điều trị, giãn tâm thất trái và ở các buồng tim khác.
Tóm lại, thời gian của cường giáp, giới tính (nam) và tuổi tác là những yếu tố dự báo chính cho sự phát triển BCTNĐGvà các biểu hiện lâm sàng của bệnh (lớn nhĩ trái, rung nhĩ, PĐTT và suy tim ).
6. DỰ BÁO VÀ ĐIỀU TRỊ BỆNH CƠ TIM NHIỄM ĐỘC GIÁP DỰA TRÊN PHÂN TẦNG NGUY CƠ CỦA BỆNH.
Cách tiếp cận điều trị nên xem xét các yếu tố ảnh hưởng đến sự phát triển của BCTNĐG vì sự thay đổi tim mạch liên tục có ảnh hưởng xấu đến tiên lượng tim mạch.
Các hướng dẫn Châu Âu về quản lý bệnh bướu giáp độc lan tỏa đưa ra chiến lược sau:
Nên điều trị bảo tồn bằng các thuốc kháng giáp trong 18 tháng với việc rút lui sau đây trong trường hợp đạt được sự thuyên giảm, nếu không thì nên điều trị phương pháp không dùng thuốckháng giáp (không hồi phục).
Đạt trạng thái bình giáp kéo dài có tầm quan trọng rất lớn trong việc kiểm soát các triệu chứng BCTNĐG, trong khi thời gian bệnh nhiểm độc giáp dài hơn và tuổi cao hơn liên quan đến tiên lượng tim mạch. Trong nghiên cứu (Babenko và cộng sự, 2011), thời gian trung bình nhóm cường là 10 tháng (6, 16) ở phụ nữ không có PĐTT và 10 tháng (6; 15) ở nam giới, trong khi đó đến 20 tháng (9 , 40) ở phụ nữ có PĐTT (p = 0,006) và đến 19 tháng (12,30) ở nam giới có PĐTT (p = 0,09).
Do đó, nguy cơ PĐTT thấp có thể nhiểm độc giáp kéo dài dưới 10 tháng nhưng cao hơn đáng kể trong các bệnh nhân kéo dài hơn. Ngoài ra, nguy cơ PĐTT ở phụ nữ trên 44 tuổi cao hơn, nhưng nam giới lại phụ thuộc vào tuổi tác. Sự khác biệt về độ tuổi và giới tính nên được xem xét trong thực hành lâm sàng và nên xét điều trị không dùng thuốc sớm (sau 8-10 tháng điều trị kháng giáp ) ở tất cả các đối tượng nam và ở phụ nữ trên 44 tuổi. Mặt khác, PĐTT ở một bệnh mới được chẩn đoán là nhiễm độc tuyến giáp là dấu hiệu của bệnh lý nhiểm độc giáp đã kéo dài và tổng thời gian của nó có thể dài hơn thời gian đã đề cập trên và đối tượng này nên được điều trị ngay từ đầu thể không thể đảo ngược. Ngoài ra tăng huyết áp tâm thu nặng có dự báo xấu về tiên lượng tim mạch và cần phải điều trị tích cực .
Việc lựa chọn phương pháp điều trị không dùng thuốc kháng giáp( phẫu thuật hoặc điều trị phóng xạ) không phải luôn luôn dễ dàng ở những bệnh nhân có BCTNĐG. Thật vậy điều trị phẫu thuật có liên quan đến nguy cơ cao trong và sau mổ. Điều trị iode phóng xạ có liên quan đến tiên lượng xấu hơn. Phương pháp điều trị phóng xạ gây viêm giáp do phóng xạ dẫn đến chứng “nhiểm độc giáp ” rò rỉ, làm tái phát rung nhĩ, co thắt mạch vành và xãy ra các biến cố về tim mạch (nhồi máu cơ tim, đột quỵ, nhồi máu phổi). Điều trị I131 có liên quan đến tỷ lệ tử vong sớm cao ở 1-2 tháng sau khi can thiệp trùng với thời gian khởi phát viêm giáp do phóng xạ..
Do nguy cơ tim mạch đã tăng lên ở bệnh nhân NĐGDLS trước đó, nên điều trị NĐGDLS nội sinh (thuốc kháng giáp hoặc phóng xạ)cho những bệnh nhân này. Hồi phục bình giáp cải thiện các thông số tim mạch (giảm nhịp tim, giảm số lượng nhĩ và thất, giảm khối cơ thất trái và cung lượng tim) (Biondi and Cooper, 2008).
Ở những bệnh nhân lớn tuổi, cần tránh bất cứ khi nào có thể vềNĐGDLS ngoại sinh. Các hướng dẫn gần đây không khuyên cáo dùng LT4 nhằm ức chế TSH huyết thanh xuống dưới 0,1 mIU / lít của các bệnh nhân nhân giáp lành tính. Điều trị ức chế dài hạn với nồng độ TSH huyết thanh dưới 0,1 mIU / l được khuyến cáo cho bệnh nhân BCTNĐG thể dãn với bệnh dai dẳng và có nguy cơ tái phát cao.
Thuốc Ức chế beta có thể được xem xét trong những bệnh nhân ung thư tuyến giáp có nguy cơ cao liên quan tăng đáp ứng adrenergic với l-T4 (Biondi và cộng sự, 2005).
Việc điều trị triệu chứng của BCTNĐG nên dựa vào cơ chế sinh bệnh cơ bản. Về mật độ β-adrenoreceptor cao, nhịp tim nhanh do tăng hoạt tính adrenergic và tăng thể tích tim , cần phải sử dụng thuốc β-blockers và thuốc lợi tiểu.
Thuốc lợi tiểu có tầm quan trọng rất lớn đối với bệnh nhân có các triệu chứng suy tim sung huyết phổi (phù, khó thở). Thuốc chẹn beta không ảnh hưởng đến việc giải phóng hocmon tuyến giáp và được sử dụng để giảm sự tăng hoạt tính giao cảm, dẫn đến giảm tải tim và nhu cầu oxy cơ tim. Sự lựa chọn β-blocker là một câu hỏi được thảo luận nhiều cho đến ngày nay. Một mặt, sự hoạt động kháng giáp của các thuốc chẹn β-beta không chọn lọc (ví dụ propranolol) đã được biết. Có bằng chứng cho thấy thuốc chẹn beta (propranolol) ảnh hưởng đến sự trao đổi chất của các hormon tuyến giáp bằng cách ức chế deiodinase type 2 trong các mô khác nhau bao gồm tế bào tim và sự chuyển đổi T4 thành T3dạng không hoạt động.
Deiodinase là selenoenzyme điều hòa sự chuyển hóa thyroxine (T4) thành triiodothyronine (T3) (Bianco và cộng sự, 2002, Kohrle, 1999).
Loại deiodinase týp 1 (D1) có trong gan, thận và tuyến giáp (Bianco và cộng sự, 2002, Peeters và cộng sự, 2003) và được cho là đóng vai trò quan trọng trong sản xuất T3 hoạt động (Kohrle, 1999).
Loại deiodinase týp 2 (D2) cho phép tạo T3 trong các tổ chức bao gồm hệ thần kinh trung ương, tuyến yên, mô mỡ nâu, cơ tim, cơ bắp, tế bào xương; Và nó ít trình diện tại gan và thận (Bianco et al. 2002, Kohrle, 1999, Peeters et al 2006)
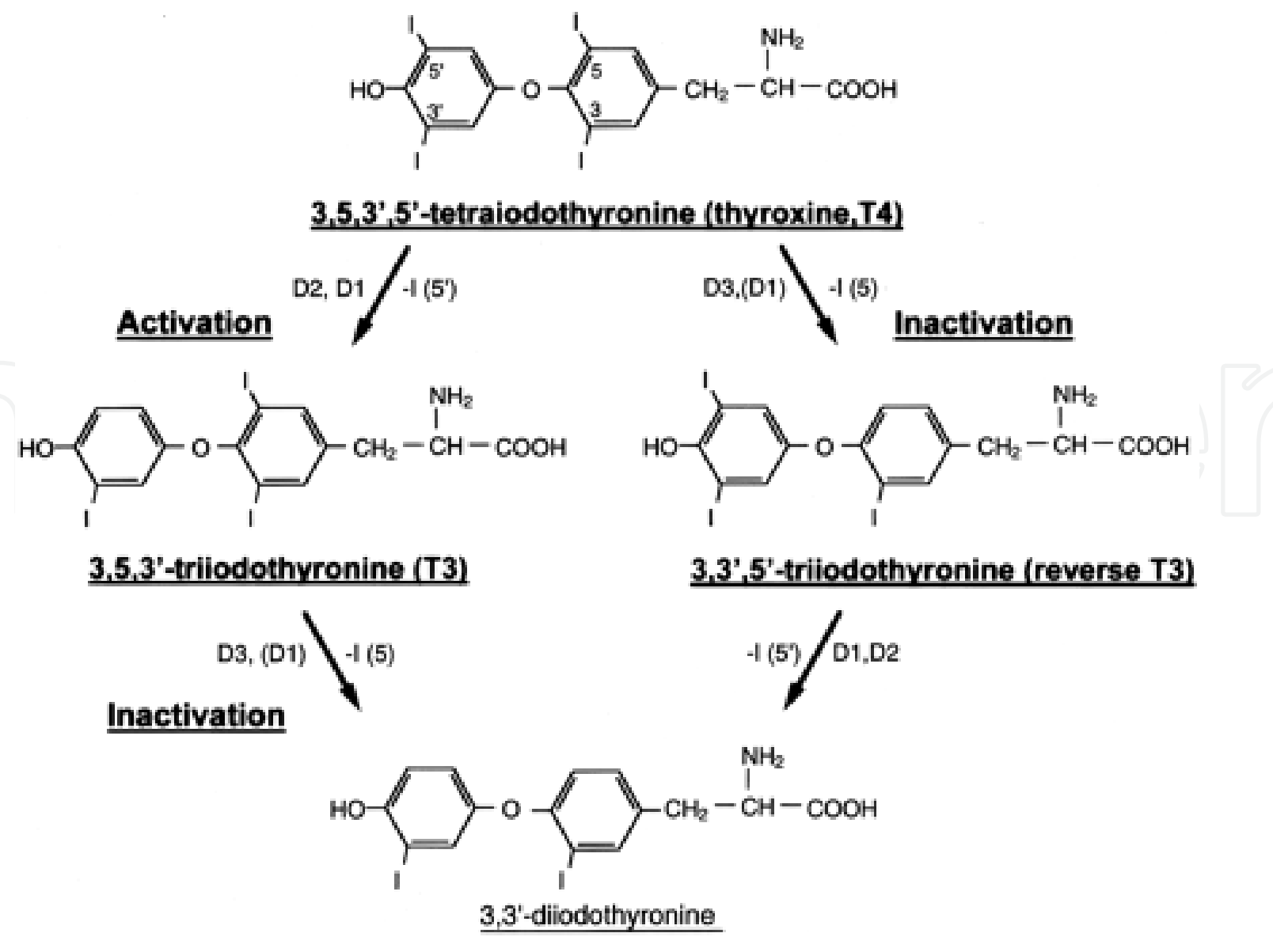
Hình 5. Cấu trúc và liên quan giữa iodothyronin hoạt hóa và không hoạt hóa bởi enzyme selenodeiodinase enzyme(from A. Bianco, 2002)
Do đó, D2 đóng vai trò chính trong sản xuất T3 tổ chức, tuy nhiên hoạt động của D2 trong cơ bắp đóng góp lớn vào đầu ra dấu ấn huyết thanh (Peeters et al, 2006,
Maia, 2005). Do đó, nồng độ FT3 trong các mô phụ thuộc vào cả tổng hợp T4 trong
tuyến giáp và tương ứng nồng độ T4 lưu hành và hoạt động deiodinase trong các mô. Sự đóng góp của D1 làm thay đổi từ 15-39% trong hầu hết các nghiên cứu đến 80% (Bianco et al.2002, Pilo, 1990) (hình.5).
Nồng độ T3 tổ chức ít phụ thuộc vào nồng độ huyết tương của hormon giáp như khi hoạt động của D2 có thể đóng góp vào lượng T3 lớn hơn. Kết quả là nồng độ T3
có khác nhau trong các cơ quan và mô khác nhau.Ví dụ, T3 bão hòa khoảng 50% ở gan và thận trong khi nó chiếm tới 95% ở hệ thống thần kinh trung ương (Bianco A et al. 2002). Theo dữ liệu khoa học, hoạt động D2 tăngnhiều lần trong một số mô ở bệnh nhân Basedow. hoạt động cao của D2 ghi nhận trong mô tuyến giáp được chiết xuất từ bệnh nhân mắc bệnh Graves lúc phẫu thuật(Salvatore et al, 1996). Có dữ liệu cho thấy các biểu hiện lâm sàng của nhiểm độc giáp không phải lúc nào cũng tương quan với nồng độ hormone giáp lưu hành. B.Biondi et al. (2000) sử dụng bảng câu hỏi (với thang điểm triệu chứng đặc biệt) cho thấy thyrotoxic biểu hiện triệu chứng ở một số bệnh nhân bị NĐGDLS.
Khám tim mạch của những bệnh nhân này (Siêu âm tim (EchoCG), nghiệm pháp gắng sức, điện tâm đồ, v.v.) cũng cho thấy những thay đổi bệnh lý nghiêm trọng (tỷ lệ rối loạn nhịp nhĩ cao, phì đại tâm thất trái, rối loạn chức năng tâm trương). Các tổn thương tim tương tự như mô tả ở bệnh nhân nhiểm độc giáp được biểu lộ trong thí nghiệm liên quan đến chuột với hoạt động biểu hiện gen D2 cao trong tế bào cơ tim (Pachucki et al, 2001).
Dựa trên những dữ liệu này, người ta cho rằng mức độ nghiêm trọng của nhiều thay đổi bệnh lý bao gồm bất thường về tim mạch ở bệnh nhân mắc bệnh Graves, có thể liên quan đến cả hai nồng độ hormon giáp lưu hành và sản xuất T3 phụ thuộc deiodinase tại mô. Đặc biệt, tiêu thụ năng lượng trong cơ đã được chứng minh là tương quan với FT4 và TSH, nhưng không phải với nồng độ FT3 (Canani et al, 2005).
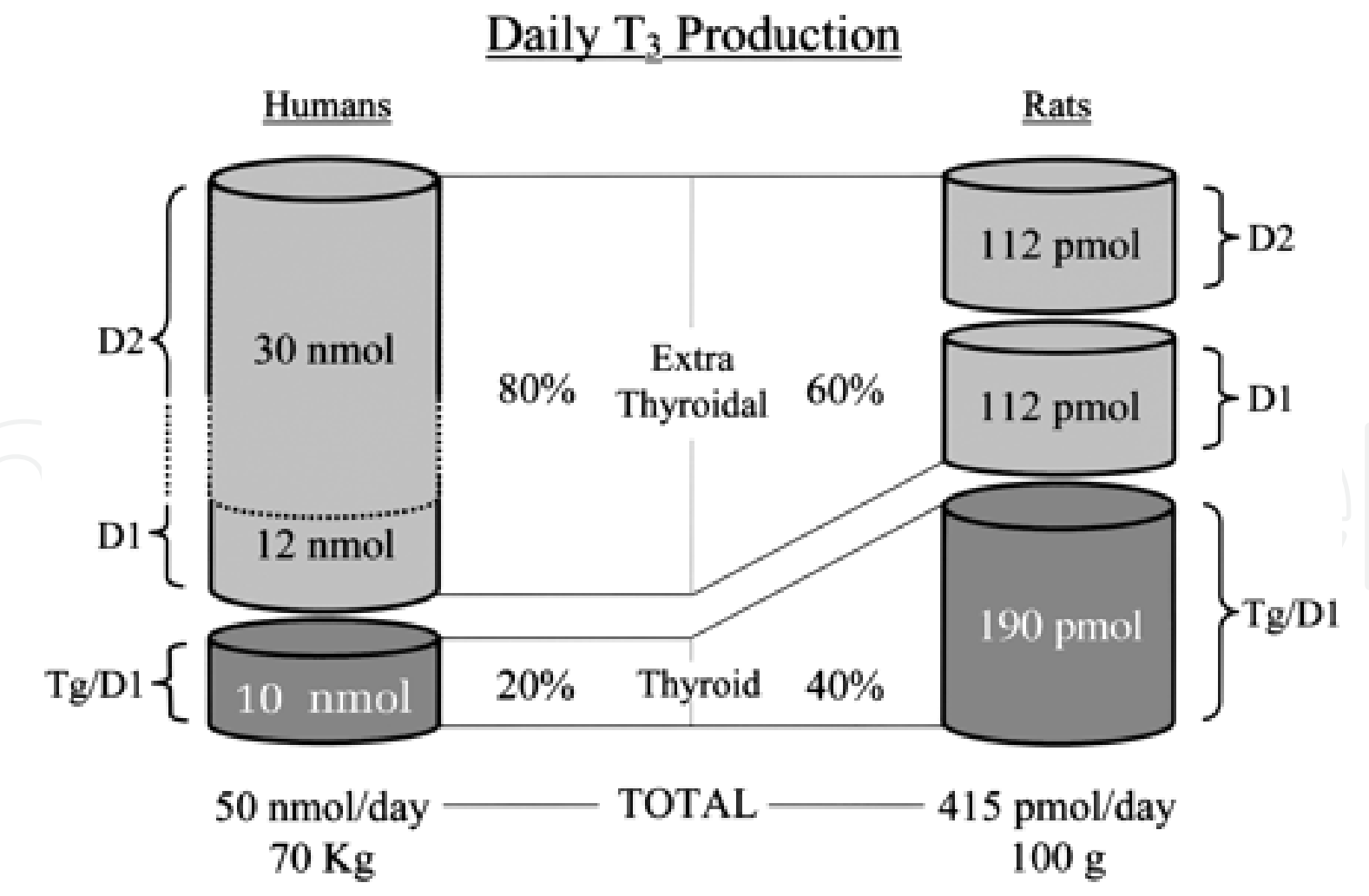
Hình 6. Con đường sản xuất T3 ở người và chuột. Các đường chấm trong xi lanh
đại diện cho sản xuất ngoài tuyến giáp của người phản ánh sự không chắc chắn về chính xácđóng góp của D1 và D2 đối với dự trử này.
Loại D2 được xem là có vai trò chính trong sự thay đổi nồng độ T3 mô, ít nhất tại các mô (như cơ tim, thành mạch) có biểu hiện gen D2 cao. Một trong chúng được tìm thấy ở người và bao gồm các đa hình D2 được đặc trưng bởi threonine (Thr) thay đổi cho alanine (Ala) trong codone 92 (D2 Thr92Ala). Bệnh nhân đồng hợp tử Ala / Ala biểu hiện hoạt động của mô D2 thấp hơn so với điện ly / Thr bệnh nhân dị hợp tử và bệnh nhân đồng hợp tử Thr / Thr. Do đó, tính đa hình này có thể làm giảm tác dụng T3 ở các mô có biểu hiện gen D2 cao (Bianco et al. 2002, Kohrle, 1999). Do đó, tính đa hình này được đề nghị ảnh hưởng đến các biểu hiện lâm sàng và mức độ nghiêm trọng của tổn thương tim ở bệnh nhân thyrotoxicosis. Nghiên cứu cho thấy rằng đa hình Thr92Ala D2 có thể tác động đến tiến trình lâm sàng của bệnh Graves và tổn thương tim (Grineva et al, 2009).
Nồng độ T3 và chỉ số T3 / T4 trước khi điều trị được coi là yếu tố dự báo sự phục hồi bệnh Graves.. Có sự khác biệt đáng kể giữa các tham số này tùy thuộc vàoSự xuất hiện đa hình của Thr92Ala D2 chứng tỏ vai trò của nó như là một yếu tố dự báo bệnh Graves.tiên lượng. Nó được xác nhận bởi sự khác biệt đáng kể về thời gian mắc bệnh trong các nhómbệnh nhân có kiểu gen khác nhau. Dạng đa hình Thr92Ala D2 dường như được bảo vệ nhưthời gian mắc bệnh và tỷ lệ tái phát thấp hơn đáng kể ở người đồng hợp tử Ala / Alabệnh nhân. Điều này dẫn đến sự ức chế các hiệu ứng T3 trong các mô có biểu hiện D2 cao, chẳng hạn như:tim, tuyến giáp và tuyến yên.
Dữ liệu chứng minh rằng đa hình Thr92Ala D2 có thểtác động đến các biểu hiện lâm sàng của bệnh Graves, bao gồm tăng thể tích tuyến giáp và timtỷ lệ. Bệnh nhân đồng hợp tử Ala / Ala cho thấy nhịp tim thấp hơn so với dị hợp tử và Thr / Thrnhững người đồng hợp tử. Tất cả những đặc điểm lâm sàng này (nồng độ hormone và nhịp tim thấp hơn, ít hơnthời gian thyrotoxicosis) góp phần vào bệnh cơ tim thyrotoxic ít nghiêm trọng hơn ở Ala / Alabệnh nhân đồng hợp tử.
Kiểu gen Ala / Ala của đa hình D2 cũng bảo vệ làm giảm nguy cơ PĐTT vàloại tiên lượng xấu đến tái cấu trúc (phì đại đồng tâm và giãn buồng tim). Do đó, thuốc giảm hoạt động D2 có thể dẫn đến giảm các biểu hiện lâm sàng của BCTNĐG, tuy nhiên, vẫn chưa có nhiều bằng chứng (Grineva et al, 2009).
Điều cần lưu ý liều cao propranolol (trên 160 mg mỗi ngày) có thể làm giảm đáng kểnồng độ T3 trong huyết tương (khoảng 30%) đồng thời liều này có thể gây giảm huyết áp nghiêm trọng ở phần lớn bệnh nhân (chỉ đạt mức độ bình thường) và một số ít người trong số họ tăng huyết áp tâm thu.
Mặt khác, mật độ β1-adrenoreceptor là yếu tố gia tăng trong nhiểm độc giáp. Thuốc ức nchế chọn lọc β1-blockers có hiệu quả hơn. Tuy nhiên, lợi thế của bất kỳ thuốc β-blocker nào trong quản lý BCTNĐGchưa có minh chứng, do đó, sự lựa chọn dựa trên những ưu điểm khác, ví dụ: Liều lượng: dùng thuốc một hoặc hai lần hàng ngày. Cần phải nói rằng những người già cũng như những bệnh nhân có suy tim cung lượng thấp và huyết áp thấp có nguy cơ hạ huyết áp (đặc biệt là hạ huyết áp tư thế) khi điều trị bằng thuốc chẹn beta. (15) Các nhóm thuốc chẹn beta chọn lọc liều thấp – betaxolol, atenolol, metoprolol liều thấp – thích hợp hơn trong nhóm bệnh nhân này và ở những bệnh nhân có chống chỉ định tương đối (ví dụ tắc nghẽn phế quản) đến các thuốc chẹn beta. Thuốc chẹn beta thường được dùng trong khi trạng thái tuyến giáp đạt được, và sau đó liều sẽ dần dần bị giảm đi và ngưng, trong một số trường hợp nếu cần thiết, liều lượng thấp sẽ được duy trì trong một thời gian dài. Loại chỉ định sau bao gồm nhịp tim nhanh kháng thuốc kháng giáp, rối loạn nhịp tim như ngoại tâm thu và rung nhĩ; Suy tim do tăng co bóp cơ tim . Thuốc chẹn beta nên sử dụng trước khi có hiệu quả các tác dụng của thuốc kháng giáp hoặc điều trị phóng xạ, cũng như trong cơn bão giáp và như là một phần của việc chăm sóc trước mổ.
Liệu pháp kết hợp bằng thuốc chẹn beta và thuốc kháng giáp có một số lợi ích về tim mạch so với đơn trị liệu. Tuy nhiên, cần đánh giá tính nhạy cảm của từng cá thể về chẹn beta. Giảm nhịp tim và không có các phản ứng phụ là những dấu hiệu chính của liều ức chế beta dùng chính xác. Hiệu quả lâm sàng tích cực đáng kể thường thấy rõ sau 5-7 ngày điều trị bằng thuốc chẹn beta, bao gồm giảm sự hoạt tính giao cảm và các triệu chứng có liên quan, giảm nhịp tim (nhịp xoang xoang nhĩ cũng như rung tâm nhĩ), các ngoại tâm thu ít gặp hơn hoặc biến mất , Trong một số trường hợp, rung nhĩ chuyển thành nhịp xoang.
Ở những bệnh nhân có nhiểm độc giáp ngoại sinh, việc dùng một thuốc chẹn betalàm giảm nhịp tim và giảm khối lượng thất trái (Fazio et al, 1995). Thuốc ức chế beta-làm giảm nguy cơ tim mạch và do đó có thể được xem xét đối với những bệnh nhân điều trị ức chế TSH lâu dài, đặc biệt là những bệnh nhân ung thư tuyến giáp nguy cơ cao, cần phải giảm TSH tích cực (Biondi và Cooper , 2008).
Glycosides trợ tim thường không được chỉ định trong nhiểm độc giáp ngay cả ở những bệnh nhân bị suy tim nặng. Thuốcglycosis làm tăng co bóp tâm thu, kéo dài tâm trương, kích thích thần kinh phế vị làm chậm tính dẫn truyền, đặc biệt là dẫn truyền nhĩ thất. Nhiễm độc tuyến giáp được đặc trưng bởi tăng động, trì hoãn dẫn truyền nhĩ thất, và sử dụng glycosid trợ tim thậm chí còn nguy hiểm vì nhiễm độc digitalis dễ dàng phát triển. Các bệnh nhân nhiểm độc giápthường có khả năng kháng các thuốc chống loạn nhịp, và amiodarone (chứa một phần ba iodine) có thể gây ra chứng nhiểm độc giáp kháng trị liệu nghiêm trọng, bao gồm cơn bão giáp.
Hiệu quả của điều trị RN phụ thuộc vào nhiều yếu tố. Người dưới 50 tuổi, thiếu các triệu chứng suy tim hoặc các bệnh lý tim mạch khác đi kèm, thời gian bệnh ngắn (<4 tháng) và RNkịch phát, huyết áp tâm thu bình thường và suy giáp nhanh do thuốc kháng giáp là những yếu tố tiên đoán chính phục hồi nhịp xoang Trong khoảng một phần ba bệnh nhân. Chuyển tự nhiên sang xoang nhịp điệu xảy ra ở trạng thái bình giáp kéo dài 3 tháng. Nếu không thì nên áp dụng phương pháp quản lý chuẩn về rung tâm nhĩ. Mối quan hệ gián tiếp giữa xác suất chuyển nhịpthành công và thời gian rung tâm nhĩ từ bất kỳ nguyên nhân nào cần được xem xét trước khi làm thủ thuật (cả dược học hoặc điện học).
Bệnh nhân BCTNĐG có rung nhĩ cần dựa vào thang điểm CHA2DS2-VASc ≥ 2 ( nam ) và ≥ 3 nhằm khuyến cáo sử dụng thuốc chống động dự phòng đột quỵ.
Do cường giáp có liên quan đến việc tăng độ nhạy với thuốc chống đông đường uống. Cơ chế có thể là thyroxine làm tăng ái lực của warfarin đối với các vị trí thụ thể trong gan, dẫn đến giảm sản xuất các yếu tố đông máu. Một cơ chế khác có thể là tăng quá trình dị hóa các yếu tố đông máu phụ thuộc vitamin K.
Aspirin nguy cơ gia tăng hormon giáp dạng tự do vì thế các thuốc chống đông thế hệ mới như Apixaban, Dabigatran, Edoxaban và Rivaroxaban cần xem xét sử dụng ở bệnh nhân BCTNĐG rung nhĩ có nguy cơ cao đột quỵ
KẾT LUẬN
PĐTT được sử dụng để đánh giásự hồi phục ở bệnh nhân BCTNĐG . Trong nghiên cứu cơ bản thyroxine gây ra PĐTT đã được ghi nhận hoàn toàn phục hồi khi đạt được bình giáp. Nixon và cộng sự (1979) và Ching và cộng sự (1996) đã chứng minh giảm CSKCTT sau khi phục hồi chức năng tuyến giáp ở bệnh nhân bị nhiểm độc giáp Tuy nhiên, vẫn chưa chứng minh trong các nghiên cứu kéo dài hơn khi chức năng tuyến giáp đã bình thường hóa bằng liệu pháp kháng giáp thymazol (Merillon et al.1989, Makaruk và cộng sự, 1998). Theo Marcisz et al (2006) chức năng tim mạch và cung lượng tim cũng như huyết áp tâm thu cũng bị rối loạn ngay cả sau khi trạng thái tuyến giáp được phục hồi, so với nhóm chứng khỏe mạnh. Đó có thể là kết quả của hormon giáp gây ra sự biểu hiện gen protein co bóp và β-adrenoreceptors. Thay đổi có thể hồi phục không hoàn toàn và sẽ mất nhiều thời gian hơn.
Các hiệu ứng beta-adrenergic đã được điều tra trong nhiều năm. Một số tác giả đã xác nhận lợi ích ức chế beta trong phòng ngừa PĐTT ở mô hình động vật, trong khi một số khác thì không. Một số nghiên cứu về tác động của hệ thống rennin-angiotensin đối với sự phát triển của PĐTT và vai trò tiềm ẩn của chất ức chế enzym chuyển đổi (ACEi) trong điều trị PĐTT và điều trị nhiễm độc giáp. Tuy nhiên, tất cả các dữ liệu sẵn có được cung cấp bởi các nghiên cứu thực nghiệm. Theo như PĐTT là một chỉ định chung cho ACEi, khi nghiên cứu tác dụng của chúng ở bệnh nhân cóBCTNĐG ghi nhận những thay đổi đảo ngược không hoàn chỉnh, nhưng rõ ràng hơn của PĐTT và sự giãn nở tâm nhĩ trái ở những bệnh nhân điều trị bằng ACEi (Babenko và cộng sự, 2006).Do đó, các nghiên cứu gần đây đã chứng minh PĐTT tái phát không hồi phục và sự dãn nhĩ trái trongRN trong tình trạng nhiểm độc giáp kéo dài và / hoặc ở bệnh nhân cao tuổi. Nguy cơ cao ngay cả sau khi phục hồi tuyến giáp bằng thuốc kháng giáp. Thuốc chẹn beta và ACEi góp phần làm cho sự biến đổi này trở nên tốt hơn, nhưng không hồi phục một cách hoàn toàn. Do đó, phương pháp điều trị không hồi phục (không dùng thuốc) có vẻ có lợi ở những bệnh nhân có nguy cơ cao (nam, nữ trên 44 tuổi, tăng huyết áp tâm thu) về dự phòng BCTNĐG. Sau cùng nhiểm độc giáp là biểu hiện nội khoa rất quan trọng vì BCTNĐG có thể biểu hiện trong lần khám đầu tiên. Những bệnh nhân này nên được xem xét điều trị phương pháp không dùng thuốc ngay sau khi hồi phục tuyến giáp .
TÀI LIỆU THAM KHẢO
- Ademolu AB (2017). Thyrotoxic cardiomyopathy: a study of three cases. Gerontol &
Geriatric stud 1: 1-4 - Armigliato M. et al. (2006). Hyperthyroidism as a cause of pulmonary arterial hypertension:a prospective study. 2006 Oct-Nov;57(5):600-6.
- Babenko A. et al. «Effect of ingibitors converting enzime on echocardiography parametrs at a thyrotoxicosis» poster of 31 annual meting ETA, Italy, Napoly, 2-6.09.
- Babenko A. (2006). «Influence of subclinical thyrotoxicosis of varius genesis on
cardiovascular system». «Scientific notes of S-Petersburg Medical Uneversity named
after Pavlov » 2006, V.13, №4, ち.65-69. - Babenko A. (2008) «Character of geometry at clinical and subclinical thyrotoxicosis»«Vestnik of S-Petersburg Uneversity» s. 11 «Меdicine», Vol. 4, dec. 2008 .40-46.
- Babenko A. et al. (2011). Analisis of contribution of various factors in development and type of remodeling left ventricule at thyreotoxicosis. Bulleten of Almazov Federal Heart,Blood and Endocrinology Centre. – 2011. – N 2 (うたечати)
- Bielecka-Dabrowa A et al. (2009) The mechanisms of atrial fibrillation in hyperthyroidism Review. Thyroid Research 2
- Biondi B. & Cooper D. (2008). The clinical significance of subclinical thyroid dysfunction.Endocr Rev 2008;29:76-131.
- Cappola A. et al. (2006). Thyroid Status, Cardiovascular Risk, and Mortality in Older Adults.JAMA. Vol. 295. 『.1033-1041
- Coban E. et al. (2006) Endothelial dysfunction in subjects with subclinical hyperthyroidism. JEndocrinol Invest 29:197–200
- Goyal S, Goyal V (2016). A study of electrocardiographic changes in thyroid disorders.International Journal of Medical Research and Review, 4: 486-490. [Cr
- Grineva E. (2009) Type 2 deiodinase Thr92Ala polymorphism impact on clinical course andmyocardial remodeling in patients with Graves’ disease. Cell Cycle. 8. Is.16P.2565-2570.
- Homoncik M. et al. (2007) Altered platelet plug formation in hyperthyroidism and hypothyroidism.
- Clin. Endocrinol. Metab. 2007. Vol. 92, № 8. P. 3006–3012.
- Marcisz』. et al. (2006). Left ventricular mass in patients with hyperthyroidism. Med SciMonit. 2006. 12(11) 『.481-486.
- Osuna PM, Udovcic M, Sharma MD (2017) Hyperthyroidism and the Heart. MethodistDebakey Cardiovasc J, 13: 60-63.
- Osman F. et al. (2007) Cardiovascular Manifestations of Hyperthyroidism Before and AfterAntithyroid Therapy. J Am Coll Cardiol, 2007; 49:71-81
- Ross DS, Burch HB, Cooper DS, Greenlee MC, Laurberg P, Maia AL, Rivkees SA, Samuels M, Sosa JA, Stan MN, Walter MA (2016) 2016 American Thyroid Association guidelines for diagnosis and management of hyperthyroidism and other causes of
Thyroid 26: 1343-1421. - Sgarbi J et al (2010) Subclinical thyroid dysfunctions are independent risk factors for mortality in a 7.5-year follow-up: the Japanese-Brazilian thyroid study.Eur J Endocrinol 2010;162:569-77.
- Soh M & Croxson M. (2008) Fatal thyrotoxic cardiomyopathy in a young man. 2008; 337: a531.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam