LIÊN QUAN GIỮA NỒNG ĐỘ MYEOPEROXIDASE (MPO) HUYẾT TƯƠNG VÀ XƠ VỮA ĐỘNG MẠCH CẢNH Ở BỆNH NHÂN ĐÁI THÁO ĐƯỜNG TYPE 2
TS. Châu Mỹ Chi*, PGS.TS Đào Thị Dừa, GS.TS Nguyễn Hải Thủy
*Bệnh viện Đa Khoa Tiền Giang – Trường Đại Học Y Dược Huế
ABSTRACT
Research of the correlation between the plasma myeloperoxidase (MPO) levels and carotid atherosclerosis in type 2 diabetic patients
OBJECTIVES of this study was to investigate the correlation between the plasma MPO level with carotid atheroserosis in the type 2 diabetic patients. METHODS: A cross- sectional study of 81 type 2 diabetic patients and 67 healthy subjects. The MPO concentrations were measured in EDTA plasma samples. The carotid artery intima-media thickness (IMT) was measured by ultrasound. RESULTS: Mean plasma MPO level in type 2 diabetic patients was higher than that of the control group (537,05±366,43 pmol/l vs 95,50±50,29 pmol/l, p <0,001). Mean IMT of patients with type 2 diabetes mellitus was 1,20±0,35mm. Prevalence of increased carotid IMT and atherosclerotic plaque in patients type 2 diabetes were 83,95% and 66,67%. The MPO concentration was correlated positively with carotid artery IMT (r=0,348; p<0,01). CONCLUSIONS: The type 2 diabetic patients have substantially elevated plasma levels of myeloperoxidase as well as atherosclerosis-related structural and functional changes of the arterial wall.
Chịu trách nhiệm chính: Châu Mỹ Chi
Ngày nhận bài: 10.6.2016
Ngày phản biện khoa học: 25.6.2016
Ngày duyệt bài: 1.7.2016
1. ĐẶT VẤN ĐỀ
Xơ vữa động mạch ở bệnh nhân đái tháo đường týp 2 xảy ra sớm hơn, nặng hơn, lan rộng hơn so với người không bị bệnh đái tháo đường và ảnh hưởng không những đến các động mạch gần mà còn ở vị trí xa gốc. Các biến chứng mạch máu lớn làm tăng nguy cơ tai biến mạch máu não cao gấp 2 – 4 lần ở người đái tháo đường so với người không bị đái tháo đường. Biến cố mạch vành là nguyên nhân hàng đầu gây tử vong trên bệnh nhân đái tháo đường (hơn 65%) và tổn thương động mạch hai chi dưới đã và đang trở thành nguyên nhân chính gây cắt cụt chi ở bệnh nhân đái tháo đường. Bên cạnh các yếu tố nguy cơ truyền thống gây xơ vữa động mạch như béo phì, tăng huyết áp, tăng đường máu mạn tính, rối loạn lipid… đã gây những bất thường ở thành mạch, rối loạn chức năng nội mạc mạch máu, tăng ngưng tập tiểu cầu và tăng đông máu dẫn đến nguy cơ tổn thương mạch máu lớn. Gần đây vai trò của các yếu tố nguy cơ không truyền thống như gia tăng nồng độ chất ức chế hoạt hóa plasminogen-1 (Plasminogen Activator Inhibitor-1; PAI-1), protein phản ứng loại C (C-reactive protein; CRP), microalbumin niệu… và nhất là myeloperoxidase (MPO) enzyme huyết tương từ các bạch cầu phóng thích được nghiên cứu ghi nhận có liên quan đến xơ vữa động mạch ở những đối tượng có nguy cơ cao trong đó có bệnh đái tháo đường.
Mục tiêu đề tài : Đánh giá mối liên quan giữa nồng độ enzyme myeloperoxidase huyết tương với bề dày lớp nội trung mạc động mạch cảnh ở bệnh nhân đái tháo đường týp 2.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
Tiêu chuẩn chẩn đoán của ADA năm 2012
Chẩn đoán ĐTĐ týp 2 dựa theo tiêu chuẩn Liên đoàn ĐTĐ thế giới và Tổ chức Y tế Thế giới 2005.
Phương pháp nghiên cứu là quan sát mô tả, cắt ngang và bệnh chứng.
Các biến số nghiên cứu
Tất cả đối tượng nghiên cứu được nghiên cứu các tham số bao gồm:
Định lượng nồng độ enzyme myeloperoxidase
ARCHITECT MPO là một xét nghiệm theo kỹ thuật hóa phát quang vi hạt, định lượng nồng độ MPO trong huyết tương người với chất chống đông EDTA trên hệ thống máy xét nghiệm miễn dịch tự động ARCHITECT được thực hiện tại khoa sinh hóa BV TW Huế. Phương pháp: CMIA, Sandwich. Đơn vị biểu thị: pmol/l
Đo bề dày lớp trung nội mạc động mạch cảnh (IMT)
Đo IMT dựa theo hướng dẫn của
ASE 2008.
– Đánh giá IMT động mạch cảnh chung theo hướng dẫn của Hội THA Châu Âu/ Hội TM Châu Âu năm 2007
+ IMT <0,9 mm: Bình thường.
+ IMT ≥0,9 mm-1,49 mm: Dày lớp nội trung mạc.
+ IMT ≥1,5mm: Mảng xơ vữa.
PHƯƠNG PHÁP XỬ LÝ SỐ LIỆU
– Xử lý số liệu bằng phần mềm
SPSS 16.0.
3. KẾT QUẢ NGHIÊN CỨU
81 bệnh nhân ĐTĐ týp 2 và 67 người chứng, chúng tôi có các kết quả sau:
Bảng 1. Đặc điểm tuổi của đối tượng nghiên cứu 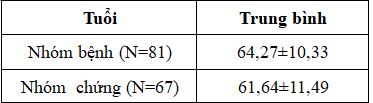
Bảng 2. Nồng độ MPO của nhóm đái tháo đường
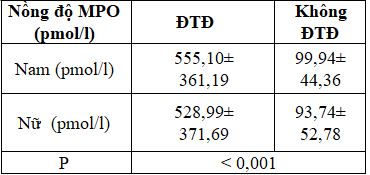
Có khác biệt nồng độ MPO giữa nam và nữ của nhóm có và không ĐTĐ ( p<0,001).
Bảng 3. Đặc điểm về bề dày động mạch cảnh (IMT)
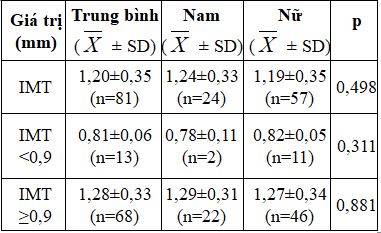
IMT trung bình 1,20±0,35mm. Không có sự khác biệt về IMT ở nam và nữ, với p>0,05.
Bảng 4. Tỉ lệ dày lớp nội trung mạc động mạch cảnh
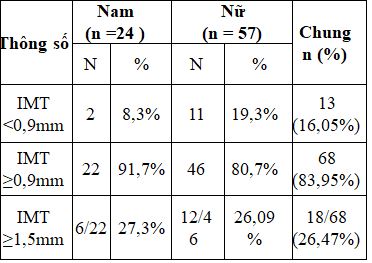
Tỉ lệ bệnh nhân có IMT ≥0,9mm chiếm 83,95%. Trong đó số bệnh nhân có IMT≥1,5mm chiếm 26,47%, (nam 27,3%) và nữ (26,09%).
Bảng 5. Tỉ lệ mảng bám động mạch cảnh ở nhóm ĐTĐ
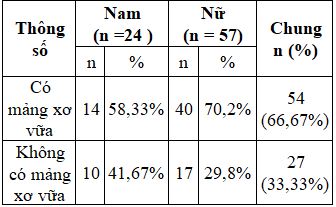
Tỉ lệ bệnh nhân đái tháo đường týp 2 có mảng xơ vữa bám ở động mạch cảnh chiếm 66,67%.
Bảng 6. So sánh nồng độ MPO với IMT
<0,9 và IMT ≥ 0,9mm
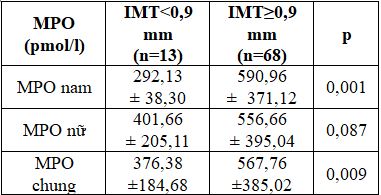
Có sự khác biệt về nồng độ MPO huyết tương giữa 2 nhóm IMT < 0,9 mm và IMT ≥ 0,9 mm (p = 0,009). Sự khác biệt cả hai giới, trong đó sự khác biệt rõ ở nam nhiều hơn nữ.
Bảng 7. Liên quan giữa MPO với IMT < 1,5 và IMT ≥ 1,5mm
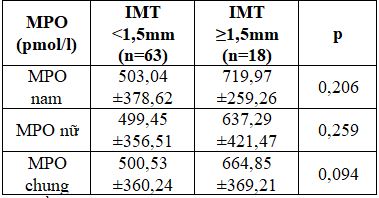
Nồng độ MPO ở nhóm có IMT <1,5mm thấp hơn nhóm có IMT≥1,5mm. Tuy nhiên, không có sự khác biệt đáng kể về nồng độ MPO huyết tương giữa 2 nhóm IMT < 1,5 mm và IMT ≥ 1,5 mm (p =0,094).
Bảng 8. Liên quan giữa MPO với mảng xơ vữa
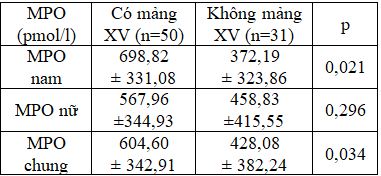
Có sự khác biệt nồng độ MPO ở nhóm có và không có mảng xơ vữa (p <0,05). Sự khác biệt có ý nghĩa ở nam (p<0,05). Không có sự khác biệt đối với nữ (p>0,05).
Bảng 9. Tương quan giữa MPO với một số yếu tố nguy cơ
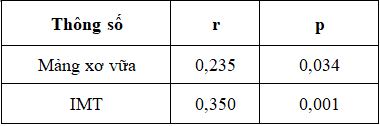
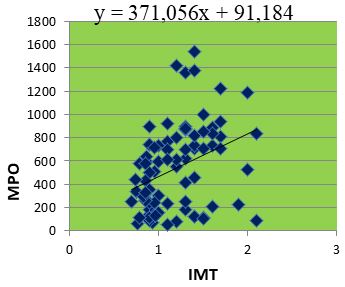
Đồ thị 1. Tương quan giữa MPO và IMT
Có mối tương quan thuận giữa MPO và IMT ở bệnh nhân ĐTĐ týp 2 ( r = 0,350; p = 0,001).
Phương trình hồi quy tuyến tính
y = 371,056x+91,184.
Bảng 10. Tương quan hồi quy đa biến giữa MPO với các yếu tố nguy cơ
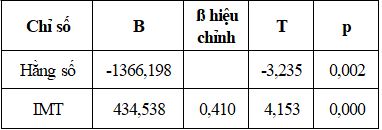
R= 0,54 ; R2 điều chỉnh = 0,255
Phương trình hồi quy đa biến:
y=1,174 QTc+ 434,538 IMT-1366,198
Bảng 11. Diện tích dưới đường cong ROC giữa IMT với MPO
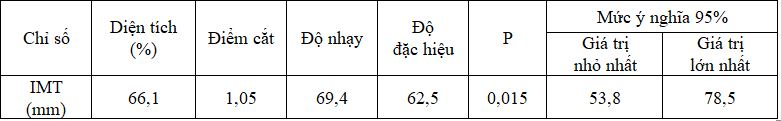
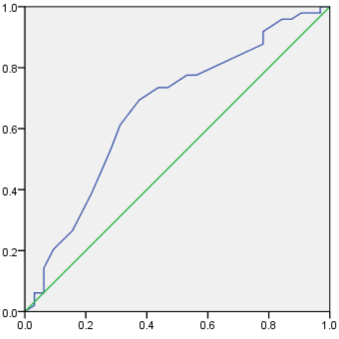
Đồ thị 2. Đường cong ROC giữa MPO với IMT
Khi ở điểm cắt IMT >1,05 mm thì sẽ có nguy cơ tăng MPO với diện tích dưới đường cong là 66,1%, mức ý nghĩa (khoảng tin cậy) 95%: 53,8%-78,5%, độ nhạy 69,4 %, độ đặc hiệu
62,5 %.
4. BÀN LUẬN
4.1. So sánh nồng độ MPO nhóm đái tháo đường và nhóm chứng
Nồng độ trung bình của MPO ở nhóm ĐTĐ là 537,04±366,42 pmol/l, nồng độ MPO ở nam là 555,10±361,19 pmol/l và ở nữ là 528,99±371,69 pmol/l, không có sự khác biệt về nồng độ MPO giữa nam và nữ ở bệnh nhân ĐTĐ týp 2, với p>0,05.
So sánh về nồng độ giữa hai nhóm có bệnh ĐTĐ và không ĐTĐ đã cho thấy có sự khác biệt có ý nghĩa giữa hai nhóm (537,04 ± 366,42 pmol/l so với 95,50 ± 50,29 pmol/l, với p=0,000).
Nồng độ MPO huyết tương ở nam ĐTĐ cao hơn nam chứng (555,10 ± 361,19 pmol/l so với 99,94± 44,36 pmol/l, p <0,001) và MPO ở nữ ĐTĐ cao hơn nữ chứng (528,99±371,69 pmol/l so với 93,74±52,78 pmol/l, p <0,001).
Số bệnh nhân có giá trị nồng độ MPO cao hơn giá trị trung bình của nhóm chứng 145,79 pmol/l (tính từ kết quả X+SD của nhóm chứng) có 64 trường hợp, chiếm tỉ lệ 77,33%. Nguy cơ tăng MPO≥145,79pmol/l (OR) của nhóm bệnh ĐTĐ là 24,26, khoảng tin cậy 95% là 9,34-65,54, p<0,05.
4.2. Bề dày lớp nội trung mạc (IMT) động mạch cảnh
Trong nghiên cứu của chúng tôi IMT trung bình của động mạch cảnh ở bệnh nhân ĐTĐ týp 2 là 1,20 ± 0,35 mm; IMT ở nam là 1,24 ± 0,33 mm; IMT ở nữ là 1,19 ± 0,35mm. Không có sự khác biệt về giá trị IMT trung bình ở nam và nữ.
Khi khảo sát IMT ≥0,9mm cho thấy có 68/81 bệnh nhân có chiếm tỉ lệ 83,95%, nam có 22/24 trường hợp (chiếm 91,67%), nữ có 46/57 trường hợp (chiếm 80,7%).
Với IMT≥1,5mm, có 18/81 bệnh nhân chiếm tỉ lệ 22,22%, nam có 12/24 trường hợp, nữ 6/57 trường hợp.
Bệnh nhân có ít nhất một mảng xơ vữa bám ở 1 hoặc 2 bên động mạch cảnh chiếm tỉ lệ 66,67%, nam có mảng xơ vữa bám chiếm 58,33% và nữ có mảng xơ vữa bám chiếm 70,2%.
Các nghiên cứu trong nước cho thấy IMT động mạch cảnh ở bệnh nhân ĐTĐ týp 2 cao hơn so với nhóm chứng như nghiên cứu của Võ Bảo Dũng (2010-2012) gồm 102 bệnh nhân ĐTĐ týp 2 mới phát hiện với 96 người chứng thì IMT trung bình của nhóm bệnh là 0,79±0,19mm còn ở nhóm chứng là 0,73± 0,11 mm, với p<0,05, của tác giả Trần Quý Hợi và Nguyễn Hải Thủy cũng ghi nhận IMT bệnh nhân ĐTĐ týp 2 cao hơn so với nhóm chứng.
Nhóm tác giả Ngô Đình Châu, Trần Hữu Dàng, Trần Trung Thông ghi nhận bệnh nhân có hội chứng chuyển hóa nếu có 5 thành tố (vòng bụng, huyết áp, triglycerid, HDL-C và đường huyết cao) thì IMT động mạch cảnh trung bình là 1,09±0,37mm.
So sánh IMT trung bình của nghiên cứu chúng tôi với của các tác giả như Võ Bảo Dũng (0,79 ± 0,19mm), của Trần Thanh Linh (1,35 ± 0,40mm) cho thấy kết quả IMT trung bình trong nghiên cứu của chúng tôi có cao hơn của tác giả Võ Bảo Dũng khác có lẽ do cách chọn bệnh khác nhau.
Ở nghiên cứu tác giả Võ Bảo Dũng trên đối tượng ĐTĐ týp 2 mới mắc, còn của chúng tôi cũng tương tự như của tác giả Trần Thanh Linh, tác giả Trần Thanh Linh ghi nhận tỉ lệ dày IMT ở nhóm bệnh nhân ĐTĐ là 81,4% và mảng xơ vữa động mạch là 61,8% , kết quả nghiên cứu của chúng tôi cũng tương tự.
Nhiều chứng cứ nghiên cứu của tác giả ở nước ngoài cũng cho thấy IMT ở bệnh nhân ĐTĐ cao hơn nhóm chứng.Bonora E và cộng sự nghiên cứu 58 bệnh nhân ĐTĐ và 56 bệnh nhân không ĐTĐ ghi nhận bệnh nhân ĐTĐ có IMT động mạch cảnh dày hơn có ý nghĩa so với không ĐTĐ.
Trong một phân tích gộp của G. Brohall cho thấy bệnh nhân ĐTĐ có IMT lớn hơn nhóm chứng, bệnh nhân rối loạn dung nạp glucose có IMT động mạch cảnh cao hơn nhóm chứng. Bệnh nhân ĐTĐ hơn 10 năm thì nguy cơ liên quan với nhồi máu cơ tim và đột quỵ gia tăng hầu hết 40% .
IMT động mạch cảnh trung bình của nghiên cứu chúng tôi cũng tương tự một nghiên cứu gần đây của Yoko Irie (2013) ở 333 bệnh nhân ĐTĐ týp 2 là 1,05 ± 0,42mm, của tác giả Y. Hayashi (2007) ở 172 bệnh nhân ĐTĐ týp 2 là 1,1± 0,4mm, của tác giả Moatassem S Amer (2014) ở 58 bệnh nhân ĐTĐ týp 2 là 1,14 ± 0,2mm và cao hơn so với 59 người chứng (0,69 ± 0,2) với p<0,001.
4.3. Liên quan giữa MPO với IMT động mạch cảnh
Có sự khác biệt đáng kể về nồng độ MPO huyết tương giữa 2 nhóm IMT <0,9 mm và IMT ≥ 0,9 mm (376,38 ± 184,68 pmol/l so với 567,76 ± 385,02 pmol/l, p = 0,009). Sự khác biệt ở cả 2 giới, trong đó sự khác biệt rõ ở nam (292,13±38,30 pmol/l so với 590,96±371,12 pmol/l, p=0,001) hơn ở nữ (401,66±205,11 pmol/l so với 556,66±395,04 pmol/l, p=0,087).
Xét về nồng độ MPO ở 2 nhóm IMT dưới 1,5mm và IMT từ 1,5mm trở lên qua nghiên cứu chúng tôi ghi nhận nồng độ MPO ở nhóm IMT≥ 1,5mm có cao hơn nhóm IMT<1,5mm. Tuy nhiên không thấy có sự khác biệt đáng kể về nồng độ MPO huyết tương giữa 2 nhóm IMT < 1,5 mm và IMT ≥ 1,5 mm (500,53 ± 360,24 pmol/l so với 664,85 ± 369,21pmol/l, p =0,094).
Chúng tôi cũng ghi nhận nồng độ MPO cao hơn đáng kể ở nhóm có mảng xơ vữa (604,60±342,91pmol/l) so với không có mảng xơ vữa (428,08±382,24pmol/l), với p=0,034. Sự khác biệt có ý nghĩa ở nam (p=0,021) và không có khác biệt ở nữ giới (p>0,05).
Heilman K và cộng sự (2009) nghiên cứu 30 bệnh nhân ĐTĐ có thời gian mắc bệnh trung bình là 5,4 ± 3,4 năm và so sánh với 30 người khỏe mạnh để xem những thay đổi về chức năng, cấu trúc của động mạch với một dấu chỉ điểm sinh hóa mới của xơ vữa động mạch là MPO.
Các đối tượng tham gia nghiên cứu được làm xét nghiệm MPO và siêu âm đo IMT động mạch cảnh. Kết quả nghiên cứu ghi nhận nhóm bệnh nhân ĐTĐ có nồng độ MPO tăng và IMT tăng so hơn với nhóm chứng với p lần lượt là p=0,006 và p=0,005 [11].
Rudolph và cộng sự (2013) cho thấy có mối liên quan chặt chẽ giữa lắng đọng MPO ở mạch máu với mảng xơ vữa. Raphaël Duivenvoorden và cộng sự (2013) cũng cho thấy có mối liên quan giữa nồng độ MPO và mảng xơ vữa động mạch cảnh viêm sau 3 tháng theo dõi bằng chụp PET/CT ở 130 bệnh nhân (r=0,25; p=0,02) .
Yu Kataoka và cộng sự (2014) nhận xét rằng gia tăng mức MPO liên quan tiến triển xơ vữa mạch ở bệnh nhân ĐTĐ khi nghiên cứu 881 bệnh nhân có bệnh lý mạch vành được kiểm chứng qua chụp động mạch vành gồm 199 bệnh nhân ĐTĐ và 682 bệnh nhân không ĐTĐ có nồng độ MPO ở 2 nhóm tương tự nhau ở đầu vào sau đó theo dõi đánh giá mức độ nặng lên của xơ vữa mạch qua siêu âm nội mạch.
Kết quả nghiên cứu ghi nhận có mối liên quan giữa tăng nồng độ MPO với tiến triển xơ vữa mạch ở bệnh nhân ĐTĐ. Điều này cho thấy tầm quan trọng của MPO trong bệnh tim mạch ĐTĐ. Như vậy, nghiên cứu của chúng tôi cũng phù hợp với các nghiên cứu cho thấy nồng độ MPO có liên quan đến xơ vữa mạch ở bệnh nhân ĐTĐ. Nghiên cứu của chúng tôi phù hợp với nghiên cứu của tác giả Purushothamn và cũng phù hợp với nghiên cứu của A. Krasniak và cộng sự cho thấy có mối liên quan giữa nồng độ MPO và mảng xơ vữa với p<0,05.
4.4. Tương quan giữa MPO với IMT
Nghiên cứu của chúng tôi ghi nhận có mối tương quan thuận giữa MPO với IMT, với r=0,350; p=0,001; Phương trình hồi quy tuyến tính đơn biến: y=371,056x+91,184. Khi ở điểm cắt IMT >1,05 mm thì sẽ có nguy cơ tăng MPO với diện tích dưới đường cong là 66,1%, mức ý nghĩa (khoảng tin cậy) 95%: 53,8%-78,5%, độ nhạy 69,4 %, độ đặc hiệu 62,5 %.
Fu Li Juan (2007) nghiên cứu 120 bệnh nhân HCCH ghi nhận tăng cả MPO huyết tương và IMT; MPO tương quan với IMT
(r = 0,0213; p < 0,05). Kết quả tương tự từ nghiên cứu của tác giả Li Tao (2008) ở 90 bệnh nhân có hội chứng chuyển hóa, MPO có mối tương quan với IMT, hệ số tương quan
(r = 0,241; p = 0,022).
Nghiên cứu của Krasniak và cộng sự (2007) ở 73 bệnh nhân suy thận mạn ghi nhận nồng độ MPO tương quan với mảng xơ vữa động mạch cảnh, hệ số tương quan r=0,24, với p<0,05 trong phân tích đơn biến; Markus Exner (2006) cũng cho thấy MPO tương quan với tiến trình hẹp động mạch cảnh với r=0,083 và p=0,008 .
KẾT LUẬN
Qua nghiên cứu mối liên quan giữa nồng độ enzyme MPO với các yếu tố nguy cơ tim mạch khác ở 81 bệnh nhân ĐTĐ týp 2 và 67 người chứng, chúng tôi có các kết luận sau
Nồng độ enzyme MPO ở bệnh nhân ĐTĐ cao hơn so với nhóm chứng (537,04±366,42pmol/l so với 95,50±50,29pmol/l; p<0,001). IMTtrungbìnhở bệnh nhânđáitháođường là1,20±0,35mm. Tỉ lệ IMT dày chiếm 83,95%vàmảngxơvữađộngmạch cảnh chiếm 66,67%.Ở bệnh nhân ĐTĐ týp 2, nồng độ MPO liên quan với IMT động mạch cảnh (p<0,05), Điểm cắt IMT >1,05 mm thì sẽ có nguy cơ tăng MPO với diện tích dưới đường cong là 66,1%, mức ý nghĩa (khoảng tin cậy) 95%: 53,8%-78,5%, độ nhạy 69,4 %, độ đặc hiệu 62,5 %. Trong phân tích hồi quy đa biến thì IMT và QTc là 2 yếu tố ảnh hưởng đến MPO.
TÓM TẮT
Mục tiêu: Đánh giá mối liên quan giữa nồng độ enzyme myeloperoxidase huyết tương với bề dày lớp nội trung mạc động mạch cảnh ở bệnh nhân đái tháo đường týp 2.Đối tượng và phương pháp. 81 bệnh nhân ĐTĐ týp 2 và 67 người chứng.
Kết quả: Nồng độ enzyme MPO ở bệnh nhân ĐTĐ cao hơn so với nhóm chứng (537,04±366,42pmol/l so với 95,50±50,29pmol/l; p<0,001). IMTtrungbìnhở bệnh nhânđáitháođường là1,20±0,35mm. Tỉ lệ IMT dày chiếm 83,95%vàmảngxơvữađộngmạch cảnh chiếm 66,67%.Ở bệnh nhân ĐTĐ týp 2, nồng độ MPO liên quan với IMT động mạch cảnh (p<0,05),Điểm cắt IMT >1,05 mm thì sẽ có nguy cơ tăng MPO với diện tích dưới đường cong là 66,1%, mức ý nghĩa (khoảng tin cậy) 95%: 53,8%-78,5%, độ nhạy 69,4 %, độ đặc hiệu 62,5 %. Trong phân tích hồi quy đa biến thì IMT và QTc là 2 yếu tố ảnh hưởng đến MPO.
Kết luận Nồng độ MPO liên quan đến xơ vữa động mạch cảnh ở bệnh nhân ĐTĐ týp 2.
TÀI LIỆU THAM KHẢO
- Nguyễn Hải Thủy (2009), “Bệnh tim mạch trong đái tháo đường”, Nhà xuất bản Đại học Huế, tr. 137-139.
- Galijašević S.(2013), “Myeloperoxidase Interactions with Nitric Oxide: A Review of Mechanistic Pathways”, Bulletin of the Chemists and Technologists of Bosnia and Herzegovina, 40, pp.1-8.
- Gorudko I.V, Kostevich V.A, Sokolov A.V, Buko I.V, Konstantinova E.E, et al (2011), “Increased Myeloperoxidase activity is a risk factor for ischemic heart disease in patients with diabetes mellitus”, Biomedical Chemistry, 5 (3),
pp. 307–312. - Hazen S.L (2004), “Myeloperoxidase and plaque vulnerability”, Arterioscler Thromb Vasc Biol, 24, pp. 1143-1146.
- Heilman K, Zilmer M, Zilmer K, Lintrop M, Kampus P, et al (2009), “Arterial stiffness, carotid artery intima-media thickness and plasma myeloperoxidase level in children with type 1 diabetes”, Diabetes Res Clin Pract, 84(2), pp.168-173.
- Jornayvaz F.R, Brulhart-Meynet M.C, James R.W (2009), “Myeloperoxidase and paraoxonase-1 in type 2 diabetic patients”, Nutrition, Metabolism & Cardiovascular Diseases, 19, pp.
613-619. - Khalil N.M, Pepato M.T, Brunetti I.L (2008), “Free radical scavenging profile and myeloperoxidase inhibition of extracts from antidiabetic plants: Bauhinia forficata and Cissus sicyoides”, Biol Res, 41, pp.165-171.
- Klebanoff SJ (2005), “Myeloperoxidase: friend and foe”, J Leukoc Biol, 77, pp. 598-625.. Mäkelä R (2009), “Role of -463-G/A promoter polymorphiism of myeloperoxidase in the development of atherosclerosis”, Tampere, pp. 40-52.
- Nicholls S.J, Hazen S.L (2005), “Myeloperoxidase and cardiovascular disease”, Arterioscler Thromb Vasc Biol, 25, pp.1102-1111.
- Paramesh S, Mahesh B, Suchetha K, Vijay Rd, Pushpalathad KC (2011), “A study on lipid profile and myeloperoxidase level in Type II diabetes mellitus with respect to age and gender”, Research Journal of Pharmaceutical, Biological and Chemical Sciences, 2 (1), pp.335.
- Rensen SS, Slaats Y, Nijhuis J, Jans A, Bieghs V, et al (2009), “Increased hepatic myeloperoxidase activity in obese subjects with nonalcoholic steatohepatitis”,Am J Pathol., 175, pp.1473-1482.
- Roman R. M, Wendland A.E, Polanczyk C.A (2007), “Myeloperoxidase and coronary arterial disease: From research to clinical practice”, Arq Bras Cardiol, 91(1), pp.11-18.
- Van der Zwan L.P, Scheffer P.G, Dekker J.M, et al (2010), “Hyperglycemia and oxidative stress strengthen the association between Myeloperoxidase and blood pressure”, Hypertension, 55, pp.1366-1372.
- Wang A.Y-M, Lam C. W-K, Chan I. H-S, Wang M, Lui S-F, Sanderson J.E (2010), “Prognostic Value of Plasma Myeloperoxidase in ESRD Patients”, American Journal of Kidney Diseases, 56 (5), pp. 937-946.
- Onut R, Balanescu AP, Constantinescu D, Calmac L, Marinescu M, Dorobantu PM. Imaging atherosclerosis by carotid intima-media thickness in vivo: how to, where and in whom? Maedica (Buchar) 2012;7(2):153–62.
- Santos IS, Alencar AP, Rundek T, Goulart AC, Barreto SM, Pereira AC, et al. Low impact of traditional risk factors on carotid intima-media thickness: the ELSA-Brasil cohort. Arterioscler Thromb Vasc Biol. 2015; 35(9):2054–9. doi: 10.1161/ATVBAHA.115.305765.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam