CẬP NHẬT CHẨN ĐOÁN HÌNH ẢNH PHÂN LOẠI
BƯỚU NHÂN TUYẾN GIÁP LÀNH TÍNH VÀ ÁC TÍNH
PGS. TS. Nguyễn Duy Huề1, PGS.TS. Bùi Văn Lệnh1,
PGS.TS. Vũ Bích Nga1, ThS.Lê Tuấn Linh1
1Trường đại học Y Hà Nội
ABSTRACT
In the past, as separate determinants on ultrasound used to be for the categorization of thyroid nodules into benign and malignant, the sensitivity and specificity were low with heterogeneous results. However, TIRADS (Thyroid Imaging Reporting and Data System) was applied in the diagnosis of thyroid nodules in 2009 and update in 2011, and then has been modified based on six ultrasonographic features: solitary, hypoechogenicity, marked hypoechogenicity, irregular/ microlobulated margins, microcalcification, taller than wider shape and classified into the following types: TIRADS 0, 1, 2, 3, 4a, 4b, 4c, 5, 6 since 2011. This TIRADS-System can be easily used in routine clinical practice with more agreeable results and high accuracy.
The high field MRI from 1.5 Tesla can not only assess the extent of thyroid nodule spread, the depth of invasion but also calculate the apparent diffusion coefficient (ADC) values on the diffusion-weighted imagings (DWI) which can differentiate benign from malignant thyroid nodules. Although the ADC cut off value hasn’t been agreed among the authors, most of us are in line with the conclusion that the lower ADC value, the more likely to be malignant thyroid nodule.
Chịu trách nhiệm chính: Nguyễn Duy Huề
Ngày nhận bài: 18.9.2016
Ngày phản biện khoa học: 8.10.2016
Ngày duyệt bài: 15.10.2016
TÓM TẮT
Trước đây siêu âm tuyến giáp chỉ dùng các dấu hiệu riêng lẻ để chẩn đoán phân biệt bướu lành và ác tính nên độ nhạy và độ đặc hiệu không cao, không thống nhất giữa các kết quả. Từ 2009 siêu âm tuyến giáp áp dụng TIRADS vào chẩn đoán bướu giáp nhân, 2011 có phân loại TIRADS mới nhất dựa vào 6 dấu hiệu siêu âm: đặc/đặc là chủ yếu, giảm âm, rất giảm âm, bờ không đều/ múi nhỏ, vi vôi hóa, chiều cao > chiều rộng, chia làm các loại: TIRADS 0,1,2,3,4a,4b,4c,5,6. Đây là bảng phân loại TIRADS dễ áp dụng trên lâm sàng, dễ thống nhất các kết quả và có độ chính xác cao.
MRI từ lực cao ≥1.5T ngoài khả năng đánh giá xâm lấn tại chỗ ung thư tuyến giáp còn có chuỗi xung khuếch tán Diffusion có thể đo được cụ thể giá trị ADC, có khả năng tiên lượng tính chất lành tính hay ác tính của khối u tuyến giáp. Các tác giả vẫn chưa thống nhất được chỉ số cut-off của ADC, nhưng nhìn chung đều thống nhất: giá trị ADC càng thấp thì nguy cơ ác tính càng cao.
I. ĐẶT VẤN ĐỀ
Bướu nhân tuyến giáp là bệnh lý nội tiết khá thường gặp, tỷ lệ phát hiện bướu nhân tuyến giáp trên lâm sàng4-7%, tỷ lệ phát hiện trên siêu âm có thể lên tới 19-67% [1]. Tỷ lệ mắc cao nhưng < 10% bướu nhân tuyến giáp là ác tính.
Chẩn đoán phân biệt bướu nhân tuyến giáp lành tính và ác tính dựa vào lâm sàng, xét nghiệm sinh hóa, chẩn đoán hình ảnh (CĐHA) và tế bào học, giải phẫu bệnh, tuy nhiên triệu chứng lâm sàng của bệnh và các xét nghiệm sinh hóa không đặc hiệu. Vai trò của CĐHA đặc biệt là siêu âm và cộng hưởng từ giúp chẩn đoán xác định, chẩn đoán giai đoạn ung thư tuyến giáp, từ đó quyết định chiến lược điều trị.
Trên thực tế bệnh nhân có bướu nhân tuyến giáp nếu siêu âm nghi ngờ ung thư sẽ được chọc hút kim nhỏ làm tế bào học trước mổ và/hoặc được phẫu thuật sinh thiết tức thì. Tùy thuộc vào kết quả tế bào học và sinh thiết tức thì trong mổ mà bệnh nhân được cắt giáp toàn bộ hoặc gần toàn bộ (nếu kết quả tế bào dương tính) hoặc cắt thùy giáp nếu kết quả tế bào là lành tính. Tuy nhiên phương pháp chọc hút kim nhỏ có nhiều âm tính giả và dương tính giả [2], sinh thiết tức thì trong mổ chỉ một số cơ sở mới làm được, vì vậy một số bệnh nhân phải mổ cắt toàn bộ tuyến giáp thì hai hoặc bị cắt toàn bộ tuyến giáp không cần thiết và phải điều trị nội tiết thay thế suốt đời. Do đó cần phải chẩn đoán chính xác bướu nhân tuyến giáp lành tính hay ác tính để có phương pháp xử trí phù hợp.
Vai trò của CĐHA, trong đó đặc biệt là siêu âm và cộng hưởng từ gần đây đã có nhiều tiến bộ, đã giúp cho chẩn đoán phân biệt bướu nhân lành tính và ác tinh ngày càng chính xác hơn. Vì vậy chúng tôi xin điểm qua một số y văn để: cập nhật các tiến bộ mới trong chẩn đoán phân biệt bướu nhân tuyến giáp lành tính và ác tính trên siêu âm và cộng hưởng từ.
II. VAI TRÒ CỦA SIÊU ÂM TRONG CHẨN ĐOÁN PHÂN BIỆT BƯỚU NHÂN TUYẾN GIÁP LÀNH TÍNH VÀ ÁC TÍNH
Đối với mỗi bướu nhân tuyến giáp, siêu âm được dùng để đánh giá đặc điểm: kích thước, độ sinh âm (giảm âm, đồng âm hoặc tăng âm), thành phần cấu tạo (nang, đặc, hoặc hỗn hợp), cũng như có hoặc không có vôi hóa nhỏ hoặc to, bờ đều hay không đều, và dòng chảy mạch máu bên trong [4], [5].
Nhiều nghiên cứu công bố khả năng dự báo bướu tuyến giáp là lành tính hay ác tính trên cơ sở các dấu hiệu siêu âm trong đó kích thước bướu không có ý nghĩa dự báo tính chất ác tính [5].
Các đặc điểm siêu âm hướng đến bướu nhân lành tính: Cấu trúc dạng nang hoặc thành phần nang là chủ yếu. Cấu trúc đặc tăng âm hoặc đồng âm, bờ đều, ranh giới rõ không có vi vôi hóa, tăng sinh mạch kiểu ngoại vi. Cấu trúc dạng hỗn hợp hoặc bọt biển có phần đặc tăng âm hoặc đồng âm [5], [6].
Các đặc điểm siêu âm hướng đến ung thư tuyến giáp: bướu đặc hoặc thành phần đặc chiếm ưu thế, giảm âm hoặc rất giảm âm, bờ không đều hoặc có múi nhỏ, có vi vôi hóa, chiều cao lớn hơn chiều rộng, tăng sinh mạch trong bướu [6], [7]. Tuy nhiên không có đặc điểm siêu âm nào được coi là tiêu chuẩn vàng trong chẩn đoán bướu giáp nhân ác tính, độ nhạy, độ đặc hiệu, giá trị dự báo âm tính và dương tính đối với các tiêu chuẩn đó biến đổi rất nhiều từ nghiên cứu này đến nghiên cứu khác.
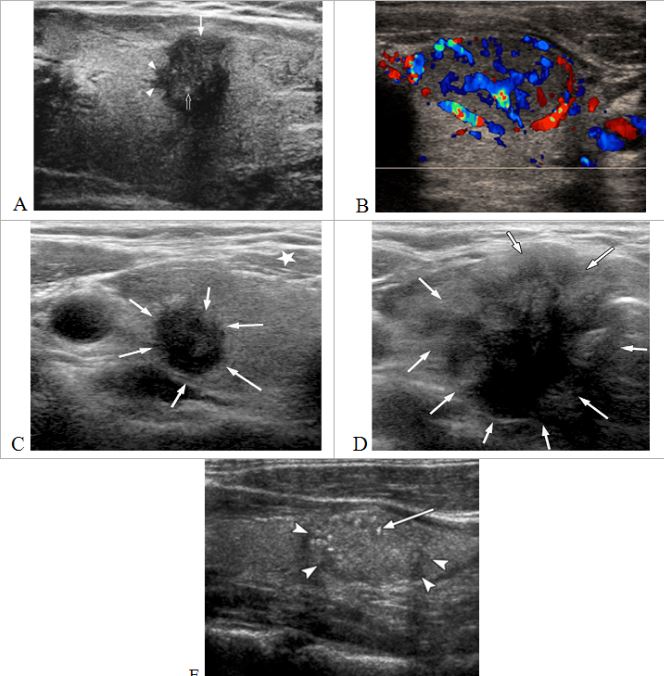
Hình 1. Các dấu hiệu gợi ý tổn thương ác tính của bướu giáp nhân. A. Bướu giảm âm có chiều cao lớn hơn chiều rộng, bờ tua gai; B. Tăng sinh mạch trong bướu; C,D: Bướu rất giảm âm so với cơ trước giáp. E. Bướu có vi vôi hóa.
Bảng 1. Giá trị của các dấu hiệu trên siêu âm chẩn đoán tổn thương ác tính của bướu giáp nhân
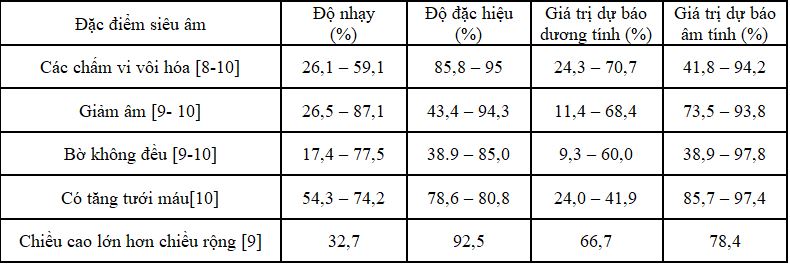
Nhiều công trình nghiên cứu đã cho thấy sự kết hợp các yếu tố nguy cơ trên siêu âm làm tăng khả năng ác tính. Một số nghiên cứu đã đưa ra phân loại nguy cơ ác tính của bướu giáp nhân dựa trên các đặc điểm siêu âm được gọi là bảng phân loại TIRADS (Thyroid Imaging Reporting and Data System). Horvath (2009) là người đầu tiên đưa ra khái niệm TIRADS, tác giả phân loại tổn thương tuyến giáp thành 10 nhóm và xếp loại TIRADS từ 1 đến 6, phân tầng nguy cơ ác tính của các nhóm TIRADS dựa theo BIRADS. Tuy nhiên cách phân loại của tác giả rất khó áp dụng trên lâm sàng [15].
Jin Young Kwak và cs (2011) cho thấy các đặc điểm siêu âm liên quan nhiều đến ác tính gồm: Cấu trúc dạng đặc hoặc thành phần đặc là chủ yếu, giảm âm, rất giảm âm, bờ không đều hoặc có múi nhỏ, có vi vôi hóa, chiều cao lớn hơn chiều rộng. Tác giả đưa ra bảng phân loại TIRADS dựa vào 6 đặc điểm siêu âm này, xếp loại TIRADS từ 1 đến 6, phân tầng nguy cơ ác tính dựa theo BIRADS:
– TIRADS 1: Mô giáp lành
– TIRADS 2: Tổn thương lành tính (0% ác tính)
– TIRADS 3: Tổn thương nhiều khả năng lành tính (< 5% nguy cơ ác tính)
– TIRADS 4: Tổn thương có nguy cơ ác tính gồm:
+ TIRADS 4a: Có một đặc điểm nghi ngờ (5 – 10% nguy cơ ác tính).
+ TIRADS 4b: Có 2 đặc điểm nghi nghờ (10 – 50% nguy cơ ác tính).
+ TIRADS 4c: Có 3-4 đặc điểm nghi nghờ (50 – 95% nguy cơ ác tính).
– TIRADS 5: Có > 4 đặc điểm nghi ngờ (> 95% nguy cơ ác tính).
– TIRADS 6: Biết chắc tổn thương ác tính trước đó.
Đây là phân loại khá đơn giản, dễ áp dụng trên lâm sàng, có thể áp dụng được ở Việt Nam[7].
III. VAI TRÒ CỦA MRI TRONG CHẨN ĐOÁN PHÂN BIỆT BƯỚU NHÂN TUYẾN GIÁP LÀNH TÍNH VÀ ÁC TÍNH
Trước đây theo các nghiên cứu nước ngoài, đa số tác giả đều nhận định cộng hưởng từ ít khi được chỉ định trong chẩn đoán xác định ung thư tuyến giáp mà thường được chỉ định với mục đích đánh giá giai đoạn xâm lấn tại chỗ của u và di căn hạch vùng cổ hoặc di căn xa. Hiện nay các máy cộng hưởng từ có từ lực cao ≥1.5T có độ phân giải cao với nhiều chuỗi xung: T2W xóa mỡ, T1W xóa mỡ, Diffusion đo được giá trị ADC… có khả chẩn đoán chính xác vị trí, kích thước, số lượng bướu nhân, nhất là đánh giá xâm lấn tại chỗ của UTTG như: u trong tuyến hay xâm lấn ra ngoài bao giáp, khối u xâm lấn các cấu trúc lân cận (động mạch cảnh chung, tĩnh mạch cảnh trong, khí quản, thực quản, trung thất trên) và đánh giá di căn hạch vùng cổ, phân biệt bướu nhân lành tính và ác tính, từ đó quyết định chiến lược điều trị.
Về xâm lấn tại chỗ, theo tổng kết của Ann D.King – 2008, cộng hưởng từ có độ đặc hiệu tới 100% trong xác định xâm lấn thành và lòng của thực quản, khí quản, nếu lấy dấu hiệu u xâm lấn làm mất lớp mỡ rãnh khí quản-thực quản để xác định có xâm lấn thần kinh quặt ngược thì độ nhạy và độ đặc hiệu cũng đều khá cao, lần lượt là 94% và 82% [16]. Theo Ji Chen Wang cộng hưởng từ có độ chính xác 90% trong đánh giá xâm lấn khí quản [17].
Theo Yousem M.D – 1995, cộng hưởng từ cũng xác định chính xác mức độ xâm lấn vào động mạch cảnh chung và các mạch trung thất: nếu u bao quanh quá 2700 chu vi động mạch thì không còn khả năng có thể bóc tách được khối u [18].
A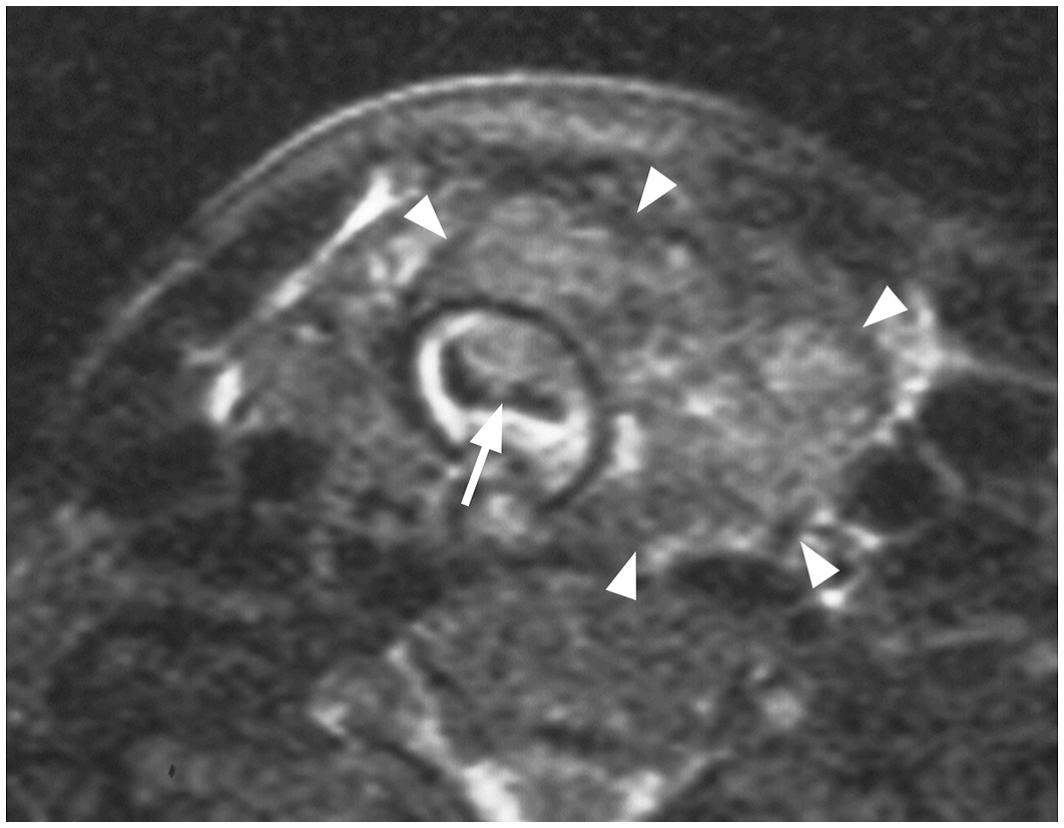
Hình2: Hình ảnh UTTG thể nhú trên chuỗi xung T2W xóa mỡ: u(đầu mũi tên) xâm lấn vào trong lòng khí quản (mũi tên).
B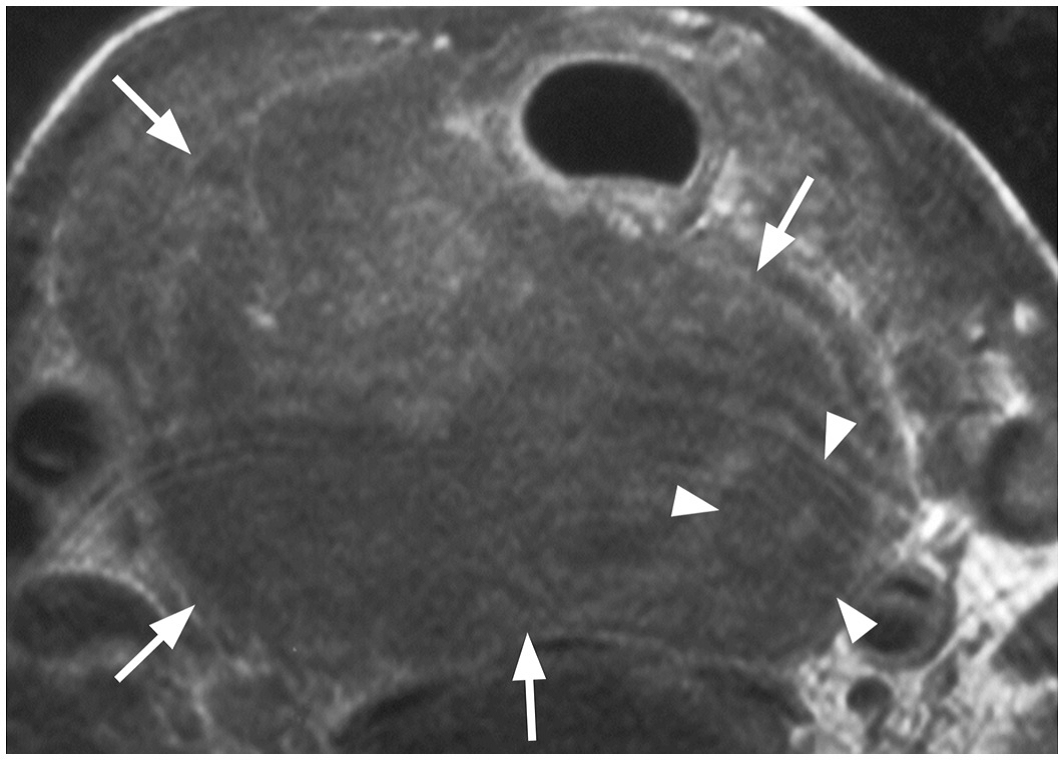
Hình3: Hình ảnh UTTG thể không biệt hóa trên T1W sau tiêm: u(mũi tên) bao quanh > 2700 và xâm lấn thực quản (đầu mũi tên).
Về đánh giá di căn hạch vùng: hạch di căn trên cộng hưởng từ có kích thước ngang trên 10mm hoặc/và tăng tín hiệu trên diffusion hoặc/và tăng tín hiệu tự nhiên trên T1W (do thyroglobulin). Theo N.D. Gross – 2001, giá trị dự báo dương tính và độ chính xác chẩn đoán di căn hạch vùng lần lượt là 86% và 85% [19].
Về chẩn đoán phân biệt bướu nhân tuyến giáp lành tính và ác tính, nghiên cứu của Razek 2008 trên 67 bệnh nhân, b 250, 500: ADC u ác 0,73; u lành 1,8±0,27 (p<0,0001); cut-off ADC 0,98; độ nhạy 97,5%; độ đặc hiệu 91,7%; độ chính xác 98,9% [20]. Srinivasan (2008) nghiên cứu 33 bệnh nhân có khối u vùng cổ trên máy MRI 3T: ADC u lành 1,5; u ác 1,1; p<0,004; cut-off ADC 1,3 [21]. Bozgeyik 2009 nghiên cứu 93 u tuyến giáp, ADC ác và lành: 0,96 và 3,06 (b100), 0,56 và 1,80 (b200), 0,3 và 1,15 (b300) [22]. Nakahira (2012) nghiên cứu 42 u tuyến giáp trên 38 bệnh nhân: cut-off của ADC là 1,60; độ nhạy 94,73%; độ đặc hiệu 82,60%; độ chính xác 88,09% [23].
A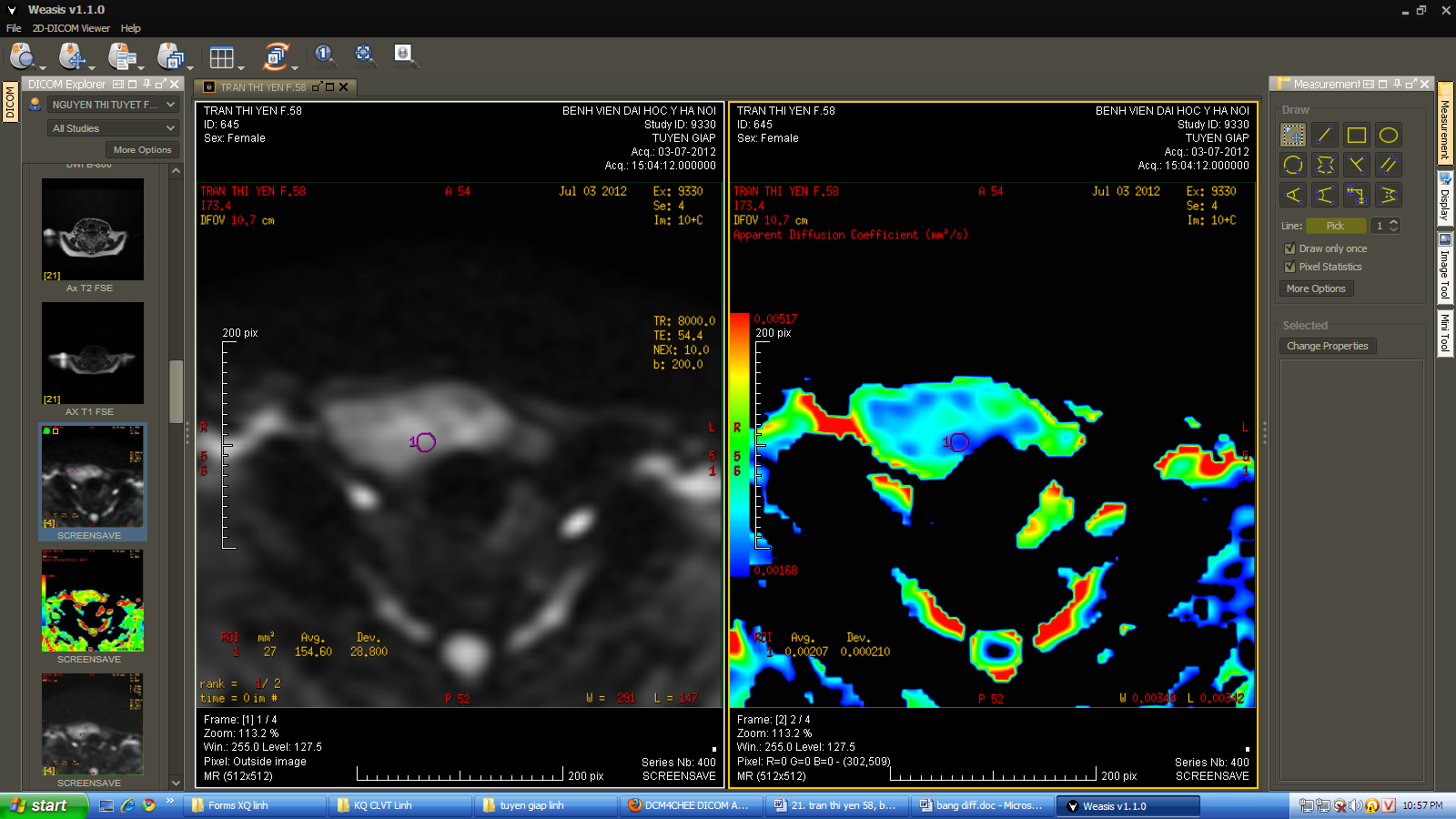
Hình 4: Hình ảnh đo ADC trên b200 của u tuyến giáp lành tính.
B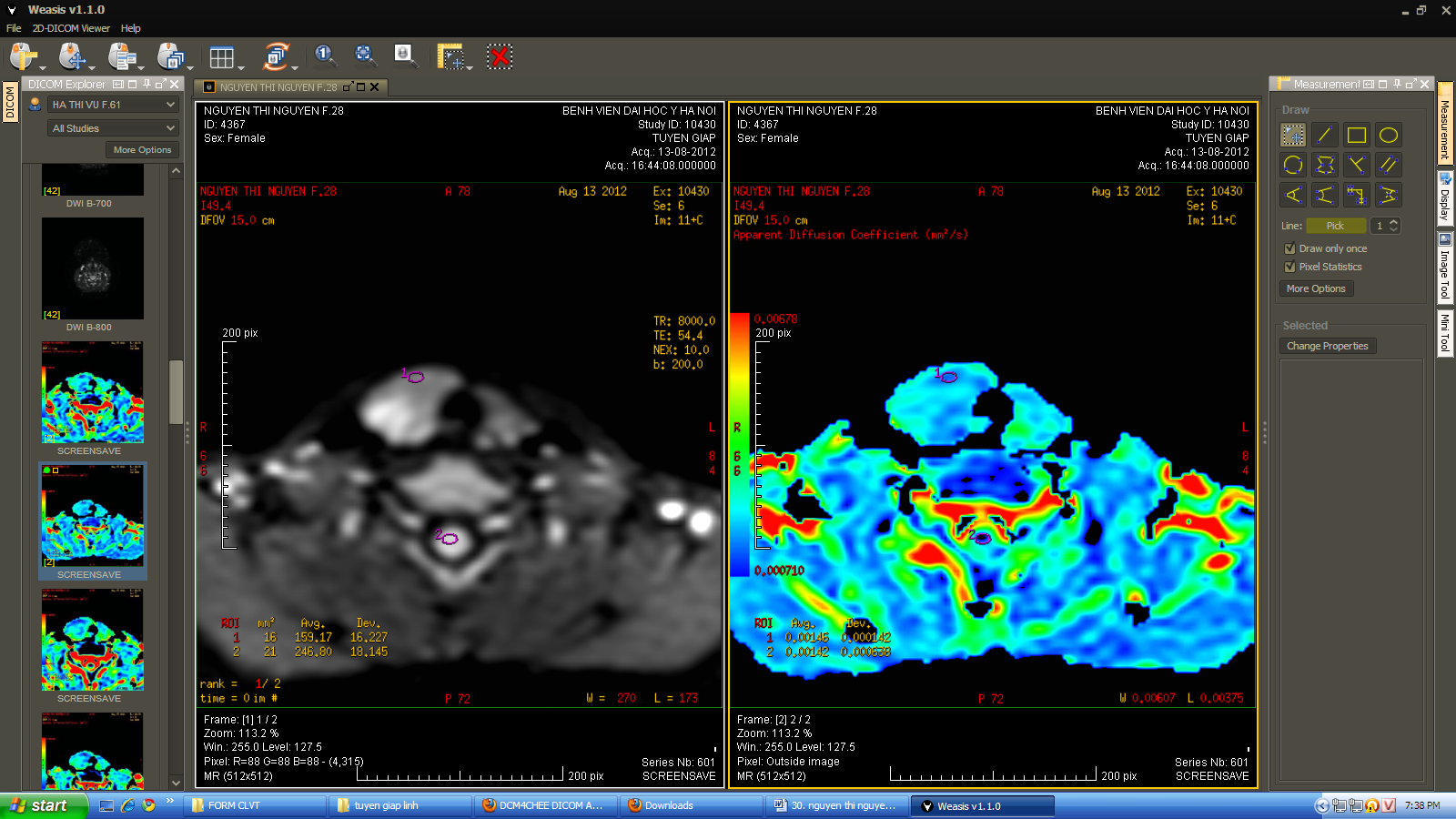
Hình 5. Hình ảnh đo ADC trên b200 của u tuyến giáp ác tính.
IV. KẾT LUẬN
Trước đây siêu âm chỉ dùng các dấu hiệu riêng lẻ để chẩn đoán phân biệt bướu lành và ác tính nên độ nhạy và độ đặc hiệu không cao, không thống nhất giữa các kết quả.
Hiện nay có phân loại TIRADS mới nhất dựa vào 6 dấu hiệu siêu âm: đặc/đặc là chủ yếu, giảm âm, rất giảm âm, bờ không đều/ múi nhỏ, vi vôi hóa, chiều cao > chiều rộng, chia làm các loại: TIRADS 0,1,2,3,4a,4b,4c,5,6. Đây là bảng phân loại TIRADS dễ áp dụng trên lâm sàng, dễ thống nhất các kết quả và có độ chính xác cao.
MRI từ lực cao ≥1.5T ngoài khả năng đánh giá xâm lấn tại chỗ ung thư tuyến giáp còn có chuỗi xung khuếch tán Diffusion có thể đo được cụ thể giá trị ADC, có khả năng tiên lượng tính chất lành tính hay ác tính của khối u tuyến giáp. Các tác giả vẫn chưa thống nhất được chỉ số cut-off của ADC, nhưng nhìn chung đều thống nhất: giá trị ADC càng thấp thì nguy cơ ác tính càng cao.
TÀI LIỆU THAM KHẢO
- Tan GH, Gharib H (1997).Thyroid incidentalomas: manegement approaches to nonpalpable nodules discovered incidentally on thyroid imaging. Ann Intem Med 126:226-231.
- Gharib H, Goellner (1993), Fine needle aspiration biopsy of the thyroid: an appraisal. Ann Intern Med. 1993; 118:282–9.
- John I. Lew and Carmen C. Solorzano (2010), Use of Ultrasound in the Management of Thyroid Cancer. The Oncologist, 15:253-258.
- Cooper DS, et al. (2009), Revised American Thyroid Association Management Guidelines for Patients with Thyroid Nodules and Differentiated Thyroid Cancer, The American Thyroid Association Guidelines Taskforce. Thyroid. Volume 19, Number 117.
- Robert A. Sofferman, Anil T. Ahuja (2012), Ultrasound of the Thyroid and Parathyroid Glands. Springer publisher.
- Moon WJ, Jung SL, Lee JH et al (2008), Benign and malignant thyroid nodules: US differentiation multicenter retrospective study. Radiology; 247(3):762–770.
- Jin Young Kwak, Kyung Hwa Han, et al (2011), Thyroid Imaging Reporting and Data System for US Features of Nodules: A Step in Establishing Better Stratification of Cancer Risk. Radiology; 260(3): 892-899.
- Khoo ML, Asa SL, Witterick IJ, Freeman JL. Thyroid calcification and its association with thyroid carcinoma. Head Neck 2002;24:651–655.
- Kim EK, Park CS, Chung WY, et al. New sonographic criteria for recommending fine-needle aspiration biopsy of nonpalpable solid nodules of the thyroid. AJR Am J Roentgenol 2002; 178:687–691.
- Frates MC, Benson CB, Doubilet PM, et al. Likelihood of thyroid cancer based on sonographic assessment of nodule size and composition. In: Radiological Society of North America Scientific Assembly and Annual Meeting Program. Oak Brook, Ill: Radiological Society of North America, 2004; 395.
- Frates MC, Benson CB, Doubilet PM, Cibas ES, Marqusee E. Can color Doppler sonography aid in the prediction of malignancy of thyroid nodules? J Ultrasound Med 2003;22:127–131.
- Papini E, Guglielmi R, Bianchini A (2002), et al. Risk of malignancy in nonpalpable thyroid nodules: predictive value of ultrasound and color-Doppler features. J Clin Endocrinol Metab;87:1941–6.
- Berni A, Tromba L, Falvo L, Marchesi M, Grilli P, Peparini N. (2002)Malignant thyroid nodules: comparison between color Doppler diagnosis and histological examination of surgical samples. Chir Ital;54:6437.
- Wienke JR, Chong WK, Fielding JR, Zou KH, Mittelstaedt CA (2003).Sonographic features of benign thyroid nodules: interobserver reliability and overlap with malignancy. J Ultrasound Med; 22:1027–1031.
- Horvath E, Majlis S, Rossi R, et al (2009), An ultrasonogram reporting system for thyroid nodules stratifying cancer risk for clinical management. J Clin Endocrinol Metab; 94(5):1748–1751.
- Ann D.King (2008).Imaging for staging and management of thyroid cancer.Cancer imaging. Vol 8- 2008 ; 57-69.
- Ji-chen Wang, Shodayu Takashima, Fumiyoshi Takayama (2001).Tracheal Invasion by Thyroid Carcinoma: Prediction Using MR Imaging. AJR 2001; 177
- Yousem DM, Hatabu H, Hurst RW et al (1995).Carotid artery invasion by head and neck masses: prediction with MR imaging. Radiology-1995; 195: 715-720.
- Gross N.D, Weissman J.L, Talbot J.M (2001).MRI detection of cervical metastasis from differentiated thyroid carcinoma. 111(11 Pt 1);1905-1909.
- Abdel Razek A.A.K, SadekA.G (2008).Role of Apparent Diffusion Coefficient Values in Differentiation Between Malignant and Benign Solitary Thyroid Nodules. JNR Am J Neuroradiol 29.
- Srinivasan A,Dvorak R(2008).Differentiation of benign and malignant pathology in the head and neck using 3T ADC values: early experience. AJNR Am J Neuroradiol;29.
- Bozgeyik Z, Coskun S(2009).Diffusion-weighted MR imaging of thyroid nodules. Neuroradiology 51(3).
- Nakahira M, Saito N(2012).Quantitative diffusion weighted magnetic resonance imaging as apowerful adjunct to fine needle aspiration cytology for assessment of cold thyroid nodules. Am J Otolaryngol;33(4).
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam