CẬP NHẬT LÂM SÀNG MỘT SỐ KIẾN THỨC LIÊN QUAN ĐẾN
BIẾN CHỨNG THẬN Ở BỆNH NHÂN ĐÁI THÁO ĐƯỜNG
PGS.TS.Hoàng Trung Vinh
Học viện Quân y
SUMMARY
Clinical update from chronic kidney disease in type 2 diabetes mellitus patients
The incidence and prevalence of diabetes mellitus (DM) continue to grow markedly throughout the world, due primarily to the increase in type 2 DM (T2DM). Although improvements in DM and hypertension management have reduced the proportion of diabetic individuals who develop chronic kidney disease (CKD) and progress to end-stage renal disease (ESRD), the sheer increase in people developing DM will have a major impact on dialysis and transplant needs. This KDIGO conference addressed a number of controversial areas in the management of DM patients with CKD, including aspects of screening for CKD with measurements of albuminuria and estimated glomerular filtration rate (eGFR); defining treatment outcomes; glycemic management in both those developing CKD and those with ESRD; hypertension goals and management, including blockers of the renin-angiotensin-aldosterone system; and lipid management
Keywords: Diabetes mellitus, chronic kidney disease, glomerular filtration rate (GFR).
TÓM TẮT
Tỷ lệ mắc và lưu hành đái tháo đường (ĐTĐ) tiếp tục gia tăng nhanh chóng trên toàn thế giới đặc biệt là ĐTĐ týp 2 (T2ĐTĐ). Mặc dầu đã có những cải thiện và hiệu quả đáng kể trong điều trị ĐTĐ và tăng huyết áp (THA) góp phần làm giảm tỷ lệ đối tượng ĐTĐ tiến triển thành bệnh thận mạn (BTM) và BTM giai đoạn cuối (GĐC) đồng thời cũng làm gia tăng đáng kể số trường hợp ĐTĐ có chỉ định điều trị bằng lọc máu và ghép thận. Trong các khuyến cáo của Hội thận học quốc tế (NKF) và Hội Nội tiết Đái tháo đường Hoa Kỳ (ADA) đã nêu ra các nội dung liên quan đến BTM do ĐTĐ bao gồm sàng lọc, chẩn đoán bệnh thận do ĐTĐ, mục tiêu và biện pháp kiểm soát các chỉ số ở bệnh nhân (BN) là chủ yếu kiểm soát glucose máu và huyết áp làm cơ sở cho điều trị đạt hiệu quả cao.
Từ khóa: Đái tháo đường, bệnh thận mạn, mức lọc cầu thận.
Chịu trách nhiệm chính: PGS.TS. Hoàng Trung Vinh.
Ngày nhận bài: 15.9.2017
Ngày phản biện khoa học: 17.9.2017
Ngày duyệt bài: 23.9.2017
ĐẶT VẤN ĐỀ
Tỷ lệ mắc và tần suất bệnh đái tháo đường gia tăng nhanh chóng trên toàn thế giới đặc biệt là ĐTĐ týp 2 (T2ĐTĐ). Đái tháo đường gây nhiều biến chứng cơ quan đích bao gồm biến chứng mạch máu nhỏ và mạch máu lớn. Trong số các biến chứng mạch máu nhỏ thì tổn thương thận do ĐTĐ xuất hiện sớm, gặp với tỷ lệ cao, là một trong các nguyên nhân chủ yếu dẫn đến tàn phế, tử vong. Mặc dù đã có những cải thiện trong điều trị ĐTĐ và tăng huyết áp (THA) góp phần làm giảm tần suất bệnh thận mạnnói chung và BTM giai đoạn cuối nói riêng song vẫn gia tăng tỷ lệ tuyệt đối các trường hợp cần phải áp dụng các biện pháp điều trị thay thế như lọc máu hoặc ghép thận. Công việc sàng lọc, phát hiện BTM do ĐTĐ cần được thực hiện thường xuyên, kịp thời làm cơ sở cho việc điều trị, kiểm soát đa yếu tố nhằm mục tiêu dự phòng, ngăn ngừa sự xuất hiện, làm chậm quá trình tiến triển hoặc kéo dài thời gian sống của bệnh nhân (BN) BTM GĐC. Các biện pháp điều trị BTM do ĐTĐ cần mang tính cá thể hóa bao gồm kiểm soát glucose, các yếu tố nguy cơ (YTNC) và biểu hiện của BTM. Tất cả các nội dung trên đều dựa vào các chứng cứ khoa học đã được nêu trong các đề tài, công trình nghiên cứu và các khuyến cáo liên quan đến các khía cạnh khác nhau của BTM do ĐTĐ sẽ được tập hợp và tóm tắt trong bài viết này.
I. DỊCH TỄ HỌC BỆNH THẬN MẠN Ở BỆNH NHÂN ĐÁI THÁO ĐƯỜNG
Trong quá trình tiến triển của bệnh khoảng 20 – 40% trường hợp ĐTĐ có biến chứng thận. Tuy vậy tỷ lệ mắc bệnh thận có sự khác nhau giữa các quốc gia, châu lục tùy thuộc vào đặc điểm đối tượng quan sát.
Theo số liệu quan sát của các tác giả châu Á công bố trên Diabcare Asia – 2008 thì một số biến chứng mạch máu gặp với các tỷ lệ: Thần kinh ngoại biên – 67,7%; võng mạc – 10,1%; thận – 8,2%; bệnh bàn chân – 6,8% [12].
Tỷ lệ BTM ở BN ĐTĐ tại Ấn độ chỉ dạo động trong khoảng 5,5 – 8,9%, trong khi đó người Anh gốc Ấn Độ thì tỷ lệ đó tăng lên 22,3%.
Nhìn chung có khoảng 25 – 45% ĐTĐ týp 1 xuất hiện BTM; 80 – 90% trường hợp với microalbumin niệu (MAU) sẽ tiến triển thành BTM lâm sàng sau 5 – 10 năm xuất hiện bệnh. Ở BN T2ĐTĐ tại thời điểm xuất hiện bệnh THA đã có khoảng 50% trường hợp biểu hiện MAU (+); 10 – 20% với MAU (+) sẽ tiến triển thành bệnh thận lâm sàng. Có tới gần 100% trường hợp với protein niệu (+) sẽ tiến triển thành BTM GĐC trung bình sau 7 – 10 năm (ADA-standart of medical care in diabetes. Diabetes care 2014; 37 (suppl 1) S14 [2], [13].
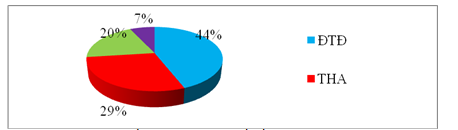
Tại Hoa Kỳ số liệu công bố năm 2017 bởi National chronic Kidney Disease Fact Sheet cho thấy có khoảng 30 triệu người tương ứng 15% dân số lớn tuổi mắc BTM trong số đó có khoảng 1/3 là do ĐTĐ (1/5 là do THA). Nếu tính chung các nguyên nhân mới xuất hiện BTM GĐC ở Mỹ được phân bố với các tỷ lệ sau: ĐTĐ – 44%; THA – 29%; nguyên nhân khác – 20% và không rõ nguyên nhân – 7% [7], [8].
Khảo sát của các tác giả Ấn Độ ở 3043 BN T2ĐTĐ trong nghiên cứu đa trung tâm cho thấy 48,4% biểu hiện BTM. Trong tổng số BN gặp 47,8% giảm mức lọc cầu thận (MLCT) rất nhẹ; 15,1% giảm nhẹ đến vừa; 1,8% giảm mức độ nặng. Cũng trong các đối tượng trên phát hiện 61,3% có albumin/creatinin ratio (ACR) từ bình thường đến tăng rất nhẹ; 25,6% tăng mức trung bình; 7,2% tăng mức độ nặng. Nếu phân chia theo giai đoạn BTM sẽ có các tỷ lệ tương ứng: 28,1% giai đoạn 1; 47,8% giai đoạn 2; 15,1% giai đoạn 3a; 6,3% giai đoạn 3b; 1,8% giai đoạn 4; 0,7% giai đoạn 5 [11].
Các tác giả Bangladesh năm 2017 đã công bố kết quả khảo sát 400 BN T2ĐTĐ với thời gian phát hiện bệnh khác nhau nhận thấy tỷ lệ BTM 3 – 5 dựa vào MLCT ước lượng theo các công thức khác nhau bao gồm MDRD, Cockcroft – Gault và CKD – EPI (chronic Kidney Disease Epidemiology) lần lượt là: 63,5%; 64,75% và 54,5%. Các YTNC làm gia tăng BTM ở BN T2ĐTĐ được xác định bao gồm giới nữ, thời gian phát hiện bệnh ≥ 5 năm; THA, kiểm soát glucose máu (> 7%) [10]. Tỷ lệ BTM GĐC do T2ĐTĐ cũng gia tăng theo thời gian. Nếu năm 1985 tại Hàn Quốc tỷ lệ đó chiếm khoảng 10% thì năm 2014 đã lên đến 48% [5].
Ở Việt Nam đã có một số tác giả nghiên cứu nhiều khía cạnh biến chứng thận ở BN ĐTĐ, tuy vậy chưa có số liệu thống kê chung về tỷ lệ mắc BTM ở BN ĐTĐ trên phạm vi toàn quốc mà chỉ là những quan sát đơn lẻ tại một số địa dư hoặc bệnh viện. Nguyễn Thị Thanh Thúy năm 2000 nhận thấy MAU (+) gặp ở 44,23% BN T2ĐTĐ; Hồ Hữu Hóa – 2009 là 45,7%. Đỗ Quốc Thiên Hương – 2014 khảo sát BN T2ĐTĐ > 60 tuổi nhận thấy 46,6% biến chứng thận nói chung. Trần Thị Ngọc Thư – 2014 nhận thấy có 38,9% trường hợp T2ĐTĐ với ACR (+) [1].
II. CƠ CHẾ BỆNH SINH TỔN THƯƠNG DO ĐÁI THÁO ĐƯỜNG
Cơ chế bệnh sinh tổn thương thận do ĐTĐ rất phức tạp, là sự phối hợp của nhiều yếu tố khác nhau. Tuy vậy yếu tố bệnh sinh chủ yếu gây tổn thương thận ở BN ĐTĐ bao gồm rối loạn huyết động và chuyển hóa trong đó đóng vai trò chủ yếu là tăng glucose máu và rối loạn lipid máu mạn tính, tương tác với nhau gây ra bệnh thận do ĐTĐ [5].
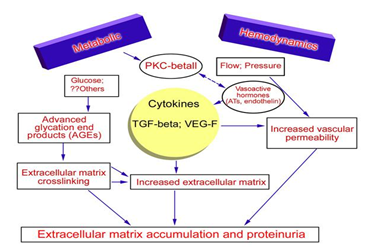
Sơ đồ 2.1. Cơ chế hình thành chất mầm gian mạch và protein niệu ở BN ĐTĐ
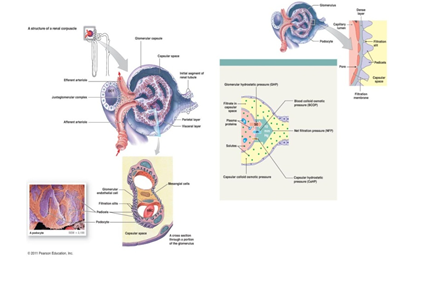
Sơ đồ 2.2. Sơ đồ rối loạn huyết động tại mao mạch cầu thận
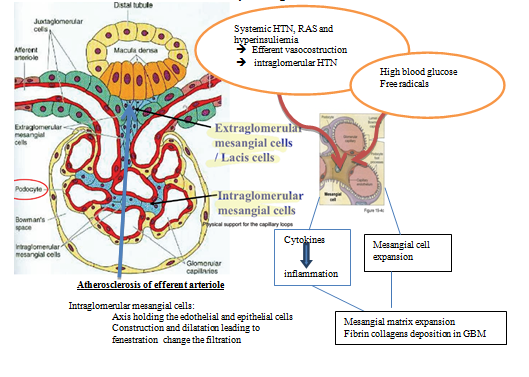
Sơ đồ 2.3. Sơ đồ tác động của các yếu tố đối với hiện tượng động mạch đi của cầu thận
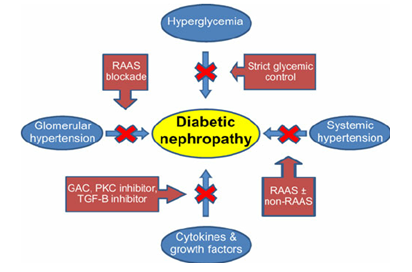
Sơ đồ 2.4. Tổng hợp các yếu tố gây bệnh thận mạn trong đái tháo đường [6]
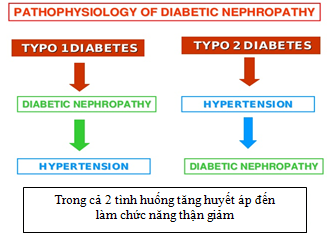 Sơ đồ 2.5. Tiến triển bệnh thận mạn trong đái tháo đường týp 1, 2
Sơ đồ 2.5. Tiến triển bệnh thận mạn trong đái tháo đường týp 1, 2
Rối loạn huyết động là cơ chế chủ yếu gây bệnh thận mạn do ĐTĐ. Sự thay đổi huyết động hệ thống và tại thận đều là các yếu tố quan trọng trong cơ chế bệnh sinh của bệnh thận do ĐTĐ. Tăng huyết áp thường xuất hiện trước khi giảm MLCT và là yếu tố làm tăng tỷ lệ tiến triển thành bệnh thận do ĐTĐ. Tăng MLCT xuất hiện ở giai đoạn sớm của bệnh và là yếu tố liên quan đến suy thận ở giai đoạn muộn. Tăng glucose máu được coi là yếu tố chủ yếu gây hiện tượng tăng MLCT. Mức độ kiểm soát glucose máu liên quan đến sự hình thành và tiến triển của bệnh thận. Nếu kiểm soát glucose máu tốt và làm giảm áp lực cầu thận cũng như huyết áp hệ thống có thể làm chậm quá trình suy giảm chức năng thận và sự thay đổi mô bệnh học của bệnh thận, sự bất thường của glycosyl hóa (đường hóa) protein tạo thành chất mầm gian mạch, sự tăng tưới máu và tăng sinh của mao mạch cầu thận. Tất cả các yếu tố trên sẽ dẫn đến sơ cứng mao mạch cầu thận. Ảnh hưởng của gen đối với sự xuất hiện của bệnh thận do ĐTĐ cũng đã được khẳng định [5].
III. TIẾN TRIỂN CỦA BỆNH THẬN TRONG ĐÁI THÁO ĐƯỜNG
Bệnh thận mạn xuất hiện ở BN ĐTĐ từ giai đoạn rất sớm thậm chí kể từ khi có tình trạng kháng insulin trong T2ĐTĐ. Sự xuất hiện và tiến triển của bệnh thận trải qua các giai đoạn [9]:
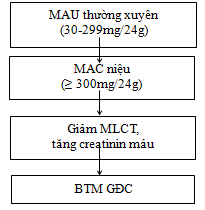
Mặc dù đa số BN ĐTĐ kèm THA có albumin niệu thường xuyên ở mức 30 – 299 mg/24h nhưng chỉ có 1/3 tiến triển đến BTM ở các giai đoạn tiếp theo.
+ ĐTĐ týp 1: 25% có tiểu albumin thường xuyên ở mức 30 – 299 mg/24h sau 15 năm; < 50% những BN này tiến triển đến bệnh thận nặng hơn.
+ ĐTĐ týp 2: 25% có albumin niệu ở mức 30 – 299 mg/24h sau 10 năm; 0,8% có creatinin ≥ 2,0 mg/dl (≥ 17,7 mmol/l).
3.1. Giai đoạn bệnh thận do đái tháo đường týp 1
Năm 1984, Mogensen và Christensen đã mô tả sự tiến triển của bệnh thận ở BN ĐTĐ týp 1 và chia quá trình này thành 5 giai đoạn [1]:
– Giai đoạn 1 là giai đoạn tăng siêu lọc, tăng kích thước thận, đặc trưng bởi sự tăng MLCT từ 20 – 50% so với độ tuổi của bệnh nhân. MAU thường ở mức > 20 µg/phút nhưng < 200 µg/phút. Sau vài tuần dùng insulin thì hiện tượng tăng siêu lọc và tăng kích thước thận giảm đi, MAU ở mức < 20 µg/phút.
– Giai đoạn 2 tiến triển thầm lặng với mức MAU bình thường hoặc gần bình thường (20 µg/phút), xuất hiện ở 90 – 95% bệnh nhân bị bệnh từ 1 -5 năm. MLCT bình thường ở hầu hết BN. Giãn mao mạch và dày màng nền cầu thận thường thấy khi kiểm tra bằng mô bệnh học.
– Giai đoạn 3 thường bắt đầu 5 -15 năm từ khi mắc bệnh. Hiện tượng giãn mao mạch và dày màng nền cầu thận tiếp tục tăng lên. MLCT bắt đầu giảm ở cuối giai đoạn này. MAU có thể ở mức 20 – 200 µg/phút (200 – 300 µg/phút). Tăng huyết áp áp cũng sẽ xuất hiện ở giai đoạn này.
– Giai đoạn 4 là giai đoạn bệnh thận đã biểu hiện rõ ràng, protein niệu thường xuyên dương tính (> 0,5 g/24h). THA thường không ổn định, MLCT giảm dần. Trên mô bệnh học quan sát sát thấy xơ cứng gian mạch cầu thận lan tỏa hoặc khu trú.
– Giai đoạn 5 là giai đoạn suy thận giai đoạn cuối, xuất hiện trung bình khoảng 20 năm kể từ khi mắc bệnh ĐTĐ týp 1. Tổn thương giải phẫu bệnh đặc trưng bởi hiện tượng xơ cứng các cầu thận.
3.2. Tiến triển của bệnh thận do ĐTĐ týp 2
Ngay từ khi mới chẩn đoán ĐTĐ týp 2 thì MAU đã có thể dương tính song có thể sẽ thay đổi nếu kiểm soát tốt glucose máu. Bệnh thận do ĐTĐ týp 2 hiếm khi có tăng MLCT và không thấy có phì đại cầu thận. Các yếu tố khác ảnh hưởng đến sự phát triển bệnh thận do ĐTĐ týp 2 có thể là THA, tăng glucsoe máu và hút thuốc lá. Bên cạnh đó, ở bệnh nhân ĐTĐ có xu hướng tăng tỷ lệ nhiễm khuẩn đường tiết niệu (có vi khuẩn niệu, viêm bàng quang, viêm bể thận) hoại tử nhú thận và bệnh thần kinh bàng quang [1], [9].
IV. ĐẠC ĐIỂM GIẢI PHẨU BỆNH CỦA THẬN TỔN THƯƠNG DO ĐÁI THÁO ĐƯỜNG
Các tổn thương giải phẫu bệnh tại thận của BN bị bệnh thận do ĐTĐ bao gồm các tổn thương ở cầu thận, mạch máu và ống kẽ thận [1]:
+ Tổn thương cầu thận:
– Xơ cứng gian mạch cầu thận lan tỏa.
– Xơ cứng gian mạch cầu thận khu trú.
– Tổn thương bao dạng giọt (Capsular drop lesion).
– Dày màng nền cầu thận.
+ Tổn thương mạch máu:
– Xơ cứng dưới nội mạch tiểu động mạch do hydalin.
– Vữa xơ động mạch lành tính.
+ Tổn thương ống thận và kẽ thận.
– Tổn thương dạng giọt nhỏ do hyalin ở ống lượn gần.
– Lắng đọng glycogen (tổn thương Armanni – Ebstain).
– Teo đét ống thận.
– Xơ hóa khe thận.
V. SÀNG LỌC, CHẨN ĐOÁN BỆNH DO ĐÁI THÁO ĐƯỜNG
Các nội dung sàng lọc, chẩn đoán bệnh thận do đái tháo đường và điều trị bệnh nhân đái tháo đường có tổn thương thận được nêu ra trong khuyến cáo thực hành lâm sàng của KDOQI – 2012 trên cơ sở có chỉnh sửa, bổ sung của khuyến cáo lần 1 năm 2007 [3], [8].
Mức độ tin cậy của các nội dung khuyến cáo căn cứ vào các thử nghiệm lớn quốc tế bao gồm:
Cấp độ chứng cứ
 Mức độ của khuyến cáo
Mức độ của khuyến cáo

Khuyến cáo sàng lọc và chẩn đoán bệnh thận do đái tháo đường [13].
+ Thời gian bắt đầu sàng lọc:
– 5 năm sau chẩn đoán ĐTĐ týp 1 (A) hoặc
– Tại thời điểm chẩn đoán ĐTĐ týp 2 (B).
+ Các xét nghiệm sử dụng trong sàng lọc chẩn đoán bệnh thận do ĐTĐ.
– Định lượng ACR 1 một mẫu nước tiểu sáng sớm (B).
– Định lượng nồng độ creatinin huyết thanh để ước lượng mức lọc cầu thận (B).
+ Tiêu chuẩn chẩn đoán bệnh thận mạn do ĐTĐ.
– Nếu tăng ACR lần 1 thì làm tiếp 2 lần trong 3 – 6 tháng tiếp theo khi k có nhiễm trùng đường niệu. Bệnh thận mạn được xác định khi (B):
. MAU – 30 – 300 mg/g:
. MAC > 300 mg/g.
. Phải có ít nhất 2 trong 3 lần xét nghiệm đạt 1 trong 2 chỉ tiêu trên.
– Hầu hết BN ĐTĐ có MAU hoặc MAC (+) là do ĐTĐ gây ra nếu có:
. Sự xuất hiện MAC (B) hoặc
. Sự xuất hiện MAU khi có bệnh võng mạc do ĐTĐ (B) hoặc ĐTĐ týp 1 xuất hiện sau 10 năm (A).
ADA năm 2009 đã đưa ra tầm soát bệnh thận do ĐTĐ bao gồm [2]:
– Đánh giá bài xuất albumin niệu mỗi năm (B) khi albumin niệu ≥ 300 µg/mg creatinin:
. Đối với BN ĐTĐ týp 1 có thời gian mắc bệnh ≥ 5 năm.
. Đối với tất cả BN ĐTĐ týp 2 tại thời điểm chẩn đoán
– Định lượng creatinin máu ít nhất mỗi năm 1 lần ở tất cả BN bất kể mức độ bài suất albumin niệu (D).
Một số nguyên nhân có thể gây MAU (+) giả:
– Xét nghiệm được thực hiện khi gắng sức.
– Bệnh nhân có biểu hiện mất nước cấp tính.
– Đái ra máu vi thể hoặc đại thể do các nguyên nhân khác.
– Phụ nữ đang có kinh nguyệt.
– Nhiễm khuẩn tiết niệu.
– Hoại tử nhú thận.
– Thu thập sai mẫu nước tiểu để xét nghiệm.
Theo ADA năm 2009 bổ sung một số nguyên nhân gợi ý bệnh thận mạn không do ĐTĐ bao gồm [13]:
– Không có bệnh võng mạc do ĐTĐ.
– Mức lọc cầu thận thấp hay giảm nhanh.
– Tiểu protein hay hội chứng thận hư diễn tiến nhanh.
– Xuất hiện protein niệu < 5 năm từ khi mắc ĐTĐ týp 1.
– Tăng huyết áp kháng trị.
– Hiện diện của cặn lắng nước tiểu hay tiểu máu đơn độc.
– Có triệu chứng hay dấu hiệu của các bệnh toàn thân khác.
– Giảm MLCT > 30% sau 2 – 3 tháng khởi trị bằng ức chế men chuyển hoặc ức chế AT1..
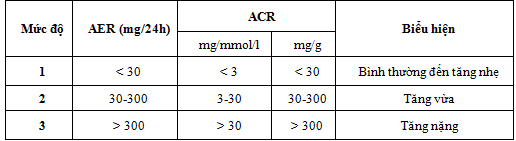
Phân loại mức độ tổn thương thận dựa vào albumin niệu
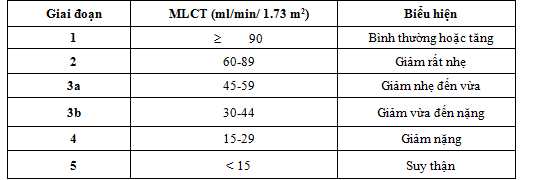
Phân loại giai đoạn bệnh thận mạn theo NKF
Tiên lượng BTM dựa vào MLCT và albumin niệu theo KDOQI-2012
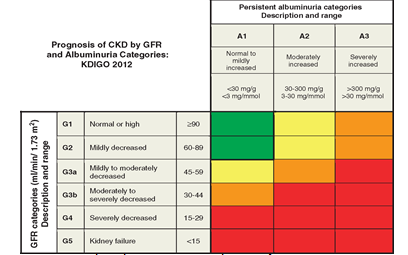
– Màu xanh: Nguy cơ thấp (nếu không có các dấu hiệu tổn thương thận hoặc BTM)
– Màu vàng: Tăng nguy cơ mức độ vừa
– Da cam : Nguy cơ cao
– Màu đỏ : Nguy cơ rất cao
VI. KHUYẾN CÁO ĐIỀU TRỊ BỆNH NHÂN ĐÁI THÁO ĐƯỜNG CÓ TỔN THƯƠNG THẬN
Khuyến cáo điều trị bệnh thận do ĐTĐ theo ADA – 2014 [13].
Mục tiêu là kiểm soát đường huyết và huyết áp tối ưu.
* Khuyến cáo kiểm soát glucose máu
+ HbA1c khoảng 7,0% sẽ có tác dụng dự phòng hoặc làm chậm tiến triển các biến chứng mạch máu nhỏ của BN ĐTĐ trong đó có BTM do ĐTĐ [1A]
+ Không nên đưa HbA1c < 7,0% ở những BN có nguy cơ xuất hiện cơn hạ đường huyết [1B]
+ Có thể duy trì HbA1c > 7,0% đối với những BN có bệnh kèm theo hoặc thời gian sống không kéo dài và nguy cơ cơn hạ đường huyết [2C]
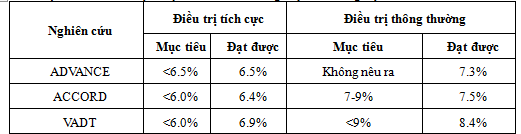
* Mục tiêu và mức đạt được của HbA1c trong một số thử nghiệm
 * Sử dụng insulin và thuốc uống ở BN BTM giai đoạn 3, 4, 5 không LMCK
* Sử dụng insulin và thuốc uống ở BN BTM giai đoạn 3, 4, 5 không LMCK
Glargine* : Điều chỉnh liều cho phù hợp
Detemir* : Điều chỉnh liều cho phù hợp
NPH* : Điều chỉnh liều cho phù hợp
Regular* : Điều chỉnh liều cho phù hợp
Aspart* : Điều chỉnh liều cho phù hợp
Lispro* : Điều chỉnh liều cho phù hợp
Glulisine* : Điều chỉnh liều cho phù hợp
* Điều chỉnh liều dựa vào đáp ứng của BN
** Thuốc không được sử dụng tại Mỹ
*** Đang tranh luận

Sau khi đạt HA mục tiêu và liều dùng đã ổn định
* Biguanides
Metformin***: FDA không sử dụng nếu creatinin máu >130mmol/l ở nam, >126mmol/l ở nữ. Ở Anh và Hội thận học Nhật Bản tạm ngừng nếu MLCT <30 ml/min/1.73 m2

* DPP-4 inhibitor
Sitagliptin: MLCT >50 ml/min/1.73 m2: 100 mg/ngày MLCT 30-50 ml/min/1.73 m2: 50 mg/ngày MLCT <30 ml/min/1.73 m2: 25 mg/ngày.

* Khuyến cáo kiểm soát huyết áp [4].
+ Chẩn đoán THA ở BN ĐTĐ với BTM: ³ 130/80 mmHg
+ Mục tiêu kiểm soát HA: < 130/80 mmHg [B].
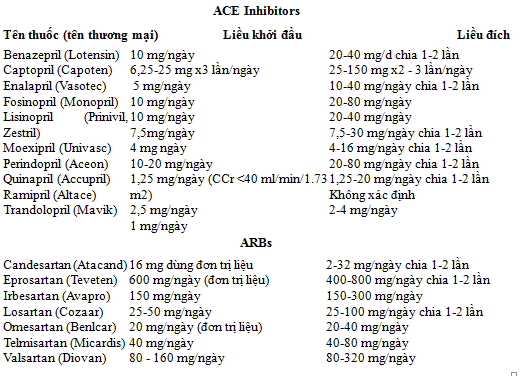
+ Thuốc được sử dụng: ƯCMC hoặc ƯC AT1 [A].
+ Thuốc khác để giảm nguy cơ bệnh tim mạch và đạt HA mục tiêu: Lợi tiểu được khuyên dùng hơn so với ƯC b hoặc chẹn kênh canxi [A].
* Theo dõi HA, MLCT và K+ khi dùng thuốc
Sau liều khởi đầu hoặc đang điều chỉnh liều
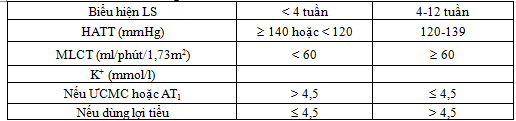
Sau khi đạt HA mục tiêu và liều dùng đã ổn định

* Khuyến cáo kiểm soát lipid máu
+ Giảm LDL-c bằng statin hoặc phối hợp statin với Ezetimibe có tác dụng giảm nguy cơ VXĐM ở BN ĐTĐ có BTM bao gồm cả BN đã ghép thận [1B].
+ Không nên bắt đầu bằng statin ở BN ĐTĐ đang LMCK vì tác dụng giảm các biến cố liên quan đến VXĐM không rõ [1B].
Điều chỉnh liều lượng thuốc điều trị RLLP
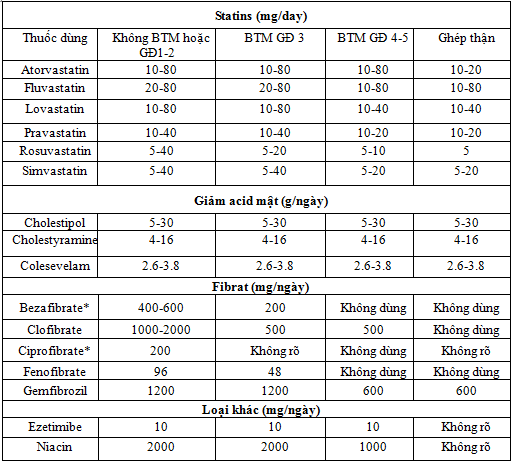
* Khuyến cáo tiết chế ăn uống [4].
+ Lượng protein ăn < 0,8 g/kg/ngày đối với BN lớn tuổi có MLCT< 30 ml/phút/1,73m2 [2C].
+ Lượng protein ăn không vượt quá 1,3g/kg/ngày đối với những BN có nguy cơ tiến triển BTM [2C].
+ Lượng muối ăn < 2g/ngày [1C].
+ Không có bằng chứng ủng hộ hoặc phủ nhận sử dụng thuốc hạ acid uric máu có tác dụng làm chậm tiến triển của BTM ở BN ĐTĐ với BTM có hay không có triệu chứng của tăng acid uric máu [không xếp cấp độ].
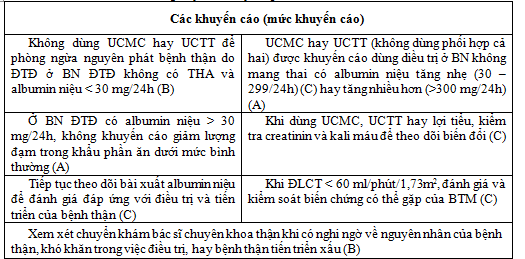
* Khuyến cáo điều trị hạ albumin niệu ở BN ĐTĐ có BTM với HA bình thường
+ Không sử dụng ƯCMC hoặc ƯC AT1 để dự phòng cấp 1 BTM do ĐTĐ khi BN ĐTĐ có HA và albumin niệu ở mức bình thường [1A].
+ Nên sử dụng ƯCMC hoặc ƯC AT1 ở BN ĐTĐ với HA bình thường có ACR ³ 30mg/g vì có nguy cơ cao gây BTM hoặc tiến triển BTM do ĐTĐ [2C].
* Một số lưu ý khi sử dụng thuốc hạ albumin niệu
+ Ở BN ĐTĐ với BTM có HA bình thường không xác định liều đích ƯCMT hoặc ƯC AT1. Nếu không có tác dụng phụ do thuốc (tăng K+, suy thận cấp) thì nên sử dụng liều thấp hơn so với liều điều trị THA.
+ Không khuyến khích phối hợp ƯCMC với ƯC AT1 cũng như các thuốc ức chế khác hệ RAA.
+ Sử dụng ƯCMC, ƯC AT1 ở BN có thai 3 tháng đầu có thể làm gia tăng tổn thương thận cấp ở trẻ sau sinh, độc với phổi, nguy cơ gây bệnh bẩm sinh hệ tim mạch, TKTW và thận.
* Theo dõi và kiểm soát BTM ở BN ĐTĐ [3], [13].
ADA năm 2014 đã nêu ra nội dung theo dõi và kiểm soát BTM ở BN ĐTĐ dựa vào MLCT với các mức sau.
+ Tất cả bệnh nhân được xét nghiệm creatinin máu, albumin niệu, kali máu mỗi năm.
+ Mức lọc cầu thận: 45 – 60 ml/phút/1,73m2
– Chuyển khám chuyên khoa thận nếu nghi ngờ có bệnh thận không do ĐTĐ.
– Xem xét điều chỉnh liều thuốc.
– Theo dõi MLCT ước tính mỗi 6 tháng
– Xét nghiệm ion đồ, bicarbonate, hemoglobin, calcium, phosphorus, PTH ít nhất mỗi năm 1 lần.
– Đảm bảo đủ vitamin D.
– Xem xét làm xét nghiệm đo mật độ xương.
– Tư vấn chế độ dinh dưỡng.
+ Mức lọc cầu thận: 30 – 44 (ml/phút/1,73m2):
– Theo dõi MLCT ước tính mỗi 3 tháng.
– Xét nghiệm ion đồ, bicarbonate, calcium, phosphorus, PTH, hemoglobin, albumin, cân nặng mỗi 3 – 6 tháng.
– Xem xét điều chỉnh liều thuốc.
+ Mức lọc cầu thận < 30 (ml/phút/1,73m2) chuyển khám bác sĩ chuyên khoa thận.
KẾT LUẬN
Tổn thương thận là một trong các biến chứng mạch máu nhỏ rất hay gặp, xuất hiện sớm ở BN ĐTĐ. Tỷ lệ biến chứng thận gia tăng theo tỷ lệ mắc bệnh và thời gian phát hiện bệnh.
Các biện pháp sàng lọc, chẩn đoán bệnh thận mạn do ĐTĐ cần được thực hiện định kỳ theo các khuyến cáo đã nêu. Dựa vào biểu hiện tổn thương thận để nêu ra và áp dụng các biện pháp điều trị, theo dõi cho phù hợp, đạt mục tiêu kiểm soát đa yếu tố trong đó quan trọng nhất là kiểm soát glucose máu và huyết áp.
Các biện pháp và mục tiêu điều trị BTM do ĐTĐ cần được cá thể hóa. Thực hiện đầy đủ, đúng các nội dung khuyến cáo đã nêu là cơ sở để dự phòng, điều trị và làm chậm tiến triển của bệnh thận mạn do ĐTĐ.
TÀI LIỆU THAM KHẢO
- Thái Hồng Quang, Hoàng Trung Vinh (2009), “Phòng chống và điều trị biến chứng thận do đái tháo đường”, Khuyến cáo về bệnh đái tháo đường của Hội Nội tiết và Đái tháo đường Việt Nam, tr.66-72.
- American Association of Diabetes Educators (2017), “Diabetes and kidney disease AADE Practice Paper”, pp.1-7.
- Bilo H., Coentrao L, Couchjoud C. et al (2015), “Clinical Practice Guideline on management of patients with diabetes and chronic kidney disease stage 3b or higher (eGFR < 45 ml/min)”, Nephrol Dial Transplant, 30(2), pp.ii1-ii142.
- Hahr A. J., Molitch M.E. (2015), “Management of diabetes mellitus in patients with chronic kidney disease”, Clinical diabetes and endocrinology, 1 (2), pp.1-9.
- Kim Y., Park C. W. (2017), “New therapeutic agents in diabetic nephropathy”, Korean J Intern Med, 32(1), pp.11-25.
- Molitch M. E., Adler A. I., Flyvbjerg A. et al (2014), “Diabetic kidney disease: a clinical update from Kidney disease: Improving Global Outcomes”, International Society of Nephrology, pp.1-11.
- National chronic Kidney Disease Fact Sheet (2017).
- National Kidney Foundation – KDOQI (2012), “KDOQI clinical practice guideline for diabetes and CKD: 2012 UPDATE”, Am I Kidney Dis, 60(5), pp.850-886.
- Radcliffe N. J., Seah J. M., Clarke M. et al (2017), “Clinical predictive factors in diabetic kidney disease progression”, J Diabetes Investig, 8(1), pp.6-18.
- Rahim M. A., Mitra P., Haque H. F. et al (2017), “Prevalence of chronic kidney disease stages 3-5 among patients with type 2 diabetes mellitus in Bangladesh”, IMC J Med Sci, 11(1), pp.19-24.
- Rajput R., Kumar K. M. P., Seshadri K. et al (2017), “Prevalence of Chronic Kidney Disease (CKD) in Type 2 Diabetes Mellitus Patients: START – India Study”, Journal of Diabetes & Metabolism, pp.1-11.
- Diabcare Asia (2008), “Study”, Med J. Indones 2010, 19, pp.235-44.
- ADA (2014), “Standart ò medical care in diabetes.”, Diabetes care, 37(1), S14.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam