COVID – 19 VÀ ĐÁI THÁO ĐƯỜNG:
TỪ CƠ CHẾ SINH LÝ BỆNH ĐẾN ĐIỀU TRỊ LÂM SÀNG
Hoàng Trung Vinh , Phạm Thị Hồng Hoa, Trần Quốc Luận
DOI: 10.47122/vjde.2022.51.2
SUMMARY
Covid-19 and diabetes mellitus: from pathophysiology to clinical management
Initial studies found increased severity of coronavirus disease 2019 (COVID-19), caused by infection with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2), in patients with diabetes mellitus. Furthermore, COVID-19 might also predispose infected individuals to hyperglycaemia. Interacting with other risk factors, hyperglycaemia might modulate immune and inflammatory responses, thus predisposing patients to severe COVID-19 and possible lethal outcomes. Angiotensin-converting enzyme 2 (ACE2), which is part of the renin–angiotensin– aldosterone system (RAAS), is the main entry receptor for SARS-CoV-2; although dipeptidyl peptidase 4 (DPP4) might also act as a binding target. Preliminary data, however, do not suggest a notable effect of glucose-lowering DPP4 inhibitors on SARS-CoV-2 susceptibility. Owing to their pharmacological characteristics, sodium–glucose cotransporter 2 (SGLT2) inhibitors might cause adverse effects in patients with COVID-19 and so cannot be recommended. Currently, insulin should be the main approach to the control of acute glycaemia. Most available evidence does not distinguish between the major types of diabetes mellitus and is related to type 2 diabetes mellitus owing to its high prevalence. However, some limited evidence is now available on type 1 diabetes mellitus and COVID-19. Most of these conclusions are preliminary, and further investigation of the optimal management in patients with diabetes mellitus is warranted.
Keywords: Diabetes mellitus, coronavirus disease 2019 (COVID-19), severe acute
respiratory syndrome coronavirus 2 (SARS- CoV-2).
TÓM TẮT
Nhiều nghiên cứu cho thấy sự gia tăng mức độ nặng của nhiễm covid – 19 ở bệnh nhân đái tháo đường (BN ĐTĐ) bởi sự xuất hiện hội chứng nhiễm trùng hô hấp cấp tính nặng do coronavirut 2 gây ra (SARS-CoV-2). Covid-19 có thể gia tăng nguy cơ nhiễm ở đối tượng tăng glucose máu. Khi tương tác với các yếu tố nguy cơ khác thì tăng glucose có thể gây biến đổi đáp ứng miễn dịch và viêm, điều này có thể làm cho tình trạng nhiễm trùng nặng hơn thậm chí gây tử vong. Enzym ức chế chuyển dạng angiotensin 2 (ACE2) thuộc hệ thống renin- angiotensin – aldosteron system (RAAS) là thụ thể chính giúp virut xâm nhập vào các cơ quan và tổ chức mặc dù dipeptidyl peptidase 4 (DPP4) có thể tương tác với cơ quan đích mang virut. Những dữ liệu nghiên cứu ban đầu cho thấy không có giả thuyết nào được chấp nhận nêu tác dụng đáng kể của ức chế DPP4 đối với SARS-CoV-2. Với đặc điểm về dược lý thì thuốc ức chế vận chuyển glucose phụ thuộc kênh Na+2 (SGLT2) có thể gây ra một số tác dụng không mong muốn ở BN covid – 19 vì vậy hạn chế được sử dụng trong một số trường hợp. Hiện nay, insulin vẫn là sự lựa chọn chủ yếu để kiểm soát tăng glucose giai đoạn cấp tính của bệnh. Đa số bằng chứng cho thấy mối liên quan của covid – 19 với ĐTĐ không có sự khác biệt giữa các típ, mặc dù trong lâm sàng thì ĐTĐT2 có tỷ lệ mắc cao hơn. Đối với ĐTĐT1 hiện có rất ít bằng chứng nghiên cứu về mối liên quan với covid – 19. Đa số các nghiên cứu hiện tại và có thể trong tương lai cũng đều nhấn mạnh việc kiểm soát tối ưu glucose ở BN ĐTĐ là điều cần thiết nhất.
Từ khóa: Đái tháo đường, bệnh do coronavirut 2019 (covid – 19), hội chứng hô hấp cấp tính nặng do coronavirut 2 (SARS- CoV-2).
Tác giả liên hệ: Hoàng Trung Vinh
Email: [email protected]
Ngày nhận bài: 5/12/2021
Ngày phản biện khoa học: 25/12/2021
Ngày duyệt bài: 15/01/2022
1. ĐẶT VẤN ĐỀ
Covid – 19 được thông báo lần đầu tiền xuất hiện tại Vũ Hán – Trung Quốc vào tháng 12 năm 2019, sau đó lan rộng ra toàn thế giới.
Chỉ tính riêng đến ngày 29/10/2020 đã có 44.351.506 trường hợp nhiễm bệnh trên toàn cầu trong đó có 1.171.253 người chết.
Tỷ lệ tử vong vào khoảng 0,5-1,0%. Tại Mỹ, từ ngày 01/3-30/5/2020 có tất cả
122.300 trường hợp chết do tất cả các nguyên nhân thì 95.235 (79%) có liên quan đến nhiễm Covid-19.
Trong cơ thể người thì ACE-2 là thụ thể chủ yếu cho Covid-19 xâm nhập vào các cơ quan và tổ chức trong đó các tế bào của tiểu phế quản phổi có độ nhạy và nhiễm cao nhất sau đó phải kể đến tế bào cơ tim, nội mạc mạch máu và một số tế bào khác.
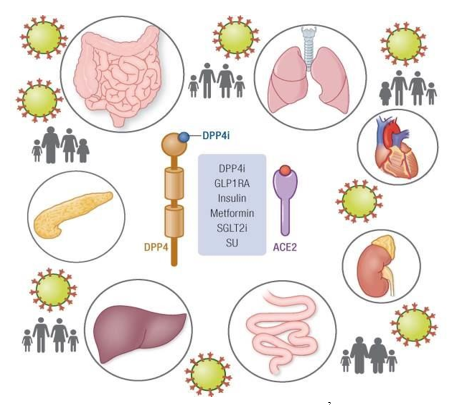
Hình 1. Các cơ quan covid – 19 có thể xâm nhập
Virut SARS-CoV-2 lan truyền từ người sang người chủ yếu qua giọt bắn của nước bọt. Sau nhiễm 5-6 ngày thì covid – 19 gây triệu chứng trên lâm sàng. Đa số SARS-CoV-2 có biểu hiện nhiễm trùng nhẹ trong thời gian đầu, trung bình 2 tuần tuy vậy cũng có những trường hợp tiến triển sang mức độ nặng với biểu hiện bởi hội chứng đáp ứng viêm hệ thống, hội chứng hô hấp cấp tối nguy hiểm (ARDS), tổn thương đa phủ tạng và shock. Những bệnh nhân có nguy cơ cao gây nhiễm covid-19 mức độ nặng hoặc tử vong bao gồm tuổi cao, nam giới, mắc bệnh mạn tính như bệnh tim mạch (CVD), béo phì, ĐTĐ típ 1 và 2. Đã có một số nghiên cứu công bố về sự kết hợp giữa bệnh tim mạch, ĐTĐ với covid-19 tại các trung tâm hồi sức tích cực. ĐTĐT2 đặc biệt ở người cao tuổi sẽ là yếu tố nguy cơ cao đối với nhiễm covid – 19, mặc dù đến nay cũng chưa hoàn toàn rõ về cơ chế.
1. Các cơ chế tiềm năng
Đái tháo đường và mức độ tăng glucose được xem như yếu tố độc lập liên quan đến mức độ nặng của bệnh cũng như gia tăng nguy cơ tử vong khi nhiễm covid – 19. Đặc biệt khi ĐTĐ đã xuất hiện biến chứng tim mạch, suy tim, bệnh thận mạn tính sẽ làm gia tăng đáng kể tỷ lệ tử vong do nhiễm covid-19. Một số giả thuyết về cơ chế dẫn đến tăng tỷ lê tử vong và tổn thương tim mạch sau nhiễm covid – 19 ở BN ĐTĐ có thể nêu như sau:
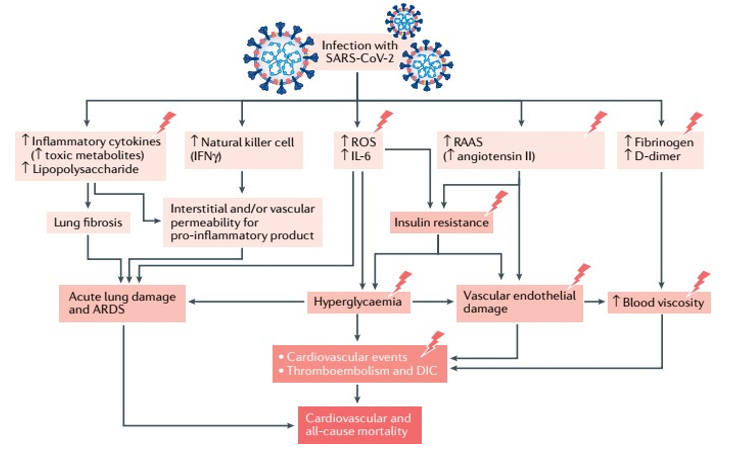
Hình 2. Một số cơ chế bệnh sinh tiềm năng ở BN ĐTĐT2 và covid-19
1.1. Covid-19 và chuyển hóa glucose
Trong tế bào bạch cầu đơn nhân của người, nồng độ glucose tăng sẽ làm gia tăng trực tiếp sự sao chép của SARS-CoV-2 và các cơ chất phân hủy glucose.
Sự sao chép SARS-CoV-2 dẫn đến phản ứng của oxi tại ty lạp thể đồng thời hoạt hóa yếu tố gây thiếu oxi 1α.
Bên cạnh đó, tăng glucose máu có thể tạo cho virut phát triển. Tóm lại tăng glucose máu hoặc đã mắc ĐTĐ sẽ trở thành yếu tố tiên lượng độc lập đối với bệnh suất và tử suất ở BN mắc SARS-CoV-2.
Sự phối hợp ĐTĐT2 với SARS-CoV-2 sẽ gây rối loạn đáp ứng miễn dịch dẫn đến tổn thương nặng hơn hoặc lan rộng tại phổi. Ở BN ĐTĐT2 nhiễm SARS-CoV-2 thường có diễn biến nặng hơn so với đối tượng không mắc ĐTĐ.
Kiểm soát kém glucose cũng là tiên lượng cho việc gia tăng cần thiết sử dụng thuốc và nhập viện cũng như tử vong.
Kiểm soát glucose kém là một biến chứng đặc trưng của covid-19 ở BN đã có suy giảm điều hòa glucose hoặc ĐTĐ. Ví dụ, nếu BN có chỉ định dùng insulin thì khi nhiễm SARS- CoV-2 sẽ làm gia tăng đáng kể liều lượng insulin (có thể lên đến 100 UI/ngày). Sự thay đổi về liều dùng insulin liên quan đến nồng độ của các cytokin gây viêm. Mặc dù nhiễm toan ceton là một biểu hiện đặc trưng liên quan với ĐTĐT1, song nếu BN nhiễm covid-19 thì nhiễm toan ceton có thể xuất hiện ở cả BN ĐTĐT2, thậm chí lên đến 77% trường hợp.
1.2. Viêm và kháng insulin
Đa số đối tượng tử vong do covid-19 đều nhận thấy có tổn thương lan tỏa tại các tiểu phế quản của phổi và xâm nhập các tế bào viêm với các màng hyalin nhô lên. Các tế bào cũng có đăc điểm viêm tương tự như tế bào cơ tim, xâm nhập tế bào lympho tại gan, tạo thành nhóm đại thực bào ở não, tổn thương dây thần kinh, xuất hiện vi tắc mạch ở cầu thận và tụy. Ở BN nhiễm covid-19 mức độ nặng quan sát thấy đáp ứng của interferon type 1 bị suy giảm đáng kể cùng với giảm hoạt tính của TNFα trong máu, biểu hiện tăng tải lượng virut trong máu và suy giảm đáp ứng viêm.
Một số BN covid-19 nặng xuất hiện cơn bão cytokin gây nguy hiểm và đe dọa tính mạng, cuộc sống. Nồng độ IL-6 và lactate dehydrogenase là yếu tố tiên lượng độc lập của BN nhiễm covid-19 nặng. IL-6 là yếu tố tiền viêm, nồng độ IL-6 có thể liên quan đến mức độ nặng của bệnh và tình trạng tiền đông máu. Thông qua sự gia tăng stress oxi hóa, IL- 6 có thể gây tổn thương protein, lipid và DNA, suy giảm cấu trúc và chức năng khác của cơ thể. Tất cả hiện tượng trên sẽ làm gia tăng tiến triển của covid-19 ở BN ĐTĐ. Để đánh giá tình trạng miễn dịch ở BN covid-19 nặng chủ yếu dựa vào tải lượng DNA của virut và lipopolysaccharide huyết tương.
Những thành phần này đều có tương quan thuận với nồng độ IL-6 huyết tương đồng thời là dấu ấn sinh học của tổn thương hô hấp tương tự như cơ chế bệnh sinh của nhiễm khuẩn huyết gây ra ARDS.
Một số cơ chế liên quan đến virut gây viêm làm gia tăng kháng insulin. Ví dụ virut gây viêm phổi như SARS và MERS thì các tế bào viêm lắng đọng trong phổi dẫn đến tổn thương phổi cấp tính, ARDS, và/hoặc tử vong. Những tế bào viêm có thể ảnh hưởng đến chức năng của cơ trơn và gan – đây là các cơ quan đáp ứng chủ yếu của insulin, chịu trách nhiệm phần lớn sự hấp thu của glucose thông qua chất trung gian là insulin.
Chính vì thế mà BN covid-19 mức độ nặng có biểu hiện yếu cơ và tăng hoạt độ các enzym gan đôi khi dẫn đến suy đa tạng với sự có mặt của dòng thác cytokin.
Covid-19 có thể dẫn đến ARDS khi đó đòi hỏi phải cho BN thở oxi áp lực dương và điều trị tích cực. ARDS đặc trưng bởi phù phổi nặng tại các vách phế nang, tiểu phế quản và nhu mô phổi cùng sự gia tăng các chỉ số viêm như CRP, tốc độ lắng hồng cầu. Bệnh nhân với covid-19 thường biểu hiện tăng các dấu ấn viêm khác như D-dimer, ferritin, IL-6 làm gia tăng nguy cơ biến chứng mạch máu nhỏ và lớn mà biến chứng mạch máu ở BN ĐTĐ lại liên quan có ý nghĩa với sự gia tăng nguy cơ tử vong nếu nhiễm covid-19.
Cơ chế sinh học phân tử của SARS-CoV-2 liên quan đến stress oxi hóa và viêm có thể dẫn đến tiến triển tương tự như trong nhiễm khuẩn huyết.
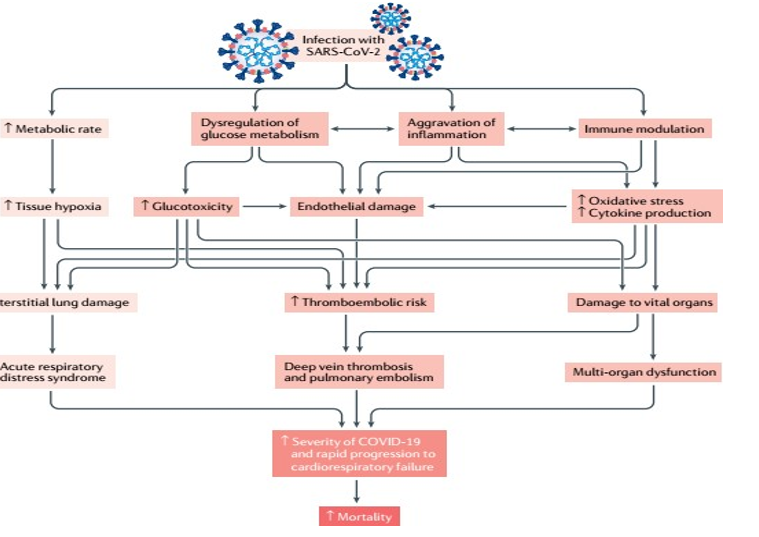
Hình 3. Tiến triển lâm sàng tiềm năng sau nhiễm SARS-CoV-2 ở BN ĐTĐ
1.3. Điều biến miễn dịch
Nhiễm covid-19 ở BN ĐTĐ cả típ 1 và 2 đều dẫn đến sự thay đổi chức năng của hệ miễn dịch. Tuổi là yếu tố nguy cơ gây ĐTĐT2 đồng thời cũng ảnh hưởng lên chức năng hệ miễn dịch có thể quan trọng tương đương đối với sự nhạy cảm và mức độ nặng của covid 19 gây ra. Tăng glucose máu có thể ảnh hưởng đến chức năng miễn dịch gây ra tình trạng rối loạn điều hòa miễn dịch và sau đó là sự xuất hiện biến chứng mạch máu lớn ở BN ĐTĐ. Đái tháo đường típ 2 liên quan đến rối loạn điều biến miễn dịch với xu hướng gia tăng theo tuổi và trở thành tiên lượng xấu ở BN khi nhiễm covid-19.
Ở đối tượng béo phì thì các cytokin tiền viêm bao gồm tế bào T hỗ trợ típ 1 có tác dụng làm tăng kháng insulin. Mặc dù vậy vai trò của cytokin trong covid-19 vẫn chưa rõ ràng. Nhiễm SARS-CoV-2 làm mất khả năng kiểm soát glucose ở BN và là nguy cơ tiến triển của bệnh hiện nay cơ chế cũng chưa rõ ràng. Nhiễm virut hô hấp cấp tính làm gia tăng INFγ- là một trong các chất gây kháng insulin ở cơ, do đó xuất hiện tình trạng cường tiết insulin để bù trừ nhằm duy trì nồng độ glucose máu ở mức bình thường và gia tăng đáp ứng của tế bào T – CD8 chống lại virut. Giả thuyết trên có thể xuất hiện ở đối tượng giảm dung nạp glucose hoặc ĐTĐ nhưng sự bù trừ đó có thể bị suy giảm. Cường insulin có thể làm gia tăng khả năng kháng virut thông qua kích thích trực tiếp chức năng của tế bào T – CD8. Khi nhiễm SARS-CoV-2 thì hệ miễn dịch chống lại virut và đáp ứng viêm có thể gây biến đổi độ nhạy cảm của insulin, xu hướng suy giảm quá trình chuyển hóa glucose.
Đối tượng rối loạn dung nạp glucose hoặc ĐTĐ có biểu hiện giảm hoạt tính của tế bào giết tự nhiên (NK), hiện tượng trên có thể giúp giải thích vì sao BN ĐTĐ tăng nhạy cảm với covid-19 và có tiến triển xấu hơn.
1.4. Renin–angiotensin–aldosterone system (RAAS)
Như đã nêu ở trên thì ACE2 là thụ thể để SARS-CoV-2 xâm nhập vào các cơ quan và tổ chức. Những nghiên cứu ban đầu cho thấy ACE2 được phân bố nhiều tại hệ hô hấp. Tuy vậy những nghiên cứu gần đây cho thấy rằng ACE2 có phân bố chủ yếu ở ruột non, thận, cơ tim, mạch máu và tụy song ở hệ hô hấp lại có phân bố hạn chế.
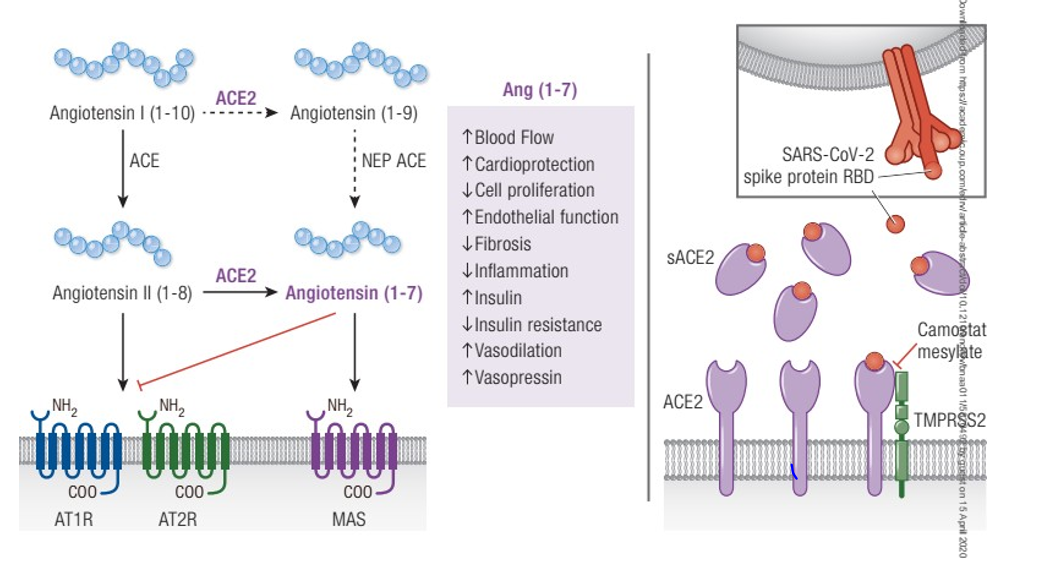
Hình 4. Mô hình coronavirut gắn với ACE2
Bằng chứng cho biết ACE2 phân bố ở nhiều tế bào và nhu mô tụy của người trong đó có tiểu đào tụy. Cũng có một số bằng chứng còn cho thấy có mối liên quan giữa ACE2 và điều hòa glucose. Nhiễm SARS-CoV-2 có thể gây tăng glucose ở BN trước đó không ghi nhận mắc ĐTĐ. ACE2 phân bố ở tuyến tụy nội tiết cùng với coronavirut có thể gây tổn thương đặc hiệu tiểu đảo, hậu quả làm tăng glucose.
Tăng glucose dường như tồn tại từ 3 năm trước khi phát hiện nhiễm SARS-CoV-2, do đó có thể đã gây tổn thương tế bào bêta tụy trong thời gian dài. Bằng chứng cho thấy ACE2 có thể gây ra sự phức tạp trong mối liên quan giữa covid-19 và ĐTĐ.
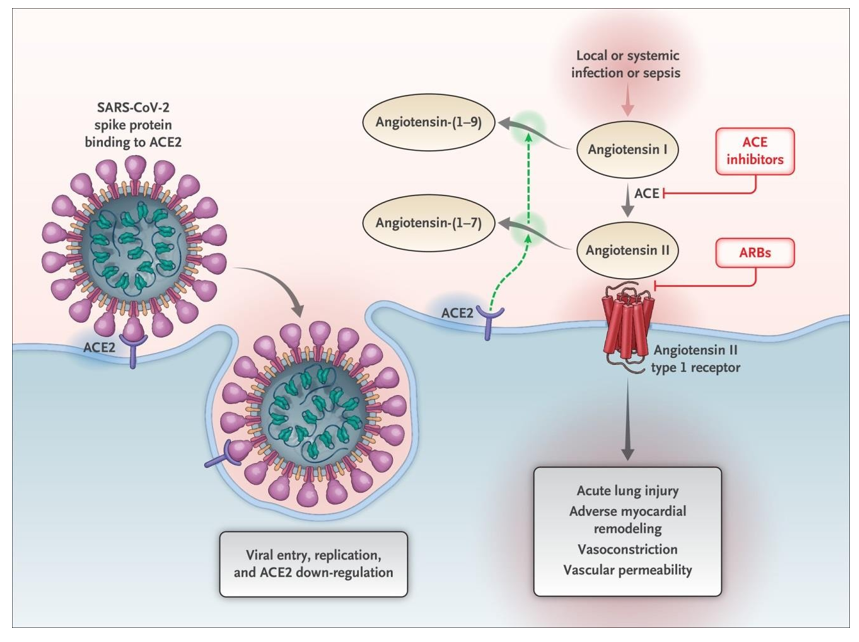
Hình 5. Tương tác giữa SARS-CoV-2 và RAAS
1.5. Mức độ nặng của bệnh nhân đái tháo đường nhiễm Covid-19
Hai nghiên cứu đầu tiên tại Mỹ cho thấy BN ĐTĐ nhiễm covid-19 phải nhập hồi sức tích cực tương ứng 58% và 33%. Sự phối hợp giữa covid -19 và ĐTĐ đã làm gia tăng mức độ nặng đồng thời của cả hai bệnh. Các biểu hiện gây nặng bệnh bao gồm tình trạng nhiễm độc glucose, tổn thương nội mạc do viêm, stress oxi hóa và các sản phẩm của cytokin đã làm tăng nguy cơ gây biến chứng, nghẽn – tắc mạch cũng như tổn thương các cơ quan quan trọng tương tự như ở BN ĐTĐ. Các thuốc thường sử dụng trong lâm sàng ở BN nhiễm Covid-19 như corticoid, thuốc kháng virut cũng có thể dẫn đến tăng glucose theo hướng không thuận lợi. Có nhiều cơ chế giải thích liên quan đến mức độ nặng của nhiễm Covid- 19 ở ĐTĐ.
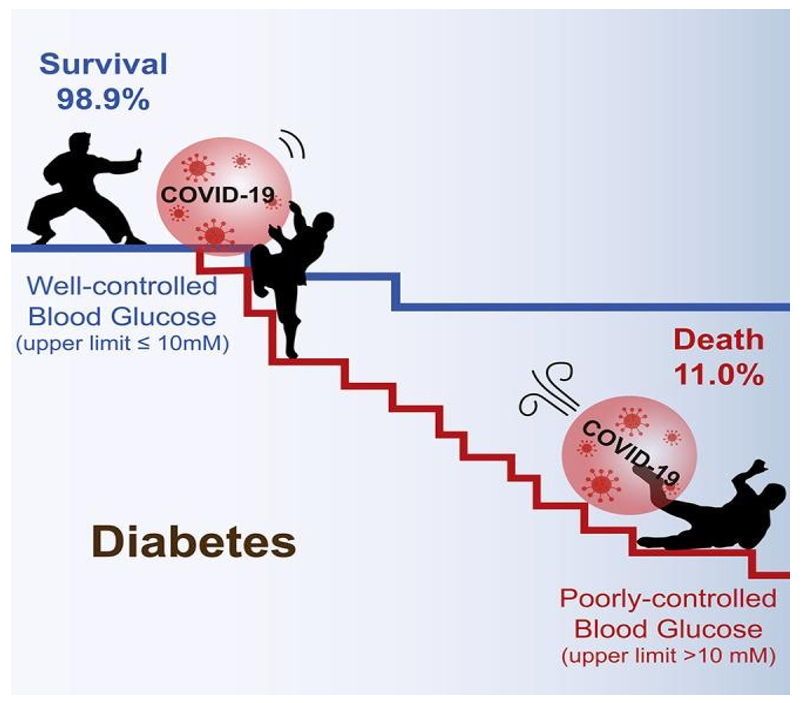
Hình 6. Liên quan tỷ lệ tử vong ở BN ĐTĐ nhiễm Covid-19
Nghiên cứu của các tác giả Trung Quốc cho thấy nếu glucose máu lúc đói tăng ≥ 7mmol/l tại thời điểm nhập viện là yếu tố độc lập gây tăng tỷ lệ tử vong ở BN nhiễm Covid- 19 không mắc ĐTĐ. Do đó theo dõi glucose máu thường xuyên và kiểm soát tốt glucose ở BN nhiễm Covid-19 sẽ giúp bệnh ít tiến triển đến mức độ nặng. Sử dụng corticoid nhóm dexamethasone có tác dụng giảm tỷ lệ tử vong ở bệnh nhân cần hô hấp hỗ trợ lên đến 36% so với 18% ở BN chỉ với hô hấp tự nhiên. Corticoid có tác dụng làm giảm nồng độ và hoạt tính của một số cytokin và dự phòng một số tác động bất lợi ở BN Covid-19 nặng.
2. Thuốc hạ glucose máu
Các thuốc thường sử dụng để hạ glucose trong điều trị ĐTĐ có thể tác động lên cơ chế bệnh sinh của Covid-19 và các tác dụng này có thể liên quan đến điều trị BN ĐTĐ và Covid-19.
2.1. Dipeptidyl peptidase -4 (DPP4)
Cũng tương tự như CD26 thì DPP4 là yếu tố quan trọng trong sự hằng định nội môi của glucose. Bên cạnh đó, DPP4 còn có tác dụng cần thiết đối với hệ miễn dịch như là một dấu ấn hoạt hóa lympho T và điều hòa sự trình diện một số chất hóa học. Ức chế DPP4 (DPP4s) thường sử dụng để hạ nồng độ glucose máu trong điều trị ĐTĐ.
Dựa vào những thông báo của BN nhiễm trùng đường hô hấp trên cho thấy có sự lo ngại về sự gia tăng nguy cơ nhiễm virut khi DPP4 bị ức chế. Tuy vậy giả thuyết trên chưa được minh chứng bởi các thử nghiệm lâm sàng. Mặc dù ACE2 được cho là thụ thể chủ yếu song DPP4 cũng có thể liên kết với SARS- CoV-2. Ức chế DPP4 có thể ảnh hưởng đến chức năng của DPP4 tương tự như thụ thể của virut song vấn đề này vẫn còn đang tranh luận. Sự trình diện của DPP4 tại lách, phổi, gan, thận và một số tế bào miễn dịch có thể bị biến đổi ở BN ĐTĐT2. Trong nghiên cứu vivo, sử dụng ức chế DPP4 như sitagliptin, vildagliptin hoặc saxagliptin không cản trở được sự xâm nhập của coronavirut vào trong tế bào. DPP4 và RAAS liên quan với nhau ở khía cạnh gen và liên quan với nguy cơ nhiễm SARS-CoV-2 và có thể làm nặng thêm Covid-19 nói riêng ở BN ĐTĐ. Mối liên quan trên được giải thích bởi sự trình diện DPP4 sẽ tăng lên ở tế bào lympho T ở BN ĐTĐT2 và liên quan với kháng insulin.
Sử dụng DPP4s sẽ làm tăng sự lưu hành các dấu ấn viêm trên chuột thực nghiệm song lại có tác dụng giảm hoạt tính DPP4 trên người, không làm tăng nồng độ các dấu ấn viêm.
Những hiểu biết hiện nay không khuyến khích theo khía cạnh có lợi liên quan đến sử dụng DPP4s ở BN ĐTĐT2 và Covid-19.
2.2. Glucagon – like – peptide 1 và đồng vận.
Bệnh nhân CVD hoặc thận có tiên lượng kém hơn so với những trường hợp không có biểu hiện tương tự. Những BN này cũng có nguy cơ cao hơn nhiễm SARS-CoV-2. Sử dụng đồng vận GLP-1 có tác dụng dự phòng CVD và bệnh thận trong đó có cả BN ĐTĐ. Khi nhiễm Covid-19 ở những đối tượng dư cân, béo phì sẽ có nhiều bất lợi do giảm khả năng chống viêm và giảm chức năng hệ miễn dịch. Đối tượng béo phì khi nhiễm Covid-19 sẽ có biểu hiện giảm khả năng dung nạp của phổi cũng như kết cục không tốt của sức khỏe nói chung. Những đặc điểm trên đều làm cho việc hỗ trợ hô hấp sẽ khó khăn hơn. Đồng vận GLP-1 có chỉ định dùng cho BN béo phì và ĐTĐT2 do thuốc có tác dụng giảm cân nặng dư thừa. Tuy vậy nếu BN có nhiễm trùng nặng như trong Covid-19 lại không được khuyên dùng bởi thuốc có tác dụng ngắn, rất lâu mới đạt nồng độ đỉnh và có thể gây nôn, buồn nôn. Tóm lại sử dụng đồng vận GLP-1 ở BN ĐTĐ với Covid-19 cũng cần thận trọng, cân nhắc.
2.3. Ức chế vận chuyển glucose kênh natri 2 (SGLT2)
Ức chế vận chuyển glucose kênh natri 2 tác dụng tại thận làm giảm nồng độ glucose, sử dụng để điều trị ĐTĐT2. SGLT2 làm giảm vận chuyển các tế bào viêm đến các mảng lắng đọng tại động mạch và giảm mức độ trình diện mRNA của một số cytokin và chất hóa học như TNFα, IL-6 và MCP1. Tuy vậy sử dụng ức chế SGLT2 có thể gây nhiễm toan ceton. Sử dụng ức chế SGLT2 đòi hỏi phải thật chi tiết, kỹ càng trong việc kiểm soát cân bằng dịch. Thuốc có tác dụng làm giảm tiến triển của bệnh, biến chứng và tử vong do tất cả các nguyên nhân kể cả ở BN ĐTĐ có nhiễm Covid-19.
2.4. Thiazolidinedione (TZD)
Sử dụng TZD có tác dụng dự phòng thứ phát đột quỵ não và những biến cố liên quan đến mạch máu mà BN SARS-CoV-2 dễ bị đột quỵ. Tuy vậy TZD có thể gây tăng cân, giữ nước, tiến triển của suy tim nếu đã mắc. Hiện tại chưa có các khuyến cáo về việc dùng TZD ở BN nhiễm Covid-19. Cần có những thử nghiệm lâm sàng để cân nhắc lợi – hại khi sử dụng TZD ở BN ĐTĐT2 nhiễm Covid-19.
3. Sử dụng thuốc hạ glucose
Các thuốc lựa chọn để hạ glucose ở BN ĐTĐT2 nhiễm Covid-19 có thể được sử dụng bao gồm DPP4s và đồng vận GLP-1 ở bệnh nhân có triệu chứng nhẹ hoặc vừa bởi vì cũng cần đề phòng tác dụng hạ glucose máu quá mức ở BN nằm viện kể cả ngoại trú.
Tuy vậy đa số các khuyến cáo cho việc lựa chọn thuốc hạ glucose ở BN ĐTĐT2 nhiễm Covid-19 lại thuộc về insulin đặc biệt khi bệnh ở mức độ nặng.
Tác dụng chống viêm của DPP4s và đồng vận GLP-1 cũng được khuyên dùng cho BN ĐTĐT2 nhiễm Covid-19 dựa vào kết quả của các thực nghiệm lâm sàng.
Dựa theo các chỉ định đã nêu thì đa số đều khuyên sử dụng insulin đối với những BN nguy kịch mắc ĐTĐT2 nhiễm Covid-19. Sử dụng insulin đường truyền tĩnh mạch để kiểm soát tối ưu glucose máu sẽ có tác dụng giảm nồng độ IL-6 và D-dimer.
Một nghiên cứu của các tác giả Trung Quốc cho thấy BN ĐTĐT2 nhiễm Covid-19 sử dụng metformin đã làm giảm tỷ lệ tử vong ở BN nằm viện so với nhóm không dùng (2,9% so với 12,3%) do metformin có tác dụng chống viêm nhờ vào việc giảm nồng độ các dấu ấn sinh học viêm. Nếu BN nặng thì không được dùng metformin. Bên cạnh đó cần phải bổ sung muối và nước cho phù hợp.
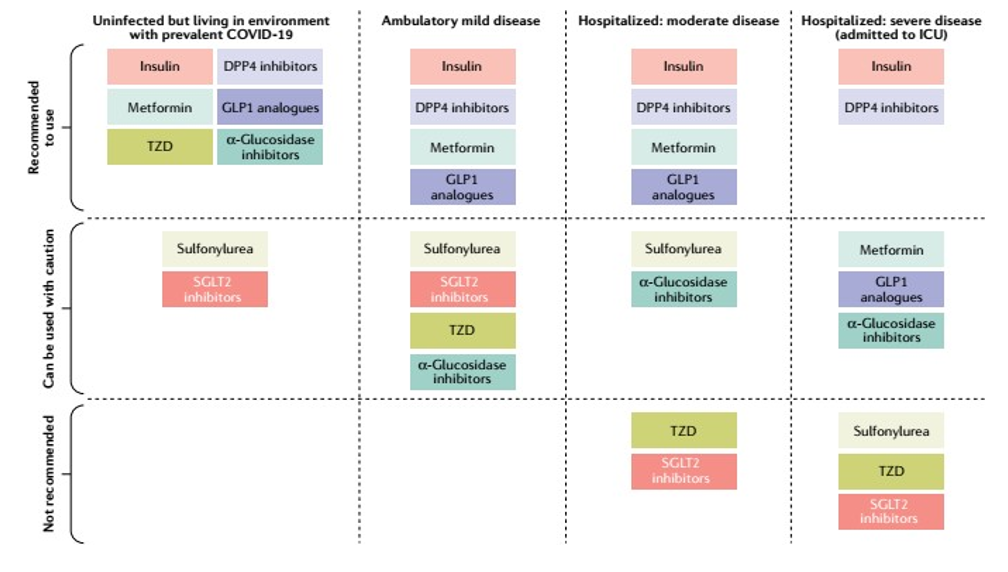
Hình 7. Sử dụng thuốc hạ glucose và BN ĐTĐ nhiễm Covid-19
4. KẾT LUẬN
Trong đại dịch Covid-19, BN ĐTĐ nếu nhiễm Covid-19 có thể biểu hiện tăng glucose máu. Nhiễm virut sẽ gây ảnh hưởng rất đáng kể lên kết quả điều trị ĐTĐ do biểu hiện rầm rộ của tình trạng viêm và thay đổi đáp ứng hệ miễn dịch dẫn đến khó khăn trong kiểm soát glucose. Nhiễm SARS-CoV-2 làm gia tăng nguy cơ nghẽn – tắc mạch và ảnh hưởng đến tim mạch, hô hấp với biểu hiện tương tự như suy chức năng ở BN ĐTĐ. Các cơ chế gây bệnh phối hợp với nhau làm cho BN ĐTĐ nhiễm Covid-19 có tiên lượng xấu. Kiểm soát glucose máu đạt mục tiêu cùng với việc điều trị các yếu tố nguy cơ tim mạch là nội dung quan trọng ở BN ĐTĐ nhiễm Covid-19. Các loại thuốc được sử dụng trong điều trị ĐTĐ và CVD dựa vào các biểu hiện tương ứng và nguy cơ cao của SARS-CoV-2. Sự phối hợp thuốc trong đó có dexamethazon và hydroxychloroquine có thể cho kết quả cao hơn so với nếu dùng đơn độc.
TÀI LIỆU THAM KHẢO
- Soo Lim, Jae Hyun Bae, Hyuk Sang Kwon, et al. (2021) “COVID-19 and diabetes mellitus: from pathophysiology to clinical management”. Nature Reviews Endocrinology, 17(1), pp.11-29.
- McGurnaghan SJ, Amanda Weir, Jen Bishop. et al (2021) “Risks of and risk factors for COVID-19 disease in people with diabetes: a cohort study of the total population of Scotland”. Lancet Diabetes Endocrinol, 9, pp. 82–93.
- Drucker DJ (2020), “Coronavirus Infections and Type 2 Diabetes-Shared Pathways with Therapeutic Implications”. Endocrine reviews 41, pp.457-469.
- Lihua Zhu 1, Zhi-Gang She 1, Xu Cheng, et al (2020), “Association of Blood Glucose Control and Outcomes in Patients with COVID-19 and Pre-existing Type 2 Diabetes”. Cell Metab 2;31(6), 1068-1077
- Vaduganathan M, Vardeny O, Pharm.D., et al (2020). “Renin– Angiotensin–Aldosterone System Inhibitors in Patients with Covid-19”. New Engl J Med, 382, pp.1653-1659.
- Ortiz A (2020) “Chronic kidney disease is a key risk factor for severe COVID-19: a call to action by the ERA-EDTA”. Nephrol Dial Transplant; 36 (1); pp.87-94.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam