Kiểu gen và kiểu hình của COVID-19 – Vai trò của chúng trong sinh bệnh học

Tổng quan
COVID-19 là một loại coronavirus mới với sự bùng phát của bệnh viêm phổi do virus bất thường ở Vũ Hán, Trung Quốc, và sau đó là đại dịch. Dựa trên mối quan hệ phát sinh loài và cấu trúc bộ gen, COVID-19 thuộc chi Betacoronavirus. Các Betacoronavirus ở người (SARS-CoV-2, SARS-CoV và MERS-CoV) có nhiều điểm tương đồng, nhưng cũng có sự khác biệt về cấu trúc gen và kiểu hình có thể ảnh hưởng đến quá trình sinh bệnh của chúng. COVID-19 chứa RNA sợi đơn (cảm nhận dương) liên kết với nucleoprotein trong capsid bao gồm protein nền. Một CoV điển hình chứa ít nhất sáu ORF trong bộ gen của nó. Tất cả các protein cấu trúc và phụ đều được dịch mã từ các sgRNA của CoV. Bốn protein cấu trúc chính được mã hóa bởi ORFs 10, 11 trên một phần ba bộ gen gần đầu cuối 3′. Cấu trúc di truyền và kiểu hình của COVID-19 trong sinh bệnh học là rất quan trọng. Bài viết này nêu bật tính năng quan trọng nhất của những tính năng này so với các Betacoronavirus khác.
Giới thiệu
Coronavirus có liên quan đến các bệnh ở người và động vật có xương sống. Coronavirus là thành viên của phân họ Coronavirinae trong họ Coronaviridae và bộ Nidovirales. Sự xuất hiện gần đây của một loại coronavirus mới với sự bùng phát của bệnh viêm phổi do virus bất thường ở Vũ Hán, Trung Quốc và sau đó bùng phát đại dịch là 2019-nCoV hoặc COVID-19. Dựa trên các mối quan hệ phát sinh loài và cấu trúc bộ gen, COVID-19 thuộc chi Betacoronavirus có sự tương đồng gần về trình tự của COVID19 với trình tự của coronavirus liên quan đến hội chứng hô hấp cấp tính nghiêm trọng (SARSr-CoV) và vi rút sử dụng ACE2 làm thụ thể xâm nhập -như SARS-CoV. Những điểm tương đồng này của SARS-CoV-2 với loại gây ra dịch SARS (SARS-CoVs) Nhóm Nghiên cứu Coronavirus của Ủy ban Quốc tế về Phân loại vi rút gọi vi rút là SARS-CoV-2. Sự hiểu biết về cấu trúc di truyền và kiểu hình của COVID-19 trong sinh bệnh học là rất quan trọng đối với việc sản xuất thuốc và vắc-xin. Vì vậy, trong bài viết đánh giá này, chúng tôi cung cấp các đặc điểm di truyền và kiểu hình mới nhất của COVID-19 để điều tra vai trò của hai yếu tố này trong quá trình sinh bệnh và so sánh nó với các gia đình của nó.
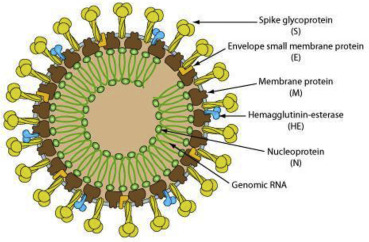
Hình 1. Sơ đồ của một coronavirus – Của Biowiki
Cấu trúc bộ gen của Coronavirus và vòng đời
COVID-19 là một hạt bao bọc hình cầu hoặc đa hình có chứa RNA sợi đơn (cảm nhận dương) liên kết với nucleoprotein trong capsid bao gồm protein nền. Lớp bì mang các dự báo glycoprotein hình câu lạc bộ. Một số coronavirus cũng chứa một protein hem agglutinin-esterase (HE).
Coronavirus sở hữu bộ gen lớn nhất (26,4–31,7 kb) trong số tất cả các virus RNA đã biết, với hàm lượng G + C thay đổi từ 32% đến 43%. Số lượng ORF nhỏ thay đổi hiện diện giữa các gen bảo tồn khác nhau (ORF1ab, cành, vỏ, màng và nucleocapsid) và, hạ nguồn gen nucleocapsid trong các dòng coronavirus khác nhau. Bộ gen của virus chứa các đặc điểm khác biệt, bao gồm một đoạn đầu N duy nhất bên trong protein đột biến. Các gen cho các protein cấu trúc chính trong tất cả các coronavirus xảy ra theo thứ tự 5′-3 ‘là S, E, M và N5.
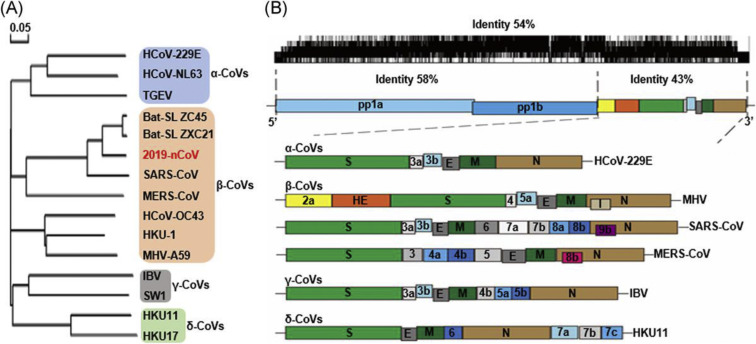
Hình 2. Cấu trúc bộ gen và cây phát sinh loài của coronavirus: A, cây phát sinh loài của các CoV đại diện, với coronavirus mới COVID-19 có màu đỏ. B, Cấu trúc bộ gen của bốn chi coronavirus: hai polypeptit dài 16 prôtêin không cấu trúc đã tiến hành từ đại diện Pp1a và pp1b. S, E, M và N đại diện cho bốn protein cấu trúc là gai, vỏ, màng và nucleocapsid. COVID-19; CoVs, coronavirus; HE, hemagglutinin-esterase. Tên virus: HKU, coronavirus do Đại học Hồng Kông xác định; HCoV, coronavirus ở người; IBV, vi rút viêm phế quản truyền nhiễm; MHV, vi rút viêm gan chuột; TGEV, vi rút viêm dạ dày ruột truyền nhiễm.
Một CoV điển hình chứa ít nhất sáu ORF trong bộ gen của nó. Ngoại trừ Gammacoronavirus có nsp1, ORFs đầu tiên (ORF1a / b), khoảng 2/3 chiều dài toàn bộ bộ gen, mã hóa 16 nsps (nsp1-16). ORF1a và ORF1b chứa một dịch chuyển khung ở giữa tạo ra hai polypeptit: pp1a và pp1ab. Các polypeptit này được xử lý bằng protease giống chymotrypsin được mã hóa bằng virus (3CLpro) hoặc protease chính (Mpro) và một hoặc hai protease giống papain thành 16 nsps. Tất cả các protein cấu trúc và phụ đều được dịch mã từ các sgRNA của CoV. Bốn protein cấu trúc chính chứa các protein gai (S), màng (M), vỏ (E) và nucleocapsid (N) được mã hóa bởi ORFs 10, 11 trên một phần ba bộ gen gần đầu tận cùng 3 ‘. Bên cạnh bốn protein cấu trúc chính này, các CoV khác nhau mã hóa các protein phụ và cấu trúc đặc biệt, chẳng hạn như protein HE, protein 3a / b và protein 4a / b (Hình 2B, bảng dưới). Những protein trưởng thành này chịu trách nhiệm cho một số chức năng quan trọng trong việc duy trì bộ gen và sao chép vi rút.
Có ba hoặc bốn protein virus trong màng coronavirus. Protein cấu trúc phong phú nhất là màng (M) glycoprotein; nó kéo dài lớp kép của màng ba lần, để lại một miền tận cùng NH2 ngắn bên ngoài virus và một đầu tận cùng COOH dài (miền tế bào chất) bên trong virion. Protein gai (S) như một glycoprotein màng loại I cấu tạo nên peplome. Trên thực tế, chất cảm ứng chính của kháng thể trung hòa là protein S. Giữa các protein vỏ có tồn tại một tương tác phân tử có thể xác định sự hình thành và thành phần của màng coronaviral. M đóng một vai trò chủ yếu trong sự hình thành nội bào của các phần tử vi rút mà không cần S. Khi có sự hiện diện của tunicamycin, coronavirus phát triển và tạo ra các virion không có gai, không có khả năng lây nhiễm, chứa M nhưng không có S.
So sánh SARS-CoV2 (COVID-19), SARS-CoV và MERS-CoV
5′UTR và 3′UTR tham gia vào các tương tác giữa và trong phân tử và có chức năng quan trọng đối với các tương tác RNA-RNA và liên kết với các protein của virus và tế bào. Ở đầu 5, Pb1ab là ORF đầu tiên của toàn bộ mã hóa chiều dài bộ gen protein không cấu trúc có kích thước 29844bp (7096aa), 29751bp (7073aa) và 30119bp (7078) trong COVID-19, SARS-CoV; và MERS-CoV, tương ứng. Ngay cả khi so sánh protein đột biến ở đầu 3 phút, giữa các coronavirus cụ thể là ba betacoronavirus này, sự khác biệt đã được hình dung, lần lượt là 1273aa, 21493aa và 1270aa ở COVID-19, SARS-CoV và MERS-CoV. Về mặt di truyền, COVID-19 ít giống với SARS-CoV (khoảng 79%) và MERS-CoV (khoảng 50%). Sự sắp xếp của protein nucleocapsid (N), protein vỏ (E) và protein màng (M) giữa các betacoronavirus là khác nhau như được mô tả trong Hình 3.
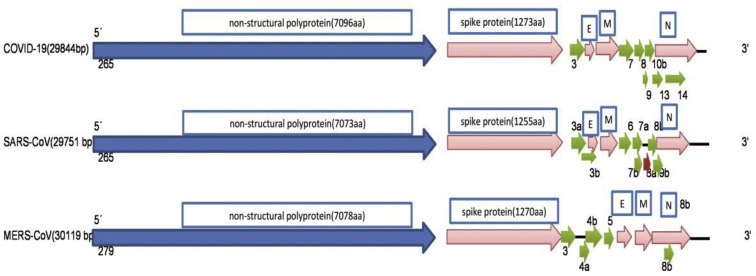
Hình 3. Vùng mã hóa 5 ′ UTR và 3 ′ UTR của COVID-19, SARS-CoV và MERS-CoV. Số lượng các cặp cơ sở giữa các betacoronavirus được hiển thị. Con số này được sửa đổi từ so sánh trình tự và tổ chức bộ gen của 2019-nCoV, 2020. Sự khác biệt trong cách sắp xếp của vỏ (E), màng (M) và nucleoprotein (N) giữa COVID-19, SARS-CoV, và MERS-CoV được hiển thị ở cuối 3 ′.
Vai trò của quá trình sao chép trong khả năng gây bệnh
SARS-CoV-2 (COVID-19) liên kết với ACE2 (men chuyển 2) bằng Spike của nó và cho phép COVID-19 xâm nhập và lây nhiễm các tế bào. Để vi rút hoàn toàn xâm nhập vào tế bào sau quá trình ban đầu này, protein đột biến phải được mồi bởi một loại enzyme gọi là protease. Tương tự như SARS-CoV, SARS-CoV-2 (COVID-19) sử dụng một protease gọi là TMPRSS2 để hoàn thành quá trình này. vì cần một protease (Hình 4)
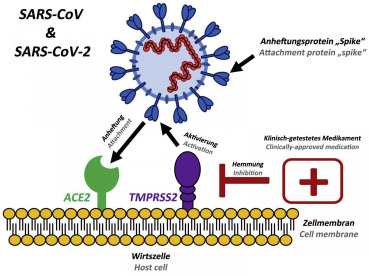
Hình 4. Protein đính kèm “tăng đột biến” của coronavirus mới COVID-19 vàSARS-CoV sử dụng cùng một yếu tố gắn kết tế bào (ACE2) và protease tế bào TMPRSS2 để kích hoạt chúng. Các loại thuốc hiện có, được phê duyệt lâm sàng chống lại TMPRSS2 ức chế sự lây nhiễm SARS-CoV-2 của các tế bào phổi.
Sau khi vi rút xâm nhập vào tế bào chủ và mở ra, bộ gen sẽ được phiên mã và sau đó được dịch mã. Sự sao chép và phiên mã bộ gen của coronavirus diễn ra ở màng tế bào chất và liên quan đến các quá trình phối hợp tổng hợp RNA liên tục và không liên tục, được thực hiện qua trung gian sao chép của virus, một phức hợp protein khổng lồ được mã hóa bởi gen sao chép 20 kb. Phức hợp sao chép được cho là bao gồm tối đa 16 tiểu đơn vị virus và một số protein tế bào. Bên cạnh các hoạt động RNA polymerase, RNA helicase và protease phụ thuộc vào RNA, thường gặp ở virus RNA, coronavirus replicase gần đây đã được dự đoán sử dụng nhiều loại enzyme xử lý RNA không (hoặc cực kỳ hiếm) được tìm thấy trong các virus RNA khác và bao gồm endoribonuclease xác định trình tự giả định, 3′-to-5 ′ exoribonuclease, 2′-O-ribose methyltransferase, ADP ribose 1′-phosphatase và, trong một tập hợp con coronavirus nhóm 2, hoạt động phosphodiesterase theo chu kỳ. Các protein được lắp ráp tại màng tế bào và RNA bộ gen được kết hợp khi hạt trưởng thành hình thành bằng cách nảy chồi từ màng tế bào bên trong.
Các yếu tố ảnh hưởng đến cơ chế bệnh sinh của vi rút
Các bệnh đồng mắc là bệnh tim mạch và mạch máu não cũng như bệnh tiểu đường. Một số bất thường cũng được quan sát thấy bao gồm suy giảm miễn dịch tế bào, kích hoạt đông máu, tổn thương cơ tim, tổn thương gan và thận, và nhiễm trùng thứ phát.16 Trong phần lớn các trường hợp bệnh nặng và tử vong, giảm bạch huyết và viêm kéo dài đã được ghi nhận. Đáng chú ý, những nhận xét này ở bệnh nhân COVID-19 tương tự như những người bị hội chứng hô hấp cấp tính nặng (SARS) trong đợt dịch năm 2003. Có thể có một cơ chế sinh học đằng sau sự bất thường dịch tễ học này.
Một số loại vắc-xin và thuốc kháng vi-rút dựa trên protein S đã được đánh giá trước đây. Du và cộng sự. Các vắc xin cho thấy có thể dựa trên protein S bao gồm protein S có chiều dài đầy đủ, vector virus, DNA, protein S tái tổ hợp và protein RBD tái tổ hợp. Xét thấy rằng, trong nghiên cứu in vitro, các liệu pháp kháng vi-rút được thiết kế dựa trên protein S bao gồm thuốc chẹn RBD-ACE2, chất ức chế phân cắt S, chất chẹn lõi dung hợp, kháng thể trung hòa, chất ức chế protease, chất ức chế protein S và RNA can thiệp nhỏ.18 Có một số các hợp chất tái tổ hợp như IFN với ribaverin chỉ có tác dụng hạn chế đối với nhiễm COVID-19.1 Vùng liên kết thụ thể của SARS-CoV-2 có ái lực cao hơn với ACE2, trong khi đó là ái lực thấp hơn đối với SARS-CoV. Enzyme chuyển mạch (ACE) và chất tương đồng của nó là ACE2, thuộc họ ACE của dipeptidylcarboxy dipeptidase. Tuy nhiên, chức năng sinh lý của chúng rất đa dạng. Mặt khác, ACE2 đóng vai trò là trang kết nối cho COVID-19. Dựa trên thông tin này, Gurwitz đề xuất sử dụng thuốc chẹn thụ thể angiotensin 1 (AT1R) có sẵn, chẳng hạn như losartan, làm phương pháp điều trị để giảm mức độ nghiêm trọng của nhiễm trùng COVID-19.20 Hiện tại, liệu pháp điều trị dựa trên việc xác định và phát triển các kháng thể đơn dòng đặc hiệu và hiệu quả chống lại COVID-19 kết hợp với remdesivir như một tiền chất tương tự nucleotide mới được sử dụng để điều trị bệnh do vi rút Ebola. Để hiểu được tốc độ lây lan của vi rút giữa người với người, điều quan trọng là phải tìm ra liệu COVID-19 có đột biến hay không để cải thiện khả năng liên kết của nó với các thụ thể của con người đối với sự lây nhiễm dựa trên tỷ lệ đột biến cao của nó. Bất kỳ sự thích ứng nào trong trình tự COVID-19 có thể làm cho nó truyền giữa người hiệu quả hơn cũng có thể làm tăng độc lực của nó. COVID-19 được cho là sẽ trở nên ít độc hơn khi truyền từ người sang người do tắc nghẽn di truyền đối với vi rút RNA thường xảy ra trong quá trình hô hấp truyền giọt.
Tổng kết
Hiện tại, không có phương pháp điều trị cụ thể cho COVID-19. Với tốc độ lây truyền cao của vi rút này giữa con người và các đại dịch của nó, điều quan trọng là phải xác định cơ sở sao chép, cấu trúc và khả năng gây bệnh của nó để tìm ra cách điều trị đặc biệt hoặc phòng ngừa. Do sự tương đồng cao của vi rút với các họ của nó, các nỗ lực đã được thực hiện để cung cấp thuốc và vắc xin cho COVID-19. Sự khác biệt về độ dài của gai khi nó dài hơn trong COVID-19 có thể đóng một vai trò quan trọng trong quá trình sinh bệnh và điều trị loại virus này. Tuy nhiên, việc xác định các chi tiết phân tử cụ thể của vi rút rất hữu ích trong việc đạt được các mục tiêu điều trị.
Nguồn tài trợ
Nghiên cứu này không nhận được bất kỳ khoản tài trợ cụ thể nào từ các cơ quan tài trợ trong khu vực công, thương mại hoặc phi lợi nhuận.
Tuyên bố về lợi ích cạnh tranh
Các tác giả tuyên bố không có xung đột lợi ích tiềm ẩn để tiết lộ.
Lời cảm ơn
Các tác giả xin gửi lời cảm ơn đến Trường Đại học Khoa học Y tế Shahrekord.
Tài liệu tham khảo
1 Y. Chen, Q. Liu, D. Guo
Emerging coronaviruses: genome structure, replication, and pathogenesis
J Med Virol, 92 (2020), pp. 418-423
2 I. Seah, R. Agrawal
Can the coronavirus disease 2019 (COVID-19) affect the eyes? A review of coronaviruses and ocular implications in humans and animals
Ocul Immunol Inflamm (2020), pp. 1-5
3. M. Cascella, M. Rajnik, A. Cuomo, S.C. Dulebohn, R. Di Napoli
Features, evaluation and treatment coronavirus (COVID-19)
StatPearls [Internet]
StatPearls Publishing (2020)
4 C.A.M. de Haan, L. Kuo, P.S. Masters, H. Vennema, P.J.M. Rottier
Coronavirus particle assembly: primary structure requirements of the membrane protein
J Virol, 72 (8) (1998), pp. 6838-6850
5 P.C.Y. Woo, Y. Huang, S.K.P. Lau, K.-Y. Yuen
Coronavirus genomics and bioinformatics analysis
Viruses, 2 (8) (2010), pp. 1804-1820
6 S. van Boheemen, M. de Graaf, C. Lauber, T.M. Bestebroer, V.S. Raj, A.M. Zaki, et al.
Genomic characterization of a newly discovered coronavirus associated with acute respiratory distress syndrome in humansmBio, 3 (6) (2012)
7 M. Czub, H. Weingartl, S. Czub, R. He, J. Cao
Evaluation of modified vaccinia virus Ankara based recombinant SARS vaccine in ferrets
Vaccine, 23 (17–18) (2005), pp. 2273-2279
8 D. Yang, J.L. Leibowitz
The structure and functions of coronavirus genomic 3′ and 5′ ends
Virus Res, 206 (2015), pp. 120-133
9 R. Lu, X. Zhao, J. Li, P. Niu, B. Yang, H. Wu, et al.
Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding
Lancet, 395 (10224) (2020), pp. 565-574
10 M. Hoffmann, H. Kleine-Weber, S. Schroeder, N. Krüger, T. Herrler, S. Erichsen, et al.
SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor
11 Y.-R. Guo, Q.-D. Cao, Z.-S. Hong, Y.-Y. Tan, S.-D. Chen, H.-J. Jin, et al.
The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak–an update on the status
Mil Med Res, 7 (1) (2020), pp. 1-10
12 I. Sola, F. Almazan, S. Zuniga, L. Enjuanes
Continuous and discontinuous RNA synthesis in coronaviruses
Ann Rev Virol, 2 (2015), pp. 265-288
13 J. Ziebuhr
The coronavirus replicase. Coronavirus replication and reverse genetics
Springer (2005), pp. 57-94
14 F. Almazán, M.L. DeDiego, C. Galán, D. Escors, E. Álvarez, J. Ortego, et al.
Construction of a severe acute respiratory syndrome coronavirus infectious cDNA clone and a replicon to study coronavirus RNA synthesis
15 K. McIntosh, J.S.M. Peiris
Coronaviruses. Clinical virology
(3rd ed.), American Society of Microbiology (2009), pp. 1155-1171
16 N. Chen, M. Zhou, X. Dong, J. Qu, F. Gong, Y. Han, et al.
Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study
Lancet, 395 (10223) (2020), pp. 507-513
17 C. Liu, Q. Zhou, Y. Li, L.V. Garner, S.P. Watkins, L.J. Carter, et al.
Research and development on therapeutic agents and vaccines for COVID-19 and related human coronavirus diseases
18 L. Du, Y. He, Y. Zhou, S. Liu, B.-J. Zheng, S. Jiang
The spike protein of SARS-CoV—a target for vaccine and therapeutic development
Nat Rev Microbiol, 7 (3) (2009), pp. 226-236
19 P. Prabakaran, X. Xiao, D.S. Dimitrov
A model of the ACE2 structure and function as a SARS-CoV receptor
Biochem Biophys Res Commun, 314 (1) (2004), pp. 235-241
20 D. Gurwitz
Angiotensin receptor blockers as tentative SARS-CoV-2 therapeutics
Drug Dev Res (2020), pp. 1-4, 10.1002/ddr.21656
21 T.P. Sheahan, A.C. Sims, R.L. Graham, V.D. Menachery, L.E. Gralinski, J.B. Case, et al.
Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses
Sci Transl Med, 9 (396) (2017)
22 M.A. Martinez
Compounds with therapeutic potential against novel respiratory 2019 coronavirus. Antimicrobial Agents and Chemotherapy
(2020)
Link bài gốc: Genotype and phenotype of COVID-19: Their roles in pathogenesis
theo LeilaMousavizadehaSorayyaGhasemibc
Bài viết được dịch thuật và sửa chữa bởi CLB Nội tiết trẻ trên DEMACVN.COM – Vui lòng không reup khi chưa được cho phép!
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam