XÁC ĐỊNH NỒNG ĐỘ VITAMIN D HUYẾT THANH VÀ CÁC KHOÁNG XƯƠNG KHÁC Ở BỆNH NHÂN SUY THẬN MẠN ĐANG ĐIỀU TRỊ LỌC MÀNG BỤNG NGOẠI TRÚ TẠI BỆNH VIỆN TRUNG ƯƠNG HUẾ
Phùng Thị Bảo Linh, Trần Đức Minh
Bệnh viện Trung ương Huế
DOI: 10.47122/vjde.2022.52.5
ABSTRACT
Determination of serum vitamin D and other bone mineral concentrations in out-patients with chronic renal failure was continuous ambulatory peritoneal dialysis at Hue Central Hospital
Objective: Determination of serum vitamin D and other bone mineral concentrations in out- patients with chronic renal failure was continuous ambulatory peritoneal dialysis. Methodology: Cross-sectional descriptive study of 40 out-patients with chronic renal failure are continuous ambulatory peritoneal dialysis at Hue Central Hospital from 5/2020 to 11/2021. Results and Conclusion: – The average 25(OH)D3 concentration in peritoneal dialysis patients was 18.76 ± 4.77 ng/mL, the lowest was 8.6 ng/mL and the highest was 31.2 ng/mL. According to the classification of KDIGO: 22.5% of patients was deficiency 25(OH)D3; 72.5% of patients was insufficiency 25(OH)D3. – The average serum adjusted total calcium concentration was: 2.21 ± 0.25 mmol/L, the lowest was 1.50 mmol/L and the highest was 2.71 mmol/L. According to the classification of KDIGO: decreased calcium: 35%, increased calcium: 2.5%, and normal was 62.5%. – The average serum phosphorus concentration was: 1.58 ± 0.48 mmol/L, the lowest was 0.61 mmol/L and the highest was 2.94 mmol/L. According to the classification of KDIGO: serum phosphorus decreased: 15%, phosphorus increased: 22.5%, normal phosphorus: 62.5%. – The average serum PTH concentration was: 724.63 ± 588.13 pg/mL, the lowest was 74.24 pg/mL and the highest was 2280 pg/mL. According to the classification of KDIGO: decreased serum PTH: 2.5%, increased PTH: 40% and normal PTH: 57.5%.
Key words: chronic renal failure, continuous ambulatory peritoneal dialysis, bone mineral.
TÓM TẮT
Mục tiêu: Xác định nồng độ vitamin D huyết thanh và các khoáng xương khác ở bệnh nhân suy thận mạn đang điều trị lọc màng bụng ngoại trú. Phương pháp và đối tượng nghiên cứu: Nghiên cứu mô tả cắt ngang gồm 40 bệnh nhân STM đang LMB ngoại trú tại Bệnh viện Trung ương Huế từ tháng 5/2020 đến tháng 11/2021. Kết quả và kết luận: Nồng độ 25(OH)D3 trung bình ở bệnh nhân LMB là 18,76 ± 4,77 ng/mL, thấp nhất là 8,6 ng/mL và cao nhất là 31,2 ng/mL. Theo phân loại của KDIGO: có 22,5% bệnh nhân thiếu 25(OH)D3; 72,5 % bệnh nhân không đầy đủ 25(OH)D3. – Nồng độ calci toàn phần hiệu chỉnh huyết thanh trung bình là: 2,21 ± 0,25 mmol/L, thấp nhất là 1,50 mmol/L và cao nhất là 2,71 mmol/L. Theo phân loại của KDIGO: calci giảm chiếm 35%, calci tăng 2,5%, bình thường chiếm tỷ lệ cao nhất là 62,5%. – Nồng độ phospho huyết thanh trung bình là: 1,58 ± 0,48 mmol/L, thấp nhất là 0,61 mmol/L và cao nhất là 2,94 mmol/L. Theo phân loại của KDIGO: Phospho huyết thanh giảm chiếm 15%, phospho tăng 22,5%, phospho bình thường 62,5%. – Nồng độ PTH huyết thanh trung bình là: 724,63 ± 588,13 pg/mL, thấp nhất là 74,24 pg/mL và cao nhất là 2280 pg/mL. Theo phân loại của KDIGO: PTH huyết thanh giảm chiếm 2,5%, PTH tăng 40% và PTH bình thường chiếm 57,5%.
Từ khóa: Suy thận mạn, lọc màng bụng liên tục, Vitamin D, khoáng xương
Tác giả liên hệ: Trần Đức Minh
Email: [email protected]
Ngày nhận bài: 03/03/2022
Ngày phản biện khoa học: 15/03/2022
Ngày duyệt bài: 30/03/2022
1. ĐẶT VẤN ĐỀ
Suy thận là sự giảm mức lọc cầu thận dưới mức bình thường. Suy thận được gọi là mạn tính khi mức lọc cầu thận giảm thường xuyên, cố định có liên quan đến sự giảm về số lượng nephron chức năng. Năm 2017, nghiên cứu NHANES-III đã đưa ra tỷ lệ bệnh thận mạn trong cộng đồng là 13%. Theo KDIGO 2012, tỷ lệ hiện mắc bệnh thận mạn trên toàn thế giới khoảng 10-16% dân số [1], [6]. Bản thân bệnh thận mạn sẽ dẫn đến nhiều rối loạn trong cơ thể như: ứ đọng các chất thải trong cơ thể, rối loạn cân bằng nội môi, rối loạn nội tiết… Các rối loạn nội tiết hay gặp như thiếu máu, tăng huyết áp, rối loạn chuyển hoá Calci, Phospho… Trong đó loạn dưỡng xương là một trong những rối loạn được nhắc đến từ lâu. Trong cơ chế bệnh sinh của loạn dưỡng xương ở bệnh nhân suy thận, rối loạn chuyển hóa vitamin D đóng một vai trò quan trọng. Vitamin D có vai trò kinh điển trong điều hòa chuyển hóa calci và còn có vai trò không kinh điển trong ảnh hưởng đến tăng sinh và biệt hóa tế bào [11]. Nồng độ vitamin D ở bệnh nhân suy thận có liên quan đến tiến triển của bệnh thận mạn tính, rối loạn khoáng chất và rối loạn xương (CKD-MBD), các biến cố tim mạch, trương lực cơ… Ở bệnh nhân bệnh thận mạn giai đoạn cuối được Lọc màng bụng, chủ yếu vẫn tồn tại suy giảm chức năng sản xuất ra men 1-α hydroxylase, tham gia chuyển hoá vitamin D, ngoài ra do cần hạn chế về chế độ ăn, giảm cảm giác thèm ăn và hạn chế các hoạt động ngoài trời nên làm giảm lượng vitamin D hấp thu và tổng hợp. Các dữ liệu cho thấy tỷ lệ bệnh nhân thẩm phân phúc mạc có nồng độ 25-OH-D3 huyết thanh <50 ng/mL lên tới 97%. Ngoài ra, giống như các sterol khác, vitamin D được vận chuyển trong huyết tương phần lớn gắn với protein, mà trong bệnh nhân suy thận giai đoạn cuối điều trị thẩm phân phúc mạc có sự mất protein qua quá trình lọc màng bụng. Vì vậy chúng tôi tiến hành thực hiện đề tài: “Xác định nồng độ vitamin D huyết thanh và các khoáng xương khác ở bệnh nhân suy thận mạn đang điều trị lọc màng bụng ngoại trú tại bệnh viện Trung ương Huế”.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Đối tượng nghiên cứu:
BN được chẩn đoán suy thận mạn giai đoạn cuối đang điều trị bằng phương pháp LMBLTNT tại khoa Nội thận – cơ xương khớp Bệnh viện Trung ương Huế từ 5/2020 đến tháng 11/2021.
2.2. Phương pháp nghiên cứu: Mô tả cắt ngang.
2.3. Phương pháp xử lý số liệu:
Số liệu được xử lý theo các phương pháp thông kê thông thường trong Y học với hỗ trợ của phần mềm Excel 2010, SPSS 16.0.
3. KẾT QUẢ
Qua nghiên cứu 40 bệnh nhân suy thận mạn đang lọc màng bụng liên tục ngoại trú tại Bệnh viện Trung ương Huế, chúng tôi rút ra được một số kết quả sau:
3.1. Dặc điểm chung của đối tượng nghiên cứu
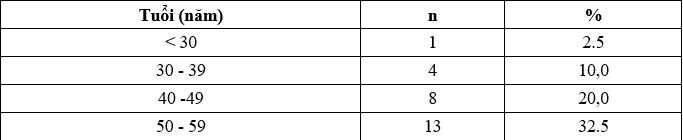
3.1.1. Phân bố bệnh nhân đang lọc màng bụng theo tuổi
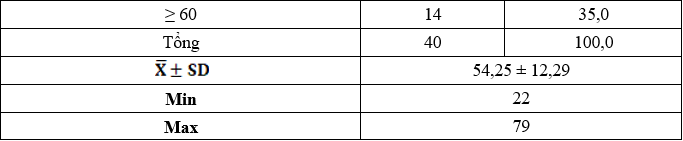
Bảng 3.1. Phân bố bệnh nhân suy thận mạn đang LMB theo tuổi
3.1.2. Phân bố bệnh nhân đang LMB theo giới
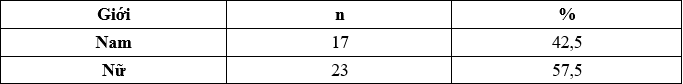
Bảng 3.2. Phân bố bệnh nhân đang LMB theo giới
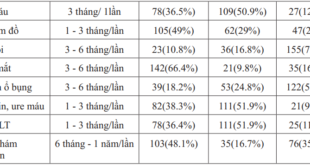
3.1.3. Tăng huyết áp ở bệnh nhân đang LMB
Bảng 3.3. Tăng huyết áp ở bệnh nhân đang LMB

3.1.4. Phân bố về BMI ở bệnh nhân đang LMB
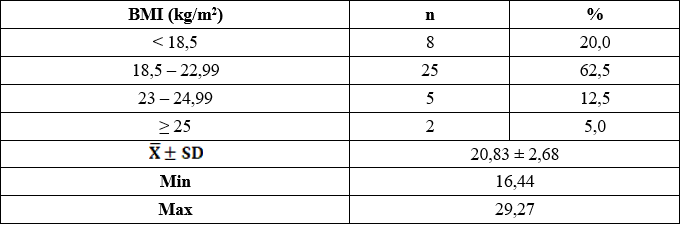
Bảng 3.4. Phân bố mức lọc cầu thận theo BMI
3.1.5. Phân bố bệnh nhân theo thời gian LMB
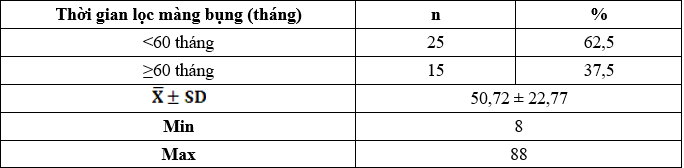
Bảng 3.5. Phân bố bệnh nhân theo thời gian LMB
3.2. Nồng độ 25(OH)D3 và các khoáng xương ở bệnh nhân LMB
3.2.1. Nồng độ trung bình 25(OH)D ở bệnh nhân LMB
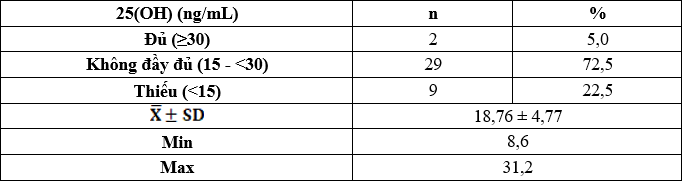
Bảng 3.6. Nồng độ trung bình 25(OH)D ở bệnh nhân LMB
3.2.2. Nồng độ calci toàn phần hiệu chỉnh ở bệnh nhân LMB
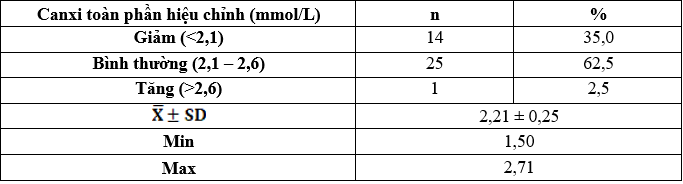
Bảng 3.7. Nồng độ calci toàn phần hiệu chỉnh ở bệnh nhân LMB
3.2.3. Nồng độ phospho ở bệnh nhân LMB
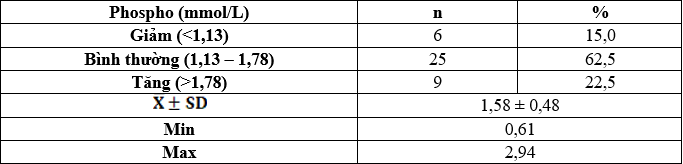
Bảng 3.8. Nồng độ phospho ở nhóm nghiên cứu
3.2.4. Nồng độ PTH ở bệnh nhân LMB
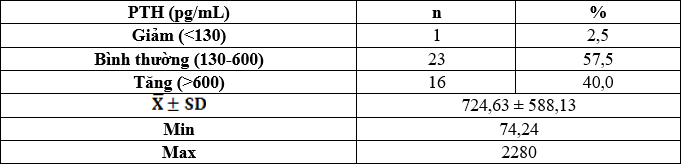
Bảng 3.9. Nồng độ PTH ở bệnh nhân LMB
4. BÀN LUẬN
4.1. Đặc điểm chung ở bệnh nhân LMB:
4.1.1. Đặc điểm bệnh nhân đang LMB theo tuổi:
Trong nghiên cứu của chúng tôi: Tuổi trung bình chung là: 54,25 ± 12,29 tuổi, tuổi thấp nhất 22 tuổi, cao nhất 79 tuổi. Tỷ lệ STM cao nhất ở nhóm tuổi ≥ 60 và thấp nhất ở nhóm tuổi <30 tuổi.
Trong nghiên cứu của Trần Đức Minh, tuổi trung bình chung: 48,20 ± 14,07, tuổi thấp nhất 21, cao nhất 76 tuổi. Tỷ lệ STM gia tăng dần theo độ tuổi, tỷ lệ mắc STM ở độ tuổi từ ≥ 60 chiếm tỷ lệ cao nhất 27,5 % và thấp nhất ở nhóm tuổi từ 30 – 39 (10%) [5]. Trong nghiên cứu của Nguyễn Thị Kim Hoa, độ tuổi trung bình trong nghiên cứu là 51,35 ± 16,94. Tỷ lệ STM trong nhóm tuổi cao nhất ở độ tuổi ≥ 60, chiếm tỷ lệ 35,48%. Độ tuổi STM chiếm tỷ lệ thấp nhất từ 30 – 39 tuổi; 12,9 % [2]. Nghiên cứu của Nguyễn Trung Hiếu: Tuổi trung bình của nhóm nghiên cứu là 45,85 ± 13,47 (năm), trong đó ít nhất là 20 tuổi, cao nhất là 77 tuổi. Đa số ở độ tuổi lao động (từ 20-59 tuổi, chiếm 83,7%) [3].
STM chiếm tỷ lệ cao nhất ở độ tuổi ≥ 60 tuổi vì theo thời gian thì MLCT giảm đi dần. Sau một thời gian, MLCT giảm đi 1ml/phút/năm (tính theo Creatinin). Giảm MLCT có liên quan đến biến chứng ở nhiều bệnh ở nhiều cơ quan: THA, thiếu dinh dưỡng, bệnh về xương, giảm hoạt động thể chất thường gặp người có độ tuổi > 60 tuổi, biến chứng của những bệnh này cũng gây ảnh hưởng đến MLCT.
4.1.2. Đặc điểm bệnh nhân đang LMB theo giới:
Trong nghiên cứu của chúng tôi: nữ chiếm tỷ lệ 57,5%, nam chiếm tỷ lệ 42,5%.
Trong nghiên cứu của Trần Đức Minh, tỷ lệ STM giữa nam/nữ là: nam chiếm tỷ lệ 55 %, cao hơn so với nữ 45% [5]. Theo nghiên cứu Nguyễn Thị Kim Hoa, tỷ lệ mắc STM ở nam và nữ tương đương nhau [2]. Nghiên cứu của Nguyễn Trung Hiếu ở 104 bệnh nhân có 58 bệnh nhân là nam giới chiếm tỷ lệ 55,8%, 46 bệnh nhân là nữ giới chiếm 44,2%, sự khác biệt này không có nghĩa thống kê [3]. Trong nghiên cứu của Taskapan [10], một nghiên cứu được tiến hành trên 273 bệnh nhân LMB thì tỷ lệ nam và nữ lần lượt là 54,9% và 45,1%. Tác giả Wang [13], nghiên cứu trên 230 bệnh nhân LMB tại Hong-Kong thì thấy tỷ lệ bệnh nhân nam là 51,3%, tỷ lệ bệnh nhân nữ là 48,7%.
Sự khác biệt về tỷ lệ giữa hai giới mắc STM của các nghiên cứu là khác nhau và khác với chúng tôi có thể là do lấy các đối tượng bệnh nhân khác nhau về địa lý và mức độ STM.
4.1.3. Đặc điểm tăng huyết áp ở bệnh nhân đang LMB:
Tăng huyết áp là triệu chứng thường gặp ở bệnh nhân LMB, trong nhiều trường hợp khó có thể phân định rõ ràng là THA gây suy thận mạn hay là biến chứng của suy thận. Tăng huyết áp gặp từ 50-75% bệnh nhân có MLCT <60ml/phút/1,73m2 và trên 80% bệnh nhân lọc máu chu kỳ và khoảng 50% bệnh nhân LMB. Tăng huyết áp kéo dài gây phì đại thất trái, xơ vữa động mạch và các biến chứng tim mạch khác [9].
Trong nghiên cứu của chúng tôi: THA chiếm tỷ lệ cao 62,5%, không THA chiếm tỷ lệ 37,5%.
Trong nghiên cứu của Trần Đức Minh: STM có THA chiếm tỷ lệ cao 87,5 %, không THA chiếm tỷ lệ 12,5%. THA độ 1 chiếm tỷ lệ cao nhất 62,5% [5]. Nghiên cứu của Nguyễn Trung Hiếu có tỷ lệ tăng huyết áp cao, chiếm 56,7%, trong đó 46.2% THA độ 1, 8,7% THA độ 2, 1,9% THA độ 3. Như vậy, đa phần các bệnh nhân không được kiểm soát được huyết áp. Điều này có thể liên quan đến tình trạng THA kháng trị ở nhóm bệnh nhân suy thận mạn tính giai đoạn cuối [3].
4.1.4. Phân bố về BMI ở bệnh nhân LMB:
Trong nghiên cứu của chúng tôi BMI trung bình là: 20,83 ± 2,68 kg/m2, thấp nhất là 16,44 kg/m2, cao nhất là 29,27 kg/m2. Kết quả nghiên cứu của chúng tôi tương tự nghiên cứu của Nguyễn Trung Hiếu cho thấy BMI trung bình là 20,46 ± 2,08 (kg/m2), trong 104 bệnh nhân nghiên cứu có 73 bệnh nhân (chiếm 70,2%) có BMI nằm trong giới hạn bình thường, chỉ có 16 bệnh nhân nhẹ cân chiếm tỷ lệ 15,4%. Xét chung cả ba nhóm bệnh nhân thì có 15 bệnh nhân thừa cân và béo phì (chiếm 14,4%), không có sự khác biệt có ý nghĩa giữa các nhóm [3].
Nghiên cứu của tác giả Taskapan [10], các đối tượng nghiên cứu có BMI trung bình là 26,1 ± 4,4 (kg/m2), trong nghiên cứu năm 2008 của tác giả Wang [13] tại Hong-Kong, BMI trung bình của các đối tượng nghiên cứu là 23,1 ± 3,4 (kg/m2).
Kết quả về BMI của các tác giả nước ngoài đều cao hơn so với nghiên cứu của chúng tôi, sự khác nhau này có thể là do sự chênh lệch về điều kiện kinh tế, tình trạng dinh dưỡng cũng như đặc điểm về chủng tộc.
4.1.5. Phân bố bệnh nhân theo thời gian LMB:
Trong nghiên cứu của chúng tôi, thời gian LMB trung bình của nhóm nghiên cứu là: 50,72 ± 22,77 (tháng) (4,23 ± 1,90 năm) trong đó LMB ngắn nhất là 8 tháng và lâu nhất là 88 tháng, đa số bệnh nhân có thời gian LMB <5 năm (chiếm 62,5%).
Nghiên cứu Nguyễn Trung Hiếu cho thấy thời gian LMB trung bình của đối tượng nghiên cứu là 6,47 ± 3,67 năm, đa số các bệnh nhân có thời gian LMB từ 1-10 năm, chiếm 81,7% [3]. So sánh với các tác giả khác thấy rằng đối tượng nghiên cứu của chúng tôi có thời gian LMB dài hơn Jamal S. Alwakeel [7] là 2,29 ± 3,5 năm, Wang [13] là 2,2 (1,2 – 4,2) năm. Chúng tôi cho rằng sự khác nhau này do tính chất ngẫu nhiên của việc lựa chọn mẫu nghiên cứu.
4.2. Đặc điểm nồng độ 25 (OH)D3 và các khoáng xương ở bệnh nhân đang LMB
4.2.1. Đặc điểm 25(OH)D3 ở bệnh nhân LMB:
Tình trạng thiếu hụt vitamin D huyết thanh có liên quan chặt chẽ với tỷ lệ tử vong sớm ở bệnh nhân LMB [50]. Nghiên cứu của chúng tôi cho thấy: Nồng độ 25(OH)D3 trung bình của nhóm nghiên cứu là 18,76 ± 4,77ng/mL, thấp nhất là 8,6ng/mL và cao nhất là 31,2ng/mL. Nhóm đủ 25(OH)D3 chiếm: 5%, nhóm thiếu 25(OH)D3 chiếm: 22,5% và nhóm không đầy đủ 25(OH)D3 chiếm: 72,5%
Nghiên cứu của Nguyễn Trung Hiếu tiến hành định lượng 25(OH)D3 trên 104 bệnh nhân LMBLLNT, kết quả nghiên cứu cho thấy nồng độ 25(OH)D3 trung bình ở bệnh nhân CAPD là 23,43 ± 7,39 (ng/mL) (58,57 ± 18,46 nmol/L), thấp hơn so với giá trị tham chiếu bình thường [3]. Trên thế giới, nghiên cứu của Wang [13] năm 2008 trên 230 bệnh nhân LMB cho thấy nồng độ 25(OH)D3 trung bình là 45,7 nmol/L (35,7 – 60,7 nmol/L). Nghiên cứu của Jamal S. Alwakeel[7] năm 2014 tìm hiểu nguy cơ thiếu vitamin D ở bệnh nhân LMB cho thấy nồng độ 25(OH)D3 là 16,1 ± 8,23 nmol/L.
Nghiên cứu của Sanjay Vikrant, Anupam Parashar ở 462 bệnh nhân CKD giai đoạn 3- 5D cho thấy: 25(OH)D3 được thực hiện ở 335 (72,5%) bệnh nhân và 90,4% được phát hiện là thiếu vitamin D.
Mức 25(OH)D3 gợi ý tình trạng thiếu vitamin D trầm trọng ở 33,7%, thiếu vitamin D ở 45,4% và không đầy đủ vitamin D ở 11,3% bệnh nhân [12].
Có sự khác nhau như vậy là do các đối tượng nghiên cứu của các tác giả là khác nhau về sắc tộc, tôn giáo, địa lý cũng như tình trạng bổ sung vitamin D ở bệnh nhân lọc màng bụng theo chỉ định của bác sĩ…
Theo nghiên cứu về tình trạng vitamin D trong cộng đồng người Việt Nam năm 2011 cùa tác giả Hồ Phạm Thục Lan [8], cho thấy nồng độ 25(OH)D ở nam giới là 36,8 ± 10,2 (ng/mL), ở nữ giới là 30,1 ± 5,9 (ng/mL). Như vậy có thể thấy nồng độ 25(OH)D ở bệnh nhân LMB thấp hơn so với người khỏe mạnh.
4.2.2. Đặc điểm rối loạn chuyển hóa calci- phospho, PTH ở bệnh nhân LMB:
Nghiên cứu của chúng tôi cho thấy: Nồng độ calci toàn phần hiệu chỉnh là: 2,21 ± 0,25mmol/L, thấp nhất là 1,50mmol/L và cao nhất là 2,71mmol/L.
Nhóm có nồng độ calci toàn phần hiệu chỉnh giảm chiếm 35%, bình thường chiếm tỷ lệ cao nhất là 62,5%, nhóm tăng calci toàn phần hiệu chỉnh chiếm tỷ lệ thấp nhất là 2,5%. Nồng độ phospho trung bình là: 1,58 ± 0,48mmol/L, thấp nhất là 0,61mmol/L và cao nhất là 2,94mmol/L.
Phospho máu giảm chiếm 15%, bình thường chiếm 62,5% và tăng chiếm 22,5%. Nồng độ PTH trung bình là: 724,63 ± 588,13pg/mL, thấp nhất là 74,24pg/mL và cao nhất là 2280pg/mL.
Giảm PTH chiếm 2,5%, bình thường chiếm 57,5% và tăng chiếm 40%.
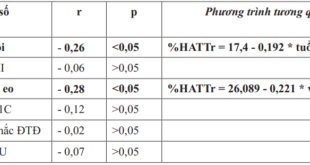
Nghiên cứu Nguyễn Thị Huyên, Đỗ Gia Tuyển, Đinh Thị Kim Dung cho thấy có mối tương quan nghịch mức độ vừa giữa nồng độ PTH với mức lọc cầu thận (r = – 0,422). Chứng tỏ mức lọc cầu thận càng giảm (suy thận càng nặng) thì nồng độ PTH máu càng tăng [4].
Nghiên cứu của Sanjay Vikrant, Anupam Parashar ở 462 bệnh nhân CKD giai đoạn 3- 5D cho thấy: Tần suất các bất thường sinh hóa khác nhau là hạ calci máu (23,8%), tăng calci máu (5,4%), giảm phosphat máu (2,8%), tăng phosphat máu (55,4%), cường cận giáp thứ phát (82,7%), và suy tuyến cận giáp (1,5 %). Khoảng 70,6% bệnh nhân có mức iPTH trên phạm vi mục tiêu của sáng kiến chất lượng kết quả bệnh thận (KDOQI).
CKD không tiểu đường so với CKD tiểu đường có iPTH cao hơn (p = 0,001), tỷ lệ bệnh nhân có iPTH trên phạm vi mục tiêu KDOQI cao hơn (p = 0,09) [12].
Có sự khác nhau về đặc điểm rối loạn chuyển hóa calci, phospho, PTH ở các nghiên cứu có là do sự khác nhau về biện pháp điều trị, số lượng bệnh, đặc điểm chủng tộc, chế độ ăn uống vận động thể lực cũng như tình trạng bổ sung vitamin D3, calci…
5. KẾT LUẬN
Qua nghiên cứu nồng độ vitamin D và các khoáng xương khác của 40 bệnh nhân suy thận mạn đang LMB từ tháng 5/2020 đến 11/2021 tại khoa Nội Thận Bệnh viện Trung ương Huế. Chúng tôi có một số kết luận sau:
- Nồng độ 25(OH)D3 trung bình ở bệnh nhân LMB là 18,76 ± 4,77 ng/mL, thấp nhất là 8,6 ng/mL và cao nhất là 31,2 ng/mL. Theo phân loại của KDIGO: có 22,5% bệnh nhân thiếu 25(OH)D3; 72,5 % bệnh nhân không đầy đủ 25(OH)D3
- Nồng độ calci toàn phần hiệu chỉnh huyết thanh trung bình là: 2,21 ± 0,25 mmol/L, thấp nhất là 1,50 mmol/L và cao nhất là 2,71 mmol/L. Theo phân loại của KDIGO: calci giảm chiếm 35%, calci tăng 2,5%, bình thường chiếm tỷ lệ cao nhất là 62,5%.
- Nồng độ phospho huyết thanh trung bình là: 1,58 ± 0,48 mmol/L, thấp nhất là 0,61 mmol/L và cao nhất là 2,94 mmol/L. Theo phân loại của KDIGO: Phospho huyết thanh giảm chiếm 15%, phospho tăng 22,5%, phospho bình thường 62,5%.
- Nồng độ PTH huyết thanh trung bình là: 724,63 ± 588,13 pg/mL, thấp nhất là 74,24 pg/mL và cao nhất là 2280 pg/mL. Theo phân loại của KDIGO: PTH huyết thanh giảm chiếm 2,5%, PTH tăng 40% và PTH bình thường chiếm 57,5%.
TÀI LIỆU THAM KHẢO
- Bộ môn Nội, Đại học y dược Huế (2013), “ Suy thận mạn”, Bài giảng Bệnh học nội khoa tập 2, Nhà xuất bản Y học, 67-75.
- Nguyễn Thị Kim Hoa (2011), “Nghiên cứu sự biến đổi các chỉ số huyết áp, protein niệu đêm/ngày ở bệnh nhân suy thận mạn”, Y học thực hành, 756(3), 41-123.
- Nguyễn Trung Hiếu (2020), Nghiên cứu nồng độ vitamin D huyết thanh ở bệnh nhân lọc màng bụng liên tục ngoại trú, Luận văn thạc sỹ Y học, Đại học Y Hà Nội.
- Nguyễn Thị Huyền, Đỗ Gia Tuyển, Đinh Thị Kim Dung (2009), “Nghiên cứu tình trạng cường tuyến cận giáp trạng thứ phát và tìm hiểu một số yếu tố liên quan ở bệnh nhân suy thận mạn chưa điều trị thay thế”, Y học lâm sàng, (39) 37-41.
- Trần Đức Minh (2014), Nghiên cứu nồng độ Lp -PLA2 huyết tương ở bệnh nhân suy thận mạn đang lọc màng bụng liên tục ngoại trú tại bệnh viện Trung ương Huế, Luận văn thạc sỹ Y học, Đại học Y dược Huế.
- Võ Tam (2012), “Suy thận mạn”, Giáo trình nội khoa sau đại học bệnh thận – tiết niệu, Nhà xuất bản Đại học Huế, 298-317.
- Alwakeel JS, Usama S, Mitwalli AH, et al (2014), “Prevalence of vitamin D deficiency in peritoneal dialysis patients”, Saudi J Kidney Dis Transpl, 25(5), pp. 981-985.
- Ho-Pham TL, Nguyen ND, Lai TQ, Eisman JA, Nguyen TV (2011), “Vitamin D status and parathyroid hormone in a urban population in Vietnam”, Osteoporos Int, 22(1), pp. 241-248.
- Levey AS, Eckardt K-U, Tsukamoto Y, et al (2005), “Definition and classification of chronic kidney disease: a position statement from Kidney disease: Improving Global Outcomes (KDIGO)”, Kidney int, 67(6), pp. 2089-2100.
- Taskapan H, Ersoy FF, Passadakis PS, et al (2006), “Severe vitamin D deficiency in chronic renal failure patients on peritoneal dialysis”, Clin Nephrol, 66(4), pp. 247-255.
- Tepper S, Shahar D, Geva D, Avizohar O, Nodelman M, Segal E et al (2014), “Identifying the threshold for vitamin D insufficiency in relation to cardiometabolic markers”, Nutrition, Metabolism and Cardiovascular Diseases, 24(5), pp. 489-494.
- Vikrant and A. Parashar (2016), “Prevalence and severity of disordered mineral metabolism in patients with chronic kidney disease: A study from a tertiary care hospital in India”, Indian J Endocrinol Metab, 20(4), pp. 460-467.
- Wang AY-M, Lam CW-K, Sanderson JE, et al (2008), “Serum 25 hydroxyvitamin D status and cardiovascular outcomes in chronic peritoneal dialysis patients: a 3-y prospective cohort study”, Am J Clin Nutr, 87(6), pp. 1631-1638.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam