LIỆU PHÁP CHỐNG ĐAU TRONG BỆNH THẦN KINH NGOẠI BIÊN DO ĐÁI THÁO ĐƯỜNG
Nguyễn Đình Toàn
Trường Đại học Y Dược Huế
DOI: 10.47122/vjde.2021.46.7
TÓM TẮT
Đau trong Bệnh lý thần kinh ngoại biên do đái tháo đường xảy ra ở khoảng 25% bệnh nhân đái tháo đường và ảnh hưởng đáng kể đến chất lượng cuộc sống. Nó thường gây ra đau rát, dị cảm và tê kiểu mang găng, mang vớ tiến triển từ bàn chân và bàn tay. Các bác sĩ lâm sàng nên xem xét cẩn thận mục tiêu và tình trạng chức năng của bệnh nhân và các tác dụng phụ có thể xảy ra của thuốc khi lựa chọn phương pháp điều trị đau trong bệnh thần kinh ngoại biên do Đái tháo đường. Pregabalin và Duloxetine là những loại thuốc duy nhất được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ phê duyệt để điều trị chứng đau này. Dựa trên các hướng dẫn thực hành hiện tại, những loại thuốc này cộng với Gabapentin và Amitriptyline, nên được xem xét để điều trị ban đầu. Liệu pháp thứ hai bao gồm các loại thuốc giống Opioid (tramadol và tapentadol), Venlafaxine, Desvenlafaxine và các chất bôi ngoài da (miếng dán Lidocain và kemCapsaicin). Isosorbide dinitrate dạng xịt và kích thích dây thần kinh qua da có thể giúp giảm đau ở một số bệnh nhân và có thể được xem xét tại bất kỳ thời điểm nào trong quá trình điều trị. Opioid và thuốc ức chế tái hấp thu serotonin có chọn lọc là những loại thuốc thứ ba không bắt buộc. Châm cứu, y học cổ truyền Trung Quốc, axit alpha lipoic, acetyl-l- carnitine, dầu hoa anh thảo và trường điện từ thiếu bằng chứng chất lượng cao để hỗ trợ việc sử dụng trong điều trị đau ở bệnh nhân bệnh thần kinh ngoại biên do ĐTĐ
Từ khóa: liệu pháp, đau, bệnh thần kinh ngoại biên, đái tháo đường
SUMMARY
Management of painful peripheral diabetic neuropathy
Nguyen Dinh Toan
Hue University of Medicine and Pharmacy
Painful diabetic peripheral neuropathy occurs in approximately 25% of patients with diabetes mellitus who are treated in the office setting and significantly affects quality of life. It typically causes burning pain, paresthesias, and numbness in a stocking-glove pattern that progresses proximally from the feet and hands. Clinicians should carefully consider the patient’s goals and functional status and potential adverse effects of medication when choosing a treatment for painful diabetic peripheral neuropathy. Pregabalin and duloxetine are the only medications approved by the U.S. Food and Drug Administration for treating this disorder. Based on current practice guidelines, these medications, with gabapentin and amitriptyline, should be considered for the initial treatment. Second- line therapy includes opioid-like medications (tramadol and tapentadol), venlafaxine, desvenlafaxine, and topical agents (lidocaine patches and capsaicin cream). Isosorbide dinitrate spray and transcutaneous electrical nerve stimulation may provide relief in some patients and can be considered at any point during therapy. Opioids and selective serotonin reuptake inhibitors are optional third-line medications. Acupuncture, traditional Chinese medicine, alpha lipoic acid, acetyl-l-carnitine, primrose oil, and electromagnetic field application lack high- quality evidence to support their use.
Keywords: management, pain, peripheral diabetic neuropathy
Chịu trách nhiệm chính: Nguyễn Đình Toàn Ngày nhận bài: 09/01/2021
Ngày phản biện khoa học: 09/02/2021 Ngày duyệt bài: 01/04/2021
Email: [email protected], [email protected]
Điện thoại: 0914000066
1. KHÁI QUÁT VỀ ĐAU TRONG BỆNH THẦN KINH NGOẠI BIÊN DO ĐÁI THÁO ĐƯỜNG
1.1. Tổng quan
Theo thống kê năm 2020 đăng trên tạp chí Endocrine and Metabolic Science, bệnh thần kinh ngoại biên chiếm tỷ lệ 40,3%, ở bệnh nhân bệnh đái tháo đường (ĐTĐ), trong đó 42,2% ở bệnh nhân ĐTĐ típ 2 và 29,1% ở bệnh nhân ĐTĐ túp 1 [2]
Biến chứng thần kinh ngoại biên do đái tháo đường (Diabetic polyneuropathy-PDN) tăng theo tuổi và thời gian mắc bệnh. Đi kèm với tỷ lệ biến chứng thần kinh là các biến chứng mạch máu lớn và mạch máu nhỏ như bệnh thận ĐTĐ, bệnh võng mạch ĐTĐ, bệnh động mạch ngoại biên…[5]
Đau là một trong những biểu hiện chính của bệnh thần kinh ngoại biên do ĐTĐ và đây là một trong những nguyên nhân gây tàn phế và giảm chất lượng sống bệnh nhân ĐTĐ
Một nghiên cứu theo dõi dọc trên 360,559 bệnh nhân ĐTĐ từ năm 2010-2015 cho thấy có 23,5% bệnh nhân có biến chứng thần kinh ngoại biên kèm đau và 4,8% có biến chứng thần kinh ngoại biên không kèm đau. Nghiên cứu cũng cho thấy tỷ lệ cắt cụt chi ở nhóm đau do bệnh thần kinh ngoại biên cao gấp 16,24 lần so với nhóm bệnh nhân đái tháo đường không có biến chứng thần kinh ngoại biên [5]
Theo Hiệp hội Quốc tế nghiên cứu về đau “Đau là cảm giác khó chịu và sự trãi nghiệm về cảm xúc gây nên bởi tổn thương mô có sẵn hay tiềm tàng, hoặc được mô tả theo kiểu của một tổn thương như vậy hoặc cả hai” [6]
Đau trong bệnh lý thần kinh ngoại biên do đái tháo đường là kết quả của tổn thương hoặc rối loạn chức năng của hệ thống thần kinh ngoại biên hoặc trung ương, hơn là kích thích các thụ thể nhận cảm đau. Gợi ý chẩn đoán khi đau không tương xứng với tổn thương mô, rối loạn cảm giác (như bỏng rát, ngứa ran) và các dấu hiệu tổn thương dây thần kinh được phát hiện trong quá trình khám thần kinh
1.2. Phân loại đau theo cơ chế gây đau [6]
– Đau cảm thụ (nociceptive pain): là đau do tổn thương tổ chức (cơ, da, nội tạng…) gây kích thích vượt ngưỡng đau.
Đau cảm thụ có 2 loại: đau thân thể (somatic pain) là đau do tổn thương mô da, cơ, khớp… và đau nội tạng (visceral pain) là đau do tổn thương nội tạng.
- Đau thần kinh (neuropathic pain): Là chứng đau do những thương tổn nguyên phát hoặc những rối loạn chức trong hệ thần kinh gây nên.
Đau thần kinh chia 2 loại: đau thần kinh ngoại vi (peripheral neuropathic pain) do tổn thương các dây hoặc rễ thần kinh (Ví dụ: đau sau herpes, đau dây V, bệnh thần kinh ngoại vi do đái tháo đường, bệnh thần kinh ngoại vi sau phẫu thuật, bệnh thần kinh ngoại vi sau chấn thương…); đau thần kinh trung ương (central neuropathic pain) do tổn thương ở não hoặc tủy sống (ví dụ: đau sau đột quỵ não, xơ não tủy rải rác, u não, chèn ép tủy…)
- Đau hỗn hợp (mixed pain): gồm cả 2 cơ chế đau cảm thụ và đau thần kinh. Ví dụ: đau thắt lưng với bệnh lý rễ thần kinh, bệnh lý rễ thần kinh cổ, đau do ung thư, hội chứng ống cổ tay…
- Đau do căn nguyên tâm lý (psychogenic pain)
1.3. Cơ chế gây đau thần kinh [3]
Cơ chế bệnh sinh của đau thần kinh: bao gồm các cơ chế ngoại vi và trung ương
- Mẫn cảm hóa ngoại vi: sự nhạy cảm hóa ở ngoại vi của các thụ thể đau sơ cấp (sợi Aδ, sợi
- do sự phóng thích của bradykinin, histamine, prostaglandines và chất
- Hiện tượng ổ phóng điện bất thường của neurone tổn thương: sau tổn thương có hiện tượng mọc chồi thần kinh (neuroma), chính là nơi tích tụ các kênh ion (vd, kênh natri) và các thụ thể (vd, norepinephrine) bình thường và bệnh lý, dẫn đến sự xuất hiện của các ổ tăng kích hoạt hoặc tự phóng điện bất thường tại nơi tổn thương. Hiện tượng này có thể gặp dọc theo sợi trục, bệnh nhân có các cơn đau nhói như điện giật ngay tại các vùng mất cảm giác.
- Hiện tượng viêm thần kinh: Áp lực, tổn thương tế bào phóng thích các chất K+, PG, BK Dẫn truyền tới tủy sống gây phóng thích chất P, Bradykinin, Histamin, 5HT tăng độ nhạy cảm của các neuron lân cận. – Hiện tượng giao thoa các sợi trục thần kinh (cross-
talking) xảy ra khi một neurone của đường dẫn truyền cảm giác đau bị tổn thương, các neurone tiếp hợp với neurone này vẫn tiếp tục phóng điện.
- Giảm hoạt động của đường ức chế hướng xuống, xuất phát từ trung não, cầu và hành não (chất dẫn truyền thần kinh gồm serotonin, norepinephrine).
- Các tổn thương, thoái hóa, tiếp theo đó là hiện tượng tái sinh hoặc tái tổ chức lại tại tủy sống, gây ra những kết nối sai lầm hoặc những kích thíh hướng tâm quá mức như sự mọc chồi của các sợi Aβ vào trong các lớp nông của sừng sau tủy (laminae I & II), mất các kiểm soát ức chế trên các lớp nông của sừng sau tủy: giảm hoạt động của các nơron trung gian ức chế có tại khoanh tủy (chất chất dẫn truyền thần kinh gồm có GABA, glycine, enkephalins).
2. CHẨN ĐOÁN ĐAU TRONG BỆNH THẦN KINH NGOẠI BIÊN DO ĐTĐ [4]
Đánh giá đau cần được xem xét thông qua các thông tin cơ bản sau:
Biểu hiện khu trú đau? (khuyếch tán hay lan truyền).
Tính chất đau? (Như kim châm, ẩm ướt, bỏng rát).
Mức độ đau? (chịu được, không chịu
được).
Thời gian xuất hiện và tồn tại cơn đau? (cấp tính, tản mạn, tái phát, kéo dài, mạn tính).
Tình trạng đau? (yên lặng, căng thẳng, khi nằm, khi ngồi, khi đứng, khi đi).
Triệu chứng đi kèm với đau? (chóng mặt, nhịp tim nhanh).
Thông tin khác? (tuổi, nghề nghiệp, thói quen trong sinh hoạt…).
Đau thần kinh thường gây đau mạn tính Vị trí khu trú đau không rõ ràng
Đan xen giữa các triệu chứng âm tính (giảm cảm giác), triệu chứng dương tính (tăng cảm đau, loạn cảm đau) và biểu hiện rối loạn thần kinh thực vật (thay đổi màu da, dày móng, ra mồ hôi lạnh, phù…) trên cùng một vùng chi phối thần kinh
Tính chất và cường độ đau: thường đau rất dữ dội. Cảm giác đau bỏng cháy, đau như dao đâm, đau như điện giật, đau giằng xé…
Có thể đau tự phát (stimulus – independent pain) hoặc đau do kích thích (stimulus evoked pain). Các kích thích thông thường không gây đau ở người bình thường lại có thể gây bùng phát đau ở bệnh nhân đau thần kinh.
Các loại thuốc giảm đau truyền thống (thuốc giảm đau không steroid, corticoid…) không có tác dụng giảm đau
Bảng 1. Cách khám chức năng từng sợi thần kinh cảm giác
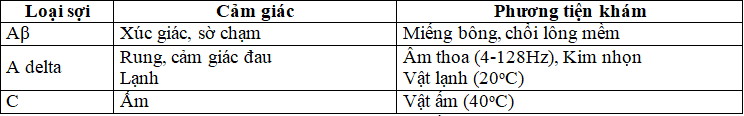
Tăng cảm đau (Hyperalgesia): là tình trạng tăng đáp ứng kích thích đau với những kích thích dưới ngưỡng gây đau. Theo loại kích thích, có thể chia tăng cảm đau thành các loại tăng cảm đau cơ học (mechanical hyperalgesia), tăng cảm đau hóa học (chemical hyperalgesia) và tăng cảm đau nhiệt độ (thermal hyperalgesia).
Loạn cảm đau (Allodynia): là tình trạng xuất hiện đau với ngay các kích thích vô hại (non-noxious stimulus). Loạn cảm đau là một dạng đặc biệt của tăng cảm đau.
Dị cảm (Paresthesia): xuất hiện các cảm
giác bất thường không do kích thích từ bên ngoài: ví dụ cảm giác kiến bò, kim châm, tê buồn…
Đau tự phát/ đau không phụ thuộc kích thích (stimulus – independent pain): cơn đau bùng phát tự nhiên, không cần kích thích từ bên ngoài.
Đau do kích thích (stimulus – evoked pain): đau khi có kích thích từ bên ngoài (cơ học, nhiệt, hóa học).
- Thang điểm đau(pain scale): gồm 10 mục đánh giá
- Không đau.
- Đau rất nhẹ, hầu như không cảm nhận và nghĩ đến nó, thỉnh thoảng đau nhẹ.
- Đau nhẹ, thỉnh thoảng đau nhói mạnh.
- Đau làm người bệnh chú ý, mất tập trung trong công việc, vẫn thể thích ứng với nó.
- Đau vừa phải, bệnh nhân có thể quên đi cơn đau nếu đang làm việc.
- Đau nhiều hơn, bệnh nhân không thể quên đau sau nhiều phút, bệnh nhân vẫn có thể làm việc.
- Đau vừa phải nhiều hơn, ảnh hưởng đến các sinh hoạt hàng ngày, khó tập
- Đau nặng, ảnh hưởng đến các giác quan và hạn chế nhiều đến sinh hoạt hàng ngày của bệnh nhân. Ảnh hưởng đến giấc ngủ.
- Đau dữ dội, hạn chế nhiều hoạt động,
cần phải nỗ lực rất nhiều.
- Đau kinh khủng, kêu khóc, rên rỉ không kiểm soát được.
- Đau không thể nói chuyện được, nằm liệt giường và có thể mê sảng.
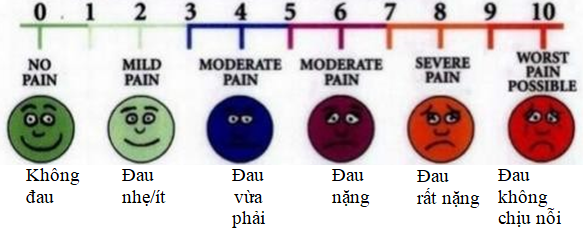
- Thang điểm cường độ đau dạng nhìn (Visual Analog Scale- VAS)
Thang điểm có 2 mặt dài 20cm, mặt không đánh dấu quay về phía bệnh nhân biểu thị mức độ đau để bệnh nhân dễ đối chiếu (Một đầu quy định không đau, đầu kia quy định rất đau); mặt đối diện về phía thấy thuốc có chia thành 10 vạch (0-10). Bệnh nhân được yêu cầu và định vị con trỏ trên thước tương ứng mức độ đau của mình. Khoảng cách từ chỗ bệnh nhân chỉ đến điểm không chính là điểm VAS.
Hình 1. B
Theo hình tượng chia ra làm 5 mức độ tương ứng như sau:
- 0: Không đau
- 1-3: Đau ít
- 4-6: Đau vừa phải
- 6-8: Đau nặng
- 8-10: Đau không chịu nỗi
Theo Tổ chức Y tế thế giới chia 3 mức: đau nhẹ/ít (1- 3), đau vừa (4- 6), đau nặng 7 – 10).
Điểm VAS từ 4 trở lên là phải điều trị đau cho bệnh nhân. Dựa vào thang điểm VAS đánh giá tác dụng giảm đau theo Oates như sau: Tốt thì điểm đau từ 0-<2,5 điểm, Khá: từ 2,5- <4,0 điểm, Trung bình từ 4,0-<7,5 và kém từ 7,5-10 điểm.
Thang điểm cường độ đau dạng số (Numerical rating scale- NRS)
- Thang điểm đau theo vẻ mặt của Wong- Baker (Wong-Baker faces rating scale – FRS)
- Tiêu chuẩn chẩn đoán đau thần kinh của Nhóm nghiên cứu đau liên hiệp Anh (2002): chẩn đoán đau thần kinh khi có ít nhất 2/5 triệu chứng
- Tăng cảm đau (hyperalgesia)
- Loạn cảm đau (allodynia)
- Đau cháy(burning pain)
- Đau như đâm (shooting pain)
- Bệnh nhân dễ bị đau, đau như xuyên, như đâm, như điện giật, cháy bỏng, rát…
- Thang điểm S-LANNSS (Leeds Assessment of Neuropathic Symptoms and
Signs) của Bennet năm 2005 dùng cho bệnh nhân tự đánh giá triệu chứng. Áp dụng trong các nghiên cứu sàng lọc đau thần kinh trong cộng đồng.
- Bảng câu hỏi đau thần kinh (Neuropathic pain questionnaire – NPQ) gồm 12 câu hỏi. Ứng dụng chẩn đoán phân biệt giữa đau thần kinh với các loại đau khác.
- Thang điểm DN4 (Douleur Neuropathique en 4 questions) nêu ra 10 triệu chứng. Chẩn đoán đau thần kinh nếu có ≥ 4/10 triệu chứng.
3. ĐIỀU TRỊ ĐAU TRONG BỆNH LÝ THẦN KINH NGOẠI BIÊN DO ĐTĐ
- Mục tiêu điều trị đau
- Làm giảm đau:
+ Điều trị nguyên nhân.
+ Sử dụng tối ưu thuốc giảm đau.
- Điều trị các triệu chứng kèm theo (mất ngủ, rối loạn cảm xúc).
- Phục hồi chức năng, cho phép bệnh nhân trở lại với các hoạt động trong cuộc sống hàng ngày.
3.2. Điều trị dùng thuốc [7]
Các nhóm thuốc sau có thể giúp kiểm soát cơn đau liên quan đến DPN: thuốc chống động kinh (AED), chất ức chế tái hấp thu serotonin- norepinephrine (SNRI) và thuốc chống trầm cảm ba vòng (TCAs). Theo khuyến cáo của ADA về xử trí DPN, các thuốc được FDA chấp thuận bao gồm Pregabalin và Duloxetine. Pregabalin và Duloxetine có thể được coi là phương pháp điều trị đầu tay đối với các cơn đau liên quan đến DPN. Các Opioid không điển hình như Buprenorphine qua da, Tapentadol và Tramadol không được khuyến cáo là liệu pháp điều trị đầu tiên hoặc thứ hai mặc dù có những rủi ro và cơ chế tác dụng khác nhau đối với các Opiod khác.
Thuốc chống trầm cảm ba vòng như
Amitriptyline, Duloxetine, và Nortriptyline có thể được sử dụng nhưng thận trọng do tăng nguy cơ phản ứng có hại. Thuốc chống viêm không steroid có thể được sử dụng như liệu pháp ngắn hạn. Gabapentin, Desipramine, và Venlafaxine không được FDA chấp thuận để quản lý cơn đau liên quan đến DPN, nhưng chúng cũng được kê đơn điều trị .
Khuyến cáo của ADA trong điều trị đau trong bệnh lý thần kinh ngoại biên do ĐTĐ
Xem xét Pregabalin hoặc Duloxetine là phương pháp tiếp cận ban đầu trong điều trị triệu chứng đau thần kinh do đái tháo đường (mức độ bằng chứng A)
Gabapentin cũng có thể được sử dụng như một phương pháp tiếp cận ban đầu hiệu quả, có tính đến tình trạng kinh tế xã hội của bệnh nhân, các bệnh đi kèm và các tương tác thuốc có thể xảy ra (mức độ bằng chứng B)
Mặc dù không được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận, thuốc chống trầm cảm ba vòng cũng có hiệu quả đối với chứng đau thần kinh ở bệnh nhan ĐTĐ nhưng nên sử dụng thận trọng vì nguy cơ tác dụng phụ nghiêm trọng cao hơn. (mức độ bằng chứng B)
Do nguy cơ cao gây nghiện và các biến chứng khác, việc sử dụng Opioid, bao gồm Tapentadol hoặc Tramadol, không được khuyến cáo như là thuốc thứ nhất hoặc thứ hai để điều trị cơn đau liên quan đến bệnh thần kinh ngoại biên do đái tháo đường. (mức độ bằng chứng E)
Bảng 2. Các thuốc điều trị đau thần kinh và cách dùng
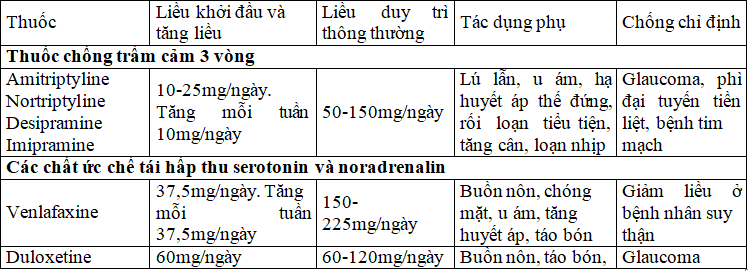
Bảng 3. Hướng dẫn lựa chọn thuốc điều trị một số đau thần kinh của Liên Hội thần kinh châu Âu và Hiệp Hội nghiên cứu đau quốc tế [1]

3.3. Các phương pháp điều trị đau không dùng thuốc
- Các can thiệp ngoại khoa: Là các biện pháp xâm nhập, tác dụng giảm đau thực sự cũng như những tác dụng phụ không mong muốn vẫn còn gây nhiều tranh cãi
- Phẫu thuật DREZ hay cắt chọn lọc rễ thần kinh cảm giác. Chỉ định trong tổn thương đám
rối cánh tay, liệt tứ chi, có triệu chứng đau thần kinh rõ liên quan đến vị trí thương tổn. Kết quả tốt trong khoảng 5 năm.
- Phong bế thần kinh giao cảm
- Kích thích tủy sống bằng điện cực
- Bơm nội tủy: đưa thuốc trực tiếp vào dịch não tủy (Opioid, clonidine, ziconotide, baclofen).
- Kích thích vỏ não vận động. Chỉ định trong đau do bệnh lý thần kinh trung ương, đau kiểu “chi ma” sau cắt cụt
- Kích thích não sâu
3.4. Các điều trị khác
-Tâm lý trị liệu Khi bệnh nhân có các sang chấn về tâm lý kèm theo, giúp giảm stress, căng thẳng.
- Can thiệp thay đổi nhận thức-hành vi Nhằm kiểm soát tình trạng đau mạn tính. Bệnh nhân được hướng dẫn, giáo dục, cung cấp các kiến thức hiểu biết về sinh lý đau bình thường và rối loạn, giúp họ thiết lập các mục tiêu điều
trị, xây dựng chương trình tập luyện vận động cụ thể, các kỹ thuật thư dãn, giảm sự nhạy cảm, thực hành suy nghĩ tích cực.
- Phản hồi sinh học (Biofeedback)
- Dinh dưỡng: ví dụ chế độ ăn cho người đái tháo đường, Vitamin và khoáng chất bổ sung có thể giúp tăng cường hệ thống miễn dịch giúp cung cấp năng lượng.
Nên hạn chế rượu bia, thuốc lá và chất kích thích.
- Các biện pháp trị liệu khác: như châm cứu, thôi miên, thiền cũng có tác dụng trong một số trường hợp.
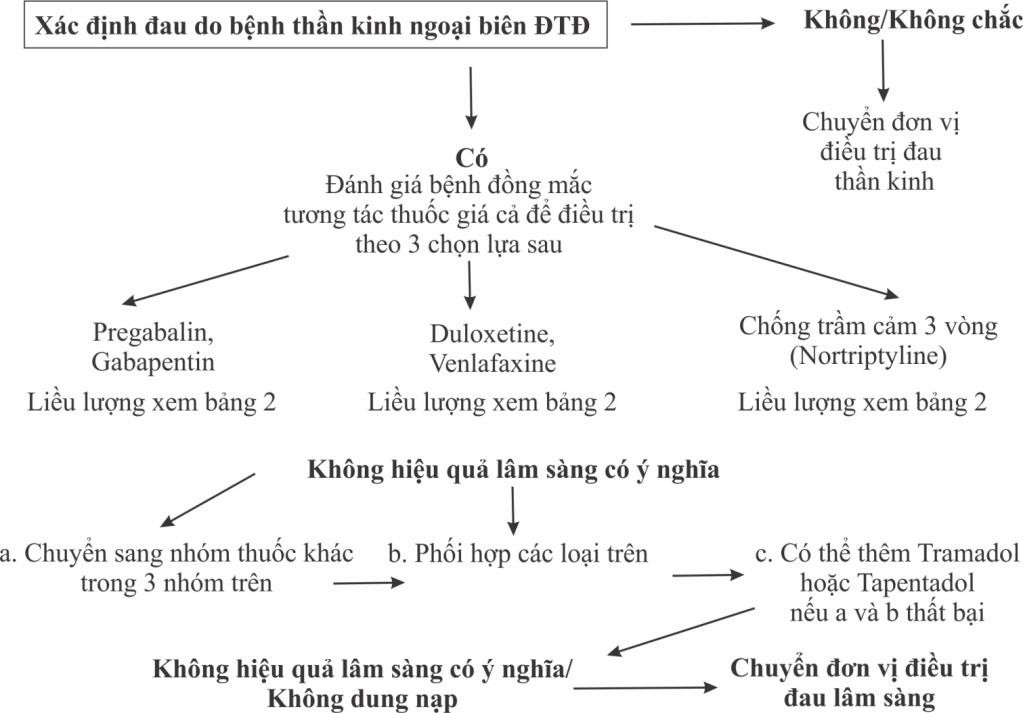
Lược đồ điều trị đau trong bệnh thần kinh ngoại biên do ĐTĐ theo ADA
4. KẾT LUẬN
Bệnh thần kinh ngoại biên là một biến chứng hay gặp trong bệnh đái tháo đường với tần suất gia tăng theo tuổi và thời gian bị bệnh cũng như liên quan đến kiểm soát không tốt đường huyết.
Trong đó đau là một biểu hiện chính của bệnh gây ảnh hưởng rất lớn đến chất lượng sống bệnh nhân điều trị cuãng như gia tăng tàn phế và đoạn chi ở bệnh nhân đái tháo đường.
Nhận diện sớm và điều trị sớm theo nguyên tắc đa mô thức sẽ giúp giảm đau và cải thiện chất lượng cuộc sống cho bệnh nhân đái tháo đường.
TÀI LIỆU THAM KHẢO
- Attal N, Cruccu G, Baron R (2010): EFNS guidelines on the pharmacological treatment of neuropathic pain: 2010 revision, European Journal of Neurology, 17:1113-1123.
- André Pfannkuche et all (2020), Prevalence and risk factors of diabetic peripheral neuropathy in a diabetics cohort: Register initiative “diabetes and nerves” Endocrine and Metabolic Science, Volume 1, Issues 1–2
- Jane C., Ballantyne et all (2011): Nonspecific Treatment Effects in pain medicine, Pain clinical updates (IASP), XIX, Issue 2, pp.1-8.
- Kampman K., Jarvis M. (2015): American Society of Addiction medicine: National Pratice Guideline for the use of medications in the treatment of addiction involving opioid
- Musa Kiyan et all (2020) Painful diabetic peripheral neuropathy: Health care costs and complications, Neurol Clin Pract Feb;10(1):47-57
- Russell K., Portenoy, Ronald M.Kanner (2011): Pain management: Theory and practice; A. Davis Company Phyladelphia.
- Rodica et all (2017). Diabetic Neuropathy: A Position Statement by the American Diabetes Association. Diabetes Care Jan; 40(1): 136-154.
- Boussageon, R., Bejan-Angoulvant, , SaadatianElahi, M., Lafont, S., Bergeonneau, C., Kassai, B.et al. (2011) Effect of intensive glucose lowering treatment on all cause mortality, cardiovascular death, and microvascular events in type 2 diabetes: metaanalysis of randomised controlled trials. BMJ 343:d4169.
- Brederson, J., Kym, P. and Szallasi, A. (2013) Targeting TRP channels for pain relief. Eur J Pharmacol 716: 61–76.
- Brennan, M.J. (2013) The effect of opioid therapy on endocrine function. Am J Med 126: S12–S18.
- Rice, A., Dworkin, R., McCarthy, T., Anand, P.,Bountra, C., McCloud, P. et al. (2014) EMA401, an orally administered highly selective angiotensin II type 2 receptor antagonist, as a novel treatment for postherpetic neuralgia: a randomised, double-blind, placebocontrolled phase 2 clinical trial. Lancet 383: 1637–1647
- Lunn, M., Hughes, R. and Wiffen, P. (2014) Duloxetine for treating painful neuropathy, chronic pain or fibromyalgia. Cochrane Database Syst Rev (1): CD007115.
- Mahoney, J., Vardaxis, V., Moore, J., Hall, A., Haffner, K. and Peterson, M. (2012) Topical ketamine cream in the treatment of painful diabetic neuropathy: a randomized, placebo-controlled, double- blind initial study. J Am Podiatr Med Assoc 102: 178–183.
- Malik, R., Tesfaye, S. and Ziegler, D. (2013) Medical strategies to reduce amputation in patients with type 2 diabetes. Diabet Med 30: 893–900
- Tesfaye, S., Wilhelm, S., Lledo, A., Schacht, A., Tolle, T., Bouhassira, D. et al. (2013) Duloxetine and pregabalin: high-dose monotherapy or their combination? The ‘COMBO-DN Study’ – a multinational, randomized, double- blind, parallelgroup study in patients with diabetic peripheral neuropathic pain. Pain 154: 2616–2625.
- Thakral, G., Kim, P., Lafontaine, J., Menzies, R., Najafi, B. and Lavery, L. (2013) Electrical stimulation as an adjunctive treatment of painful and sensory diabetic neuropathy. J Diabetes Sci Technol 7: 1202–1209
- Galloway, C. and Chattopadhyay, M. (2013)Increases in inflammatory mediators in DRG implicate in the pathogenesis of painful neuropathy in type 2 diabetes. Cytokine 63: 1–5.
- Garrow, A., Xing, M., Vere, J., Verrall, B., Wang, L. and Jude, E. (2014) Role of acupuncture in the management of diabetic painful neuropathy (DPN): a pilot RCT. Acupunct Med 32: 242–249.
 Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam
Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam Hội Nội Tiết – Đái Tháo Đường Miền Trung Việt Nam